Сульфаты щелочных металлов, и в частности кристаллы
K 2 SO 4
кристаллизируются в виде орторомбических кристаллов с пространственной
группой симметрии
D 16. Сульфаты щелочных металлов прозрачны в широком
Для исследования электронных возбуждений неактивированного кристалла сульфата калия в работе была исследована люминесценция
кристалла
K 2 SO 4. Измеренный спектр люминесценции состоял из двух
условных частей: из длинноволновой полосы, которая является широкой структурной полосой и коротковолновой части, которая состоит из ряда узких полос [2].
Как известно [1] элементарная ячейка
K 2 SO 4
содержит четыре формульные
единицы, при этом, попарно они имеют разное пространственное распределение, что приводит к давыдовскому расщеплению в спектрах фундаментального поглощения. Благодаря молекулярному аниону у сульфатов, для них характерно наличие ярко выраженных молекулярных колебаний. Что приводит к вибронной структуре спектра. Сравнение энергий переходов в
молекуле
SO2-
с максимумами в спектре люминесценции позволяют заключить,
молекулы
SO2-
известно, что самым высоколежащим заполненным состоянием
2 a 1. А нижним пустым
4 t 2, при этом энергия перехода
между ними составляет 9-10 эВ [3, 4], что очень близко к энергии
длинноволнового максимума
(EM» 8,6 эВ). Разницу между этими энергиями
можно связать с влиянием характеристического поля на энергетические уровни
иона
SO2-. Природа коротковолновых максимумов, вероятно, связана с
как группа
D 2 h имеет только одномерные неприводимые представления.
Спектр рентгенолюминесценции кристалла
K 2 SO 4, при температуре 4,2 К
состоит из интенсивной коротковолновой полосы с энергией 3,8 эВ (ее полуширина 0,3 эВ) и широкой длинноволновой, со структурой при энергиях 3,1, 2,6, 2,3 эВ.
Температурная зависимость коротковолновой и длинноволновой полос при температуре выше 50 К схожа. В этой области наблюдается быстрое тушение этих полос. В интервале температур от 4,2 К до 50 К коротковолновое свечение незначительно тушиться, а длинноволновое разгорается.
Во время исследования спектра возбуждения, было замечено, что свечение коротковолновой полосы с наибольшей эффективностью возбуждается в области экситонного и зона-зонного поглощения. Свечение коротковолновой
полосы безинерционно в интервале времени больше 1 сек. Все это может быть следствием того, что наблюдаемое свечение является экситонным, т.е. природа коротковолновой полосы связана с излучательной рекомбинацией экситона. Значительные стоксовские потери являются следствием сильной экситон- фононной связи и показывает что излучательный переход экситона происходит после колебательной релаксации возбужденного состояния, т.е. из автолокализованного состояния [5].
Длинноволновое свечение возбуждается с большей интенсивностью в области прозрачности основания, оно было связано с неидентифицированной примесью либо с собственным дефектом. Это же свечение, но с меньшей эффективностью возбуждается в области фундаментального поглощения. Это связывается с миграцией энергии от основания благодаря подвижности экситонов или электронно-дырочных пар к примеси или собственному дефекту [14].
В работе [6] были исследованы спектры люминесценции кристаллов
K 2 SO 4,
Rb 2 SO 4
при температуре жидкого азота. Показано, что структура обоих
основания, а связаны с возбуждениями анионов анионным экситоном.
SO2-, т.е. с так называемым
Анализ теоретических расчетов заполненных состояний иона
SO2-
2 a 1, а нижнее
пустое состояние зоны проводимости
4 t 2. Энергия перехода между этими
состояниями составляет 10 эВ. Проведенный анализ показывает, что зона
проводимости сульфатов будет образовываться из состояний анионов.
4 t 2
состояний катионов и s
Оценка энергии переходов зона-зона примерно 9 эВ. В спектрах
люминесценции имеются характерные ступеньки при 9,4 эВ для
K 2 SO 4
и 9,25
для
Rb 2 SO 4, которые связывают с началом межзонных переходов.
Длинноволновые максимумы сопоставляются с переходами в экситонные состояния. Для длинноволновых максимумов энергия связи экситонов
составляет 0,8 эВ для
K 2 SO 4
и 0,65 для
Rb 2 SO 4. Эти величины соответствуют для
анионных экситонов малого радиуса. Структура в длинноволновых полосах связана с расщеплением экситонных уровней в кристаллическом поле низкой симметрии.
Приведенные в работе [6] экспериментальные данные показывают, что экситонные состояния в ионных кристаллах с комплексным анионом связаны с электронными переходами внутри сложных анионов.
В работе [7] спектры люминесценции кристалла
Na 2 SO 4
были исследованы
при помощи не ионизирующей фотостимулированной люминесценции и ионизирующей рентгенолюминесценции в спектральной области 200-800 нм при комнатной температуре, для определения изменения свойств множеств стабильных фаз этого кристалла. А так же несколько измерений
рентгенолюминесценции кристалла предварительно нагретого до 400 К в течении одного часа.
Исследованный спектр ФСЛ состоит из множества взаимно перекрываемых полос. Максимумы этих полос 330, 345, 385, 460 и 630 нм. Спектр РЛ хоть и имеет другую форму, но также состоит из пяти полос с максимумами 320, 360, 425, 500 и 600 нм. Спектр РЛ у предварительно нагретых образцов до 400 С, хоть и отличается от спектров ФСЛ и РЛ по форме, но состоит из тех же пяти полос с максимумами на тех же позициях что и в спектре РЛ при комнатной температуре. При термальном воздействии пик 5 увеличился, а пик 4 уменьшился. Разные формы спектров возможно относятся к трансформации которая имеет место в структуре, как следствие перехода фаз I
→II →III при нагреваний. Как известно [8] фаза III метастабильна при комнатной температуре и обычном атмосферном давлении и медленно переходит в фазу V. Спектр измерен по истечении 30 минут после достижения комнатной температуры, и это подтверждает, что кривая соответствует фазе III
кристалла
Na 2 SO 4. Так изменение чувствительности относительной
интенсивности в обоих исследованиях РЛ относиться к самодиффузий натрия на щелочном основании при процессах переноса заряда, которое в следствии порождают фазовые переходы.
Одинаковое количество полос излучения при ФСЛ, РЛ и РЛ при 400˚С, предполагает, что одинаковые центры рекомбинации используются в обоих процессах для обоих фаз. А основные отличия в характеристике ФСЛ могут относиться к внутренним механизмам процессов проходящих главным образом в пустых ловушках. Слабая энергия инфрокрасного излучения освобождает дырки из центров люминесценции, что является источником: 1) возврат в ловушку путем превращения в ловушку другого центра или 2) возврат на место путем излучения возбужденного активатора. С другой стороны рентгеновские лучи обладают более высокой проникающей способностью чем инфрокрасное излучение и возбуждают дырки в объеме кристалла, вызывая прямую рекомбинацию электронов и дырок на центрах свечения и вследствие этого интенсивность при РЛ выше.
Также была исследована термостимулированная люминесценция,
кристалла
Na 2 SO 4. Было обнаружено важное свечение в синей области (380 нм)
при 230-240˚С. В кристалле
Na 2 SO 4
в температурном диапазоне 180-240˚С
показаны три стабильные фазы (V, III и I), одна метастабильная фаза (II) и одна нестабильная (IV). По этому низкотемпературный максимум ТСЛ достигающий пика при 235˚С, может коррелировать с процессом переноса заряда, который возникает из за структурных превращений из V в I фазу. Скачок электропроводности для данного образца произошедший при температуре 240˚С, хорошо согласуется с появлением низкотемпературного пика ТСЛ. Когда температура растет выше 240˚С остается стабильной только фаза 1.
В стабильной фазе положение атомов натрия и серы похожи, но основное отличие связано с тем, что сульфаты тетраэдрические и эти атомы в них направленно разупорядоченны.
1.2 Приместные излучения сульфатов щелочных металлов
Сульфат кальция, активированный диспрозием представляет большой интерес в качестве твердотельного термолюминесцентного дозиметрического материала. Исследование термостимулированной люминесценций активированных диспрозием сульфатов щелочных металлов показало, что при
облучении люминофора ионы
Dy 3+могут являться ловушкой электронов и
трансформироваться до формы
Dy 2+. В процессе термостимулированной
люминесценции подвижная дырка рекомбинирует с ионом
Dy 2+, появившийся в
результате этого ион
Dy 3+
переходит в возбужденное состояние с энергией
соответствующей энергии рекомбинации. Релаксация иона в основное
состояние дает характеристические полосы свечения природе встречается в трехвалентном состоянии [9].
Dy 3+. Диспрозий в
В работе [10] исследована люминесценция кристалла
LiNaSO 4: Eu,
методами термостимулированной люминесценции и фотолюминесценции. В результате этого, при помощи обоих методов было обнаружено сильное
излучение ионов излучение ионов
Eu 3+. После облучения (51 С/Kg) было обнаружено слабое
Eu 2+, что наглядно демонстрирует наличие слабого
Eu 3+® Eu 2+превращения. После этого, при нагреве кристаллов для измерения
кривой свечения, излучение ионов
Eu 2+
отсутствовало. Это может быть связано
с парой
Eu 3+- Eu 2+, т.е. ионы
Eu 3+
замещают ионы натрия, а ионы
Eu 2+занимают положение по соседству с ионами лития.
Облучение порождает дырочные центры захвата, такие как
O -.
Вместе с тем, совместно с дырочными центрами захвата должны создаваться и электронные центры захвата, но природа их создания именно в таком ключе, еще не определена.
В работе [11], авторами исследовалась термостимулированная
люминесценция и фотолюминесценция
LiNaSO 4: Eu
облученного ионным
пучком
7 Li
с энергиями 24 и 48 МеВ. При исследовании
термостимулированной люминесценции, у облученных кристаллов обнаружены пики разгорания при температурах 412 и 481 К. Эти отличия могут быть связаны с изменением населенности центров люминесценции при
имплантировании в решетку кристалла
LiNaSO 4: Eu
ионов 7 Li
при облучении,
которые в свою очередь могут стать основами для центров люминесценции и центров захватов. Внедренная примесь европия была определена в виде двухвалентного и трехвалентного ионов. Имплантация ионов лития в матрицу усложняет дальнейший процесс по исследованию термостимулированной люминесценции и формирование имплантацией лития постоянных дефектов делают такие образцы непригодными для повторного применения.
Исследование воздействия ионов
Er 3+
и Yb 3+
внедренных в кристаллы
LiNaSO 4, на структурные и нелинейные оптические свойства этих кристаллов сделано в работе [12]. Была проведена работа по количественному и качественному исследованию температуры фазового перехода, и нелинейных
оптических свойств второго порядка чистого и активированного (ионами
Er 3+и
Yb 3+) кристалла сульфата лития и калия. Показано, что длина связи между центральным атомом и внедренным ионом и температура фазового перехода тесно связана с местоположением атомов, т.е. ионом примеси оказывает
большее влияние на участок где находится ион
Na 1+
чем на участок с ионом
Li 1+. Более того, замещение в кристалле
LiNaSO 4 ионе
Na 1+
ионами
Er 3+ и
Yb 3+уменьшает нелинейный оптический выход второго порядка и сегнетоэлектрическую температуру, зависимость которых линейна.
Магнитные свойства ионов
Tl 2+в кристаллах
K 2 SO 4
исследованы в работе
[13]. При температуре жидкого азота стабильность магнитных центров
Tl 2+
оказалось высокой. Анализируя структуру кристалла
K 2 SO 4
было
предположено, что исследованные магнитные центры
Tl 2+
замещают
К + в
положении
К 1 и имеют нелокальную компенсацию заряда.
В работе [14] были исследованы поглощение, излучение и термостимулированная люминесценция в кристаллах сульфатов щелочных металлов активированных медью.
Полосы ультрафиолетового поглощения, обнаруженные в области 4,6-5,4
эВ, в кристаллах активированных медью, в основном характерны запрещенным
3 d ® 4 s
переходам иона
Cu +, которые являются частично разрешенными для
кристаллов с фононным взаимодействием [15, 16, 17, 18]. Полосы поглощения
соответствуют разрешенным
s ® p
переходам, наблюдаемым в области
вакуумного ультрафиолета. О том что медь входит в сульфаты щелочных металлов в двухвалентном состоянии, известно из ранних работ по исследованию ЭПР [19, 20]. Из спектра оптического поглощения необлученного образца можно сделать вывод, что медь входит в решетку сульфата в двух видах: в одновалентном и двухвалентном состояний [14].
После облучения, в кристаллах
Cs 2 SO 4: Cu
и K 2 SO 4: Cu
интенсивность
полосы поглощения иона
Cu 2+
возрастает, что является свидетельством того,
что электрон захватывается на ионе Cu 2+
в матрице кристалла (Рисунок 1.1)
Похожее превращение
Cu 2+® Cu + под воздействием ионизирующего
излучения показано для
LiNbO 3
[21]. Уменьшение интенсивности полос ионов
Cu + при облучении, в случае с
RbSO 4: Cu
должно приписываться к захвату
электрона ионом
Cu +
и превращение в
Cu 0. Превращение
Cu + ® Cu 2+, после
облучения кристалла, дает полосу поглощения, соответствующую
Cu 2+ в
ближней инфракрасной области. Такое же превращение
Cu + ® Cu 0
при
облучении было показано в работе [20]. В результате, можно сделать вывод,
что оба иона металлов.
Cu +
и Cu 2+могут захватывать электроны в сульфатах щелочных
В работе [22] исследованы различные оптические свойства и термостимулированная люминесценция кристаллов сульфатов щелочных
металлов активированных таллием. Ионы
Tl +
находятся в
6 s 2
основном
электронной конфигурации. Этот тип иона характеризуют
тремя полосами поглощения, которые обозначаются как А, B, и C. Полоса С
соответствует разрешенному дипольному переходу в возбужденный уровень
0,04
 0,03
0,03
0,02
0,01
0,00
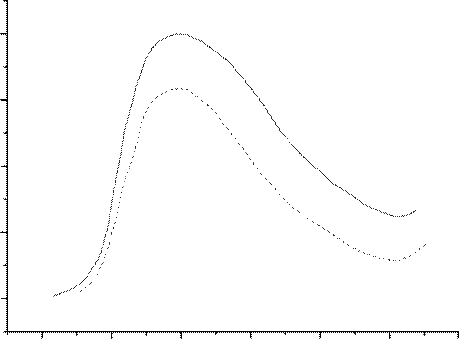
1,3 1,4 1,5 1,6 1,7 1,8 1,9
energy, eV
Рисунок 1.1 – Оптическое поглощение кристалла
K 2 SO 4: Cu. а) необлученный
образец, б) образец облученный g -лучами с энергией 255,4 С/kg (0,99 MR) [14]
K 2 SO 4: Tl,
Cs 2 SO 4: Tl и
Rb 2 SO 4: Tl
в ультрафиолетовой области спектра могут относиться к
S 0® Р 1
разрешенному переходу иона
Tl +. Спектр поглощения кристаллов сульфатов
щелочных металлов активированных таллием был так же исследован в работе
[23], и была обнаружена только одна полоса поглощения в области 5,8 эВ.
Исследования оптического поглощения облученных кристаллов сульфатов щелочных металлов активированных таллием дают примерно такие же результаты. Но было обнаружено плечо в области 5,5-5,6 эВ, вместе с
уменьшением интенсивности полосы С иона
Tl +, что демонстрирует, что в
кристаллической решетке некоторые из ионов
Tl +, под воздействием
высокоэнергетического облучения захватывают дырку или электрон и
превращаются
Tl 2+и
Tl 0
соответственно. Delbecq и соавторы в работах [24, 25]
рассматривали формирование обоих Tl 2+и Tl 0
ионов в кристалле
KCl: Tl. Но оба
найденных центра были нестабильны при комнатной температуре. Позднее
Butterworth с соавторами [26] было показано, что в кристалле
KCl: Tl
под
воздействием рентгеновского излучения могут изменить валентность, все ионы
Tl +
и увеличивается концентрация F центров. Ионы
Tl 0
сформированные в
исследованиях оказались стабильными при комнатной температуре.
Но в данном контексте будет более уместной работа [27] по исследованию
ЭПР кристаллов
K 2 SO 4: Tl
и Rb 2 SO 4: Tl. Они получили стабильные линии ЭПР
ионов
Tl 2+
при температуре 77 К и под воздействием рентгеновских лучей для
данных кристаллов. Примерно, при температуре 250 К ионы
Tl 2+
превращаются в
Tl +
и при комнатной температуре и выше, полосы ЭПР ионов
Tl 2+
не наблюдаются.
Другой фактор, который непременно надо брать в расчет это то, что в этих
и других сульфатах появляются и остаются последствия радиационного повреждения. Они могут быть обнаружены в виде анион радикалов, каждый из которых потерял по электрону, под воздействием излучения в неактивированных сульфатах щелочных металлов [28, 29, 30, 31].
Следовательно, логическим заключением может быть то, что некоторые из
ионов
Tl +
под воздействием облучения захватывают электроны и переходят в
их атомное состояние.
Таким образом, полоса поглощения в области 5,5-5,6 эВ полученная на трех видах кристаллов сульфатов щелочных металлов может относится скорее
к ионам
Tl 0
чем к ионам
Tl +. Спектр оптического поглощения облученных
кристаллов измеренный после начала термолюминесценции показывает аннигиляцию частиц в процессе термостимулированной люминесценции. Механизм изменения валентного состояния примеси напрямую связан с результатами термолюминесценции.
Флуоресценция кристаллов
K 2 SO 4: Tl,
Cs 2 SO 4: Tl
и Rb 2 SO 4: Tl
дает больше
информации о возбужденном энергетическом уровне иона
Tl +. Спектры
который
является основой для поглощения, не является полосой флуоресценции, при комнатной температуре.
Edgerton и Teegarden [32, 33] при облучении светом с длинной волны лежащей внутри полос поглощения A, B и С, кристаллов KI и KCl активированных таллием, обнаружили только одно излучение. Эта полоса излучения полученная у сульфатов щелочных металлов активированных
Tl +
Р 1®
S 0 переходу [24]. Но в работе [32] было предложено, что
уровень
Р 0 достаточно заселен при температурах близких к комнатной и
выше, и поэтому, полученное при комнатной температуре излучение
уровню.
На основе сказанного выше, можно сделать вывод, что излучение в сульфатах щелочных металлов активированных таллием может быть связано с
триплетным состоянием иона
Tl +. Если уровень
1 Р флуоресцирует при
в триплетные уровни. Сильное
излучение, которое наблюдалось при 4 еВ соответствует характеристическому
излучению ионов Tl +
при
3 Р ® 1 S переходе. Позиции уровня
3 Р определяются
1 0 1
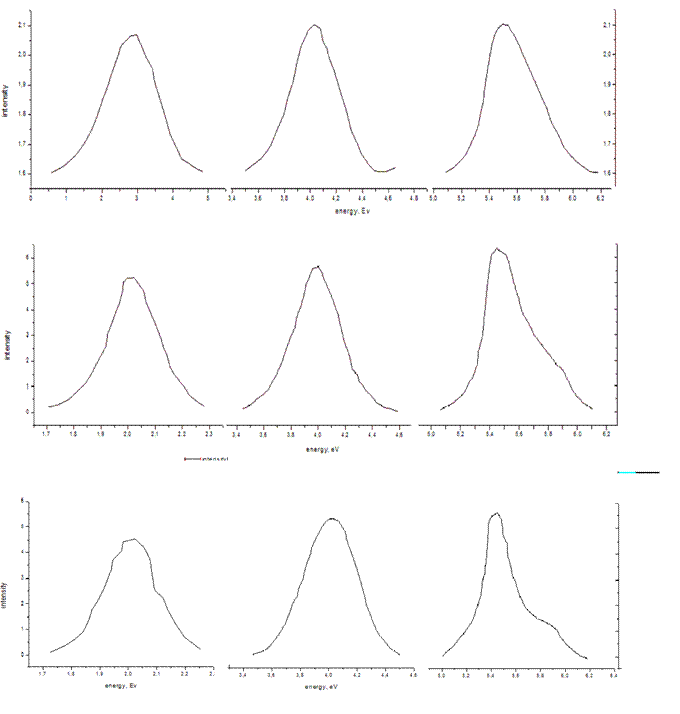 по пику излучения в области 5,4 эВ.
по пику излучения в области 5,4 эВ.
Рисунок 1.2 – Флуоресценция и спектр возбуждения допированное Tl (общая шкала по оси Y). (а) сульфат цезия: 1 и 2 Излучения при возбуждении при 5,44 eV, 3 – Возбуждение для излучения 4 eV, (б) сульфат Рубидия: 1 и 2 Излучения при возбуждении при 5,4 eV, 3 – Возбуждение для излучения 4 eV, (с) Сульфат потазиума 1 и 2 Излучения при возбуждении при 5,44 eV, 3 – Возбуждение для излучения 4 eV [22]
Переходы которые соответствуют поглощению и флуоресценции в трех кристаллах сульфатов щелочных металлов, представлены на конфигурационной координатной диаграмме (рисунок 1.3).
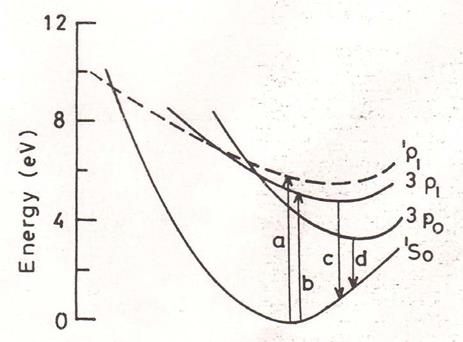
Рисунок 1.3 - Конфигурация координационной схемы для ионов Tl+в щелочных сульфатах. Различные переходы: (а) – С полоса поглощения, (б) – А полоса возбуждения, (с) – Излучения с 3P1 (около 4 eV), (d) - Излучения с 3P0 (около 2,05 eV) [10]
Кривая свечения показывает, что все эти кристаллы имеют комбинацию из трех пиков, при относительно низкой дозе облучения. Кривые свечения могут относиться к термальной мобилизации дырок из анион - радикалов под воздействием облучения. Такая термальная мобилизация и последующая
аннигиляция дырок в кристаллах
CaSO 4
и BaSO 4
была обнаружена в работах
[34, 35]. Термальная стабильность дырочных центров образованных под воздействием излучения в сульфатах щелочных металлов рассматривались в
работах [28, 36]. Было видно, что
O -наименее стабильный радикал, который
Для
SO -
температура термального обесцвечивания приближается к 415 К и
SO -
|
и SO -
дырок, а третий пик
SO -.
Tl +
соответствующий
P 1 ® S 0
переходу. А полоса на 2,4 эВ может относиться
переходу во время флуоресценции.
В работе [37] Gupta с соавторами предложили два возможных механизма рекомбинации центров свечения в сульфатах щелочных металлов. Одним из них является захват электронов на катионе или дефекте кристаллической решетки. Второй механизм подразумевает сценарий, когда примесь ведет себя как электронная ловушка. Во время рекомбинации захваченный электрон освобождается и примесь возвращается в свое первоначальное валентное состояние. Результаты исследования оптического поглощения полностью подтверждают второй механизм. Таким образом, внедренная примесь ведет
себя в качестве электронной ловушки. Механизм формирования атома исчезает во время процесса термолюминесценции.
Tl 0
Это подтверждается исследованием поглощения
Tl 0, которое полностью
исчезает после исследования термостимулированной люминесценции облученных образцов. Это явление объясняется рекомбинацией термально
мобилизованных дырок на Tl 0
(1.1)
Tl 0 + hole ⎯ h ⎯⎯ eat ® Tl +
(1.1)
Освобождение электрона из
Tl 0
под воздействием нагрева маловероятно.
Первый ионизационный потенциал металла таллия в области равен 6 эВ и
нагрев образца не может способствовать освобождению электрона из
Tl 0
центров. Часть рекомбинационной энергии тратится на перевод ионов
Tl + в
возбужденное состояние и он дает характеристическое свечение. Такие же
механизмы в которых ионы Tl +
захватывают электроны при облучении, а за тем
дырки рекомбинируют на том же месте в процессе термостимулированной
люминесценции для кристаллов
KCl: Tl, были представлены в работе [24].
Подразумевая, что
SO -
является дырочным центром, представленный
Спектр остаточного свечения также предполагает существования такого же механизма в представленных излучениях, дырки мобилизуют себя при комнатной температуре.
SO 2- ⎯⎯ irr ® SO - + e -
4 4
Tl + + e -® Tl 0
(1.2)
Tl 0 + SO - ⎯ h ⎯ eat ⎯ ing ®(Tl +)* + SO 2-
4 4
(Tl +)*® Tl + + hn
Ионы таллия входят в кристаллическую решетку сульфатов щелочных металлов в одновалентном состоянии. В спектре оптического поглощения
ионам Tl +
соответствует полоса С. Флуоресценция показывает излучение ионов
Tl +, которое соответствует переходам из уровней
3 P и
3 P на
1 S уровень.
небольшой части внедренных в решетку ионов
Tl +.
Tl +
выступает в роли
электронной ловушки в процессе облучения. При нагревании
Tl 0
рекомбинирует с дырочными центрами и эта рекомбинация пораждает термостимулированную люминесценцию. Спектры термостимулированной люминесценции состоят из таких же полос что и спектр флуорисценции.
Методы синтеза и оптические характеристики кристаллов
Li 2 SO 4
активированных фосфором и редкоземельными элементами (Dy и Eu)
рассмотрены в работе [38]. При исследовании термостимулированной
люминесценции в кристалле
Li 2 SO 4: P, Dy, наиболее заметный пик виден на 416
К с плечами на 388 К и 464 К. Акцент был сделан на увелечении
чувствительности при помощи добавления соактиваторов. Солегирование
Dy 3+
дает добавочный заряд системе, поэтому можно внедрять только ограниченную
концентрацию ионов
Dy 3+, часть внедренных ионов Dy могут присутствовать в
групповой форме. Солигирование ионами
P 5+
в S 6+состоянии приводит к
компенсации заряда и увеличение концентрации ионов
Dy 3+
на местах
Li +.
Luo и соавторы [39] наблюдали увеличение чувствительности в кристалле
MgSO 4: Dy
при солегировании фосфора. Фосфор играл такую же роль как и в
LiF: Mg, CuP
[40, 41, 42], хотя механизм термолюминесценции в этих
кристаллах немного, но отличается. Экспериментальные результаты термостимулированной люминесценции и ЭСР позволяют сделать вывод о том,
что
Mg 2+
вакансия
SO -
комплекс могут принимать участие в процессе
MgSO 4
[43]. С
солегированием фосфора, комплексы дырочных захватов могут содержать
фосфоновые радикалы
PO 3-
и могут быть сформированы вакансии
Mg 2+.
термолюминесценции в кристалле
BaSO 4: Eu
при солегировании фосфора. На
самом деле, было незначительное увеличение концентрации радикалов, но
сигнал ЭСР соответствующий ионам
Eu 2+
показал их трехкратное увеличение
при солегировании фосфора. Увеличение чувствительности
термолюминесценции в кристалле
BaSO 4: Eu
приписываемое распределению
примеси соответственно компенсации заряда становится возможным благодаря присутствию соактиваторного фосфора. Размер увеличения чувствительности наблюдаемое для обоих образцов, становится пропорциональна количеству
солегированного
P 5+. Увеличение выхода термолюминесценции связана с
двумя эффектами. Первое, компенсация заряда приводит к уменьшению вакансии, отвечающих за безизлучательную рекомбинацию, и второе, в кристаллическую решетку внедряются больше ионов активатора.
1.3 Зонная структура сульфатов щелочных металлов.
Люминесцентные свойства сульфатов щелочных и щелочноземельных металлов порождают интерес у исследователей, в связи с тем что они могут быть использованы в качестве активного вещества в твердотельных термолюминесцентных дозиметрах ионизирующего излучения. В спектре
катодолюминесценции облеченного электронным пучком кристалла
CaSO 4
имеется полоса с максимумом в области 3,65 эВ [45]. Можно сделать вывод, что эта полоса излучения связана с собственными дефектами кристаллической
решетки. Рентгенолюминесценция кристалла
K 2 SO 4
при температуре 4,2 К дает
полосу с максимумом на 3,8 эВ, который соответствует излучению
самозахваченного экситона [46]. В кристаллах
K 2 SO 4,
Cs 2 SO 4
и Rb 2 SO 4
была
исследована быстрая люминесценция (t < 2 нc) под воздействием наносекундного импульса пучка электронов, спектры которых состояли из двух полос с максимумами на 3,8 эВ и 5,8 эВ. Авторы работы [47] связали эти термически стабильные полосы быстрого излучения с межзонным электронным переходом между двумя подзонами валентной зоны, которые разделены между собой энергетическим барьером. Межзонный электронный переход является результатом образования дырки в нижней подзоне валентной зоны. Дырки образуются в нижней подзоне валентной зоны в результате перехода электрона из валентной зоны в зону проводимости. Энергия необходимая для такого перехода электрона составляет от 15,5 эВ до 21,5 эВ.
Собственная люминесценция кристаллов сульфатов щелочных и щелочноземельных металлов рассмотрена в работе [48]. Теоретические расчеты
[49] ширины запрещенной зоны для кристалла
K 2 SO 4
и экспериментальные
данные спектров создания пиков термостимулированной люминесценции полученные авторами [50] совпадают и дают значение ширины запрещенной зоны равное 9,1 эВ. Исследование температурной зависимости интенсивности излучения показало, что свечение тушится именно в том температурном
диапазоне, где самозахваченная дырка
SO -
частично делокализуется в момент
K 2 SO 4
190-200 К, и для
кристалла
Na 2 SO 4
120-190 К.
|
В процессе полиморфного перехода переориентация анионного комплекса когда имеет место захват дырочек. Полное соответствие максимумов полос
в спектрах катодо-, фото- и рентгенолюминесценции дает вывод предполагать что упомянутый выше характер рекомбинаций является верным.
В работе [51] исследована быстрое внутреннее излучение с участием оксианионного и катионного возбуждения в сульфатах металлов. Спектр
быстрого свечения для кристаллов
K 2 SO 4,
R b 2 SO 4,
Cs 2 SO 4,
CaSO 4,
SrSO 4
и BaSO 4
облученных одиночным электронным импульсом при температурах 80 К и 300
К (Рис 1.4) могут быть разделены на три типа. Спектр кристалла
CaSO 4
является
примером первого типа, и быстрое свечение кристаллов
Na2 SO 4,
LiKSO 4,
(NH 4)2 SO 4
могут также относиться к этому типу. Только бесструктурная
внутризонная люминесценция наблюдалась во всем спектральном диапазоне в
сульфатах. Похожее явление наблюдалось в работе [52], где внутризонная люминесценция связывалась с переходами горячих дырок между уровнями валентной зоны кристалла. Отсутствие коротковолнового края внутризонной люминесценции демонстрирует, что в вышеупомянутых системах ширина валентной зоны составляет порядка 7 эВ.
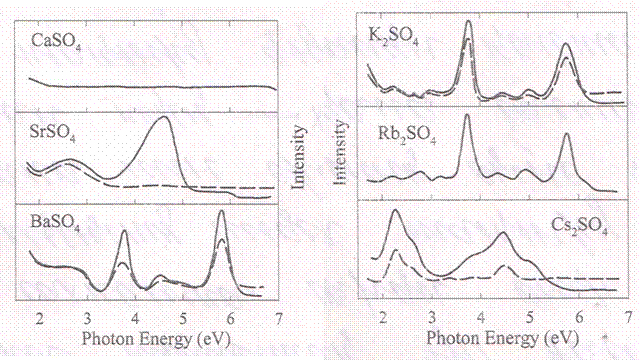
Рисунок 1.4 - Спектр быстрого излучения (τ<2 нс) измеренный для образцов K2SO4 Rb2SO4Cs2SO4CaSO4Sr2SO4и BaSO4облученные импульсом в один электрон при 80 К (сплошна линия) и 300 К (прерывистая линия) [51]
Второй тип спектров быстрого свечения типичен для кристаллов
CaSO 4 и
SrSO 4. При температуре 80 К полосы быстрого излучения скорее всего соответствуют дырочной внутризонной люминесценции. Быстрое свечение второго типа быстро тушиться при нагревании образца до температуры 300 К. Необходимо воздействие для увеличения интенсивности дырочной внутризонной люминесценции, которая протекает параллельно тушению быстрой люминесценции. Третий тип спектров быстрого свечения наблюдается
в кристаллах кристаллов
K 2 SO 4,
R b 2 SO 4, и
BaSO 4. В этих материалах быстрое
свечение может наблюдаться даже при комнатной температуре, спектр которого достаточно широк с ярко выраженными полосами на 3,8 эВ и 5,8 эВ. При увеличении температуры образца интенсивность полос излучения уменьшается, пока дырочная внутризонная люминесценция в спектральной
области
h u > 6 эВ
и выше.
Возбуждение быстрой люминесценции начинается с порогового значения
энергии
Et= 14 -16 эВ. Широкий сигнал при более низких энергиях
возбуждающих фотонов доказывает, что нельзя полностью исключать
инерциальные компоненты внутреннего излучения. В сульфатах, ширина запрещенной зоны составляет порядка 9 эВ [53], а ширина валентной зоны составляет порядка 7 эВ. Валентная зона разделена энергетической зоной с энергией 14-15 эВ. Сильная температурная зависимость интенсивности полос быстрого свечения свидетельствует о том, что эта зона достаточно узкая. Отличие в спектральной структуре кристаллов возможно связано с разными значениями ширины этой энергетической зоны, находящейся внутри валентной зоны.
Расчеты структур полос для кристаллов
K 2 SO 4 и
LiKSO 4
представлены в
работах [54, 55] и [56] соответственно. По этим расчетам валентная зона
кристалла
K 2 SO 4
разделена на три подзоны и средняя и нижняя из них
расположена в 15-16 эВ и 20-21 эВ соответственно от нижней части зоны
проводимости. В кристалле
LiKSO 4
верхняя и средняя подзоны не разделены
между собой. Теоретические расчеты согласуются с экспериментальными данными и подразумевает, что энергия 14-15 эВ соответствует энергии для перехода электрона из средней подзоны валентной зоны в зону проводимости.
Диаграмма энергетических зон кристалла
K 2 SO 4
представлена на рисунке
1.5 Полосы быстрого излучения не зависят от энергии возбуждающих фотонов в спектральной области 15-21 эВ, и поэтому перед излучательной рекомбинацией дырке необходимо всплыть на верхний уровень средней подзоны валентной зоны. Положение максимума ширина полос быстрого излучения определяется распределением плотности состояний в верхней подзоне валентной зоны серы и шириной этой подзоны. Структура спектров возбуждения быстрого излучения определялся параметрами средней подзоны валентной зоны. Минимум энергии ионизации для самого отдаленной
электронной оболочки равна 20,5 эВ для 3p
K + [57], 14 эВ для 5p
С s+
[58] и 18
эВ для 5p
Ba 2+
[59].
Представлены полосы возбуждения в соответствующей спектральной области спектра возбуждения быстрого излучения. Состояния бария и калия не вносят прямой вклад в излучательную рекомбинацию, которое дает быстрое излучение, потому что дырка термализуется еще до рекомбинации. С другой
стороны, 5p
состояние
С s+
на поверхности средней валентной подзоны и
быстрое излучение возбужденное энергией 14-15 эВ в кристалле
Cs 2 SO 4
может
соответствовать типичной кросслюминесценций. Энергетическая зона между верхней и средней валентными подзонами становиться уже при повышении температуры, и следовательно интенсивность быстрой люминесценции уменьшится и параллельно увеличивается вероятность излучательной рекомбинации частиц с верхней в среднюю валентную подзону.
В работе [61] рассмотрено процессы электронно-дырочных пар и молекулярных экситонов. Было проведено исследование спектров возбуждения
свечения ионов
Dy3+
при энергии 2,58 эВ, используя синхротронное излучение с
энергиями 6-30 эВ для кристалла
CaSO 4: Dy
при температуре 8 К.
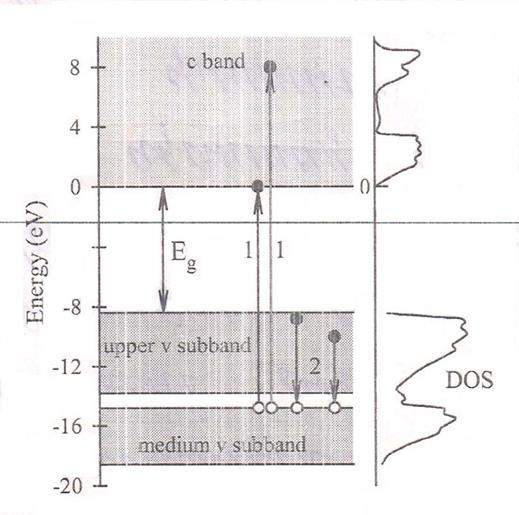
Рисунок 1.5 - Схематическая диаграмма энергетической зоны для K2SO4.
Правая сторона показывает распределение общую плотность состоянии [6].
Электрон переходит с средние под-полосы валентной полосы в зону проводимости (стрелки 1) и излучательная рекомбинация электрона с верха под-зоны с дыркой в середине под-зоны (стрелка 2) [60]
Излучение ионов
Dy3+
эффективно возбуждается при энергиях больше 10,8
эВ в области ионизации
SO2-. для центров свечения
Dy3+. Эффективность
- дырочных пар. Различные виды собственной люминесценций наблюдались в сульфатах металлов при люминесценции самозахваченного экситона, при термически стабильной и быстрой внутризонной люминесценции с продолжительным спектром от 1,6 эВ до 7,3 эВ, при быстрой люминесценции соттветствующей излучательному переходу между валентными подзонами.
В работе [62] рассмотрены электронные спектры в области вакуумного ультрафиолета некоторых сульфатных солей. Экспериментальные исследования в данной области представлены работами по измерению спектров люминесценции возбужденных фотонами и рентгеном [62, 63, 64]. Исследованные спектры поглощения сульфатных солей позволяют сделать вывод о том, что присутствует слабое поглощение в области 2-5 эВ. И так же
определено, что начиная с области 4-6 эВ и дальше в сторону больших энергии имеет место сильное поглощение.
Моделирование эластооптических свойств кристалла
K 2 SO 4
приведено в
работе [65]. Для расчета электронно - оптического спектра кристалла сульфата калия в орторомбической фазе был применен метод функционала плотности. В основе этих расчетов лежали компоненты эластооптического тензора
p im (i, m = 1,2,...,6), полученные для индексов
i, m = 1,2,3. Рассчитанные, основные
индексы отражения для кристалла
K 2 SO 4
в области пропускания 0,4-7,3 эВ в
удовлетворительной форме согласовывается с экспериментальными данными, принятыми в расчет, при вводе с атомных осцилляторов в области энергии 0-0,4 эВ.
При увеличении индексов отражения кристалла
K 2 SO 4
под давлением в 1
ГПа, наблюдалось согласование с увеличением плотности кристалла индуцированного давлением, была предсказано, что отражение кристалла относительно стабилизируется. Это заключение полностью согласуется с известным соотношением Лоренца-Лоренца.
В основе исследования можно предполагать, что данные были получены в
виде изотропных точек в области прозрачности кристалла
K 2 SO 4. Предельная
величина оказываемого давления, при котором не будет сжатия материала равна 2 ГПа. Рассчитанные компоненты эластооптического тензора кристалла
K 2 SO 4
оказались заниженными приблизительно в два раза. Это, видимо явилось
причиной преувеличения компонентов тензора пластической жесткости.
Структура энергетических зон монокристалла
LiKSO 4
рассмотрена в работе
[66]. Для монокристалла
LiKSO 4
была рассчитаны энергические уровни и спектр
отражения, при помощи метода первопринципов LCAO. Были определены, по крайней мере три подзоны в валентной зоне и зоне проводимости. Экспериментальное исследование спектров отражения в системе кристалла
LiKSO 4
хорошо согласуются с теоретическими расчетами для нижнего значения
энергии зоны. Возникновение анизотропии эффективной массы необходимо объяснить возможной несоизмеримостью фазовых переходов. Монокристалл сульфата лития калия кажется многообещающим материалом для изучения несоизмеримости фазовых переходов.
В работе [67] электронная структура собственных и приместных Mn
центров в кристаллах
A 2 BX 4
со структурой
b - K 2 SO 4. На рисунке 1.6
представлена структура энергетических уровней монокристаллов
Cs 2 CdI 4
для
кристаллического вида
b - K 2 SO 4,
Sr 2 GeS 4. Валентная зона в этих кристаллах
сформирована
s -и
p -орбиталями йода. А зона проводимости состоит из s -
орбитали цезия и
p -орбитали кадмия.
Результаты расчетов наглядно демонстрируют, что в монокристаллах
Cs 2 CdI 4
присутствуют непрямые внутризонные переходы. Максимумы
валентной зоны расположены на позиции Г в зоне Брюллена, минимум зоны
проводимости расположен ближе к позиции T для структуры типа
b - K 2 SO 4 и
для структуры типа
Sr 2 GeS 4
расположены ближе к позиции Z.
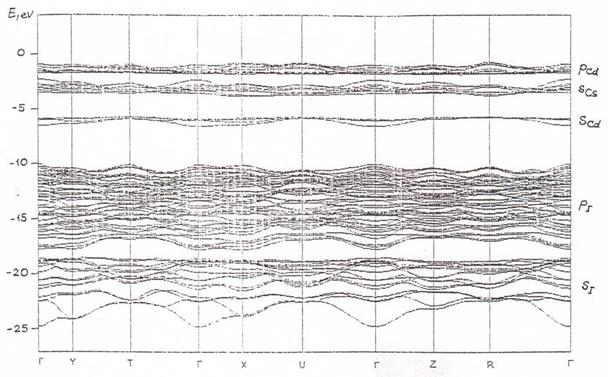
Электронная зонная структура Cs2CdI4одиночных кристаллов с типам кристаллической решетки β-K2SO4
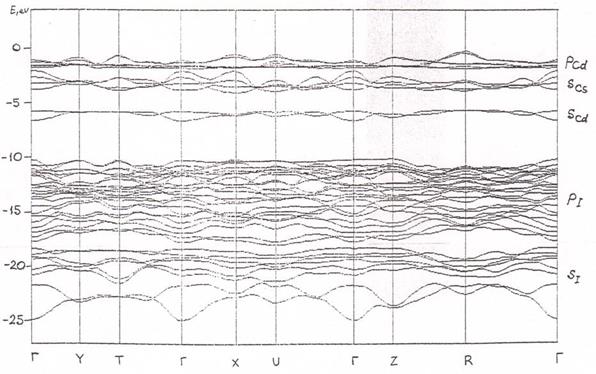
Рисунок 1.6 –Электронная зонная структура Cs2CdI4 одиночных кристаллов с типам кристаллической решетки Sr2GeS4[67]
Расчетное значение энергии запрещеной зоны равна 3,53 эВ и 3,59 эВ в
точке Г, для кристаллических типов
b - K 2 SO 4
и Sr 2 GeS 4
соответственно, а так же
3,51 эВ для самого короткого внутризонного перехода в обоих типов. Фазовые
переходы в
Cs 2 CdI 4
из b - K 2 SO 4
в Sr 2 GeS 4
вызывает сдвиг максимума валентной
зоны с позиции Z к Т.
Кластеры
(Mn 2+ Cl)2-
являются структурными элементами
[ N (CH 3)4
]2 MnCl 4.
Оптические переходы происходят с основного состояния
A 1. Фазовые
переходы оказывают сильное влияние на позиции основных термов энергии.
В работе [21] рассмотрен ротор фаз ионной проводимости в качестве новой идеи для квазиупругого нейтронного рассеяния. Для проверки ротора фаз
кубической катионной проводимости кристаллов
Na 3 PO 4,
Li 2 SO 4 и
LiNaSO 4
было
использовано квазиупругое нейтронное рассеяние. При помощи высокого разрешения обратного рассеяния, для описания переноса натрия
экспериментально доказано, что в кристалле
Na 3 PO 4
в основном перенос натрия
происходит через тетраэдральные позиции. Временные масштабы катионных перемещений и анионных реориентаций хорошо выделяются в кристаллах Na 3 PO 4. А в разных сульфатах ситуация полностью другая, здесь оба типа движения является причиной квазиупругих распространении время пролетных исследований.
Для кристаллов
Li 2 SO 4
квазиупругое рассеяние преобладает диффузией
лития, но отделить друг от друга вклады в реориентационное и поступательное движение при высоких волновых векторах очень трудно.
Исследование в таком же ключе кристаллов
LiNaSO 4
кажется
многообешающим. Мы можем подобрать данные с помощью двух лоренцевых линии, меньшее из которых может легко быть интерпретирована методом Чадли-Эллиота. Широкий компонент показывает все характерные черты локализованных реориентированных движений.
1.4 Дефектообразование в сульфатах щелочных металлов
В последние годы большое количество соединений семейства
A ' A '' BX 4
(где
A ',
A '= Li, Na, K, Rb, Cs, NH 4, N (CH 3)4
и др. и
BX 4 = SO 4, SeO 4, ZnCl 4, ZnBr 4, BeF 4,
MoO 4, WO 4
и др.) являются очень интересными объектами из за разнообразия
физических свойств последовательности фазового перехода, включающего в себя несоизмеримые суперионные, ферроэлектрические, сегнетоэлектрические
фазы. Исключительно с суперионными проводниками (Li 2 SO 4,
LiNaSO 4
и др.)
соединения
A ' A '' BX 4
демонстрируют высокотемпературную неупорядоченную
|
|
Kurzynski [68] квалисифицировал эти соединения на четыре отдельные
группы согласно последовательности структурных фаз. Кристалл
LiKSO 4
был
выделен в отдельную группу, в виду его необычной последовательности фазовых переходов (Рис 1.7).
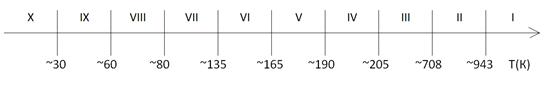
Рисунок 1.7 – Последовательность фазовых переходов кристалла
LiKSO 4
[69]
Температуры в этой схеме, в основном, соответствуют литературным данным, посвященным процессам нагревания [70, 71, 72, 73, 74, 75, 76].
Несмотря на большое количество экспериментальных и теоретических
работ посвященных исследованиям кристаллов
LiKSO 4
в температурном
диапазоне 200-1000 К, существуют еще не мало спорных точек зрения относительно последовательности фазовых переходов. Эти спорные моменты связанные в основном с существованием, или ее отсутствием, некоторых фазовых переходов и симметрий этих структурных фаз.
На самом деле, установлены только структуры соответствующие фазам I и
|
принадлежащей пространственной группе
4 (P 6
/ mmc) [77].
|
LiKSO 4
находится в фазе (III),
которая обладает гексогональной симметрией принадлежащей
|
(P 63
) с двумя формульными единицами в
элементарной ячейке[78, 68]. Между этими гексагональными фазами существует структурная фаза (II) которая симметрией конечно ниже, чем гексагональная. В этой фазе присутствуют и орторомбическая и модулированная структуры. Модулированная структура несоизмерима между 743 К и 940 К, и соизмерим в температурном диапазоне 711-743 К [77]. Pimenta с соавторами [79] представил модель, которая согласовывает эти два объяснения: двойное-К орторомбическая модуляция расстройства вероятности.
На рисунке 1.8 представлена проекция структуры при комнатной температуре в плоскости, перпендикулярной к гексагональной оси с [78, 68]. Ион калия локализуется вдоль гексагональной оси. Ионы сульфата ориентируются таким образом, чтобы три иона кислорода располагались перпендикулярно гексагональной оси, а четвертый вдоль тройной оси этой структуры. Инны лития и серы также локализуются вдоль тройной оси этой структуры. Два иона сульфата этой же элементарной ячейки направлены по винтовой к плоскости шестигранника, вдоль оси с. Принимая во внимание полярность данной группы симметрии, можно сделать вывод о приоэлектричности этого кристалла при комнатной температуре [80]. Также в этой фазе вдоль гексагональной оси присутствует оптическая активность [76,
80]. Еще один немаловажный аспект в структуре кристалла
LiKSO 4
при
комнатной температуре, который связан с динамичным ориентационным
разупорядочением ионов сульфата. Шультц, Цукер и Фрэч [68] наблюдали как ион кислорода занимает три разные позиции вокруг тройных осей. Средняя позиция по тройным осям, и это сохраняет структуру симметрии. При понижении температуры в кристалле происходит фазовое превращение при 205 К. Bansal и соавторы [70] при исследовании рамановской спектроскопии, для фазы IV предложили треугольную структуру вдоль пространственной
|
|
(P 31 c). А Tomaszewski и Lukaszewicz [71] предложили
|
|
(P 63m c). При
исследовании нейтронной дифракции Zhang, Yan и Boucherle [81] предположили что имеет место предложенная в работе [70] треугольная симметрия и определили атомные положения в этой симметрии. Bhakay- Tamhane и Sequiera [74] предложили что присутствие двух видов малых размеров побудило авторов [71] отдать предпочтение к структуре с более высокой симметрией.
Проекция треугольной структуры на базисную плоскость представлено также на рисунке 1.8. Отличием в данной структуре от структуры при комнатной температуре является то что сульфат поворачивается в своей элементарной ячейке. В работе [81] показано, что в этой фазе ориентация ионов сульфатов сохраняется неизменной.
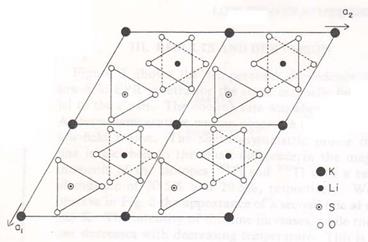
Рисунок 1.8 - Проекция четырех элементарных ячеек кристалла LiKSO4 в базисной плоскости для III и IV фазы. Затушеванные треугольники
представляют ориентацию сульфата тетраэдров в фазе III. Один сульфат в каждой элементарной ячейки является переориентация в фазе IV (пунктирные треугольники). Два тетраэдра через элементарные ячейки смещаются на с / 2 вдоль оси c [69]
Если продолжать процесс охлаждения кристалл подвергается следующему фазовому переходу при температуре около 190 К. Моноклинная структура с
пространственной группой
C4(Cc)
представлена в работах [74, 76],
|
2v (
 2015-09-06
2015-09-06 1396
1396








