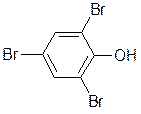 Реакции электрофильного замещения водорода в бензольном ядре для фенолов протекают значительно легче и в более мягких условиях, чем для бензола, т.к. «ОН» группа является заместителем - электронодонором, ОН – группа направляет следующий заместитель в орто-пара положения. Например, реакция галогенирования:
Реакции электрофильного замещения водорода в бензольном ядре для фенолов протекают значительно легче и в более мягких условиях, чем для бензола, т.к. «ОН» группа является заместителем - электронодонором, ОН – группа направляет следующий заместитель в орто-пара положения. Например, реакция галогенирования:
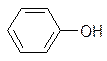 |
+Br2
®
-HBr
Аналогично протекают реакции нитрования и сульфирования.
Фенолы хорошо восстанавливаются в присутствии никелевого катализатора:
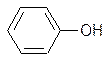 | 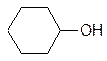 |
H2/Ni 250°C

циклогексанол
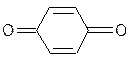
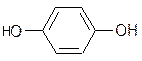
Фенолы легко окисляются. Особый интерес вызывают хиноны. Они широко распространены в природе и играют роль структурных компонентов стимуляторов роста, антибиотиков, а также участвуют в окислительно-восстановительных процессах, сопровождающих дыхание:
 | |||
 | |||
-2еˉ,-2Н+
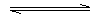
+2еˉ,+2Н+
гидрохинон хинон
Фенолы играют важную роль в химической промышленности, поскольку они наряду с другими веществами применяются в качестве основных исходных веществ для получения пластических масс.
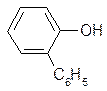
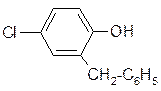 Дезинфицирующая жидкость “лизол” содержит о-фенилфенол и 2-бензил – 4-хлорфенол, которые обладают бактерицидным действием. Даже простейший раствор фенола является сильным дезинфицирующим средством. Под названием карболовой кислоты его используют в медицинских учреждениях. Антимикробную активность различных соединений сравнивают с активностью фенола при помощи так называемого “фенольного коэффициента”.
Дезинфицирующая жидкость “лизол” содержит о-фенилфенол и 2-бензил – 4-хлорфенол, которые обладают бактерицидным действием. Даже простейший раствор фенола является сильным дезинфицирующим средством. Под названием карболовой кислоты его используют в медицинских учреждениях. Антимикробную активность различных соединений сравнивают с активностью фенола при помощи так называемого “фенольного коэффициента”.
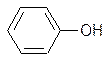
фенол о-фенилфенол 2-бензил-4-хлорфенол
Для того чтобы предохранить древесину от гниения, ее пропитывают креозотом – фракцией каменноугольной смолы, богатой фенолом, а также о-, м- и п-крезолами:
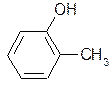 | 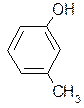 | ||
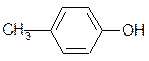
о-крезол м-крезол п-крезол
Фенольные соединения встречаются в различных растениях, например в Larrea mexicana – вечнозеленом кустарнике с резким запахом, произрастающим на севере Мексики и в юго-западных районах США. Токсичные начала сумаха и дуба также имеют фенольную природу. Фенолы обладают прижигающим действием и способны вызывать серьезные повреждения кожи, слизистой оболочки и мембран. Одним из наиболее интересных природных производных фенола является мессалин, способный вызывать галлюцинации.
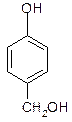
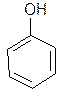
Активность фенолов в реакциях электрофильного замещения настолько велика, что даже формальдегид в кислых растворах реагирует с фенолом. На этой реакции основано получение бакелитовых смол – дешевого и широко применяющегося полимера:
 | |||||
 | |||||
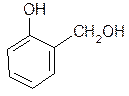 | |||||
+ nСН2О

 +
+
n -Н2О
 |  | ||||
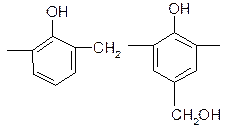 | |||||

n
Нафтолы
Наибольший интерес представляют гидроксипроизводные нафталина –
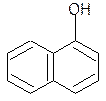 a- и b-нафтолы:
a- и b-нафтолы:
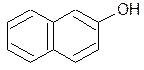 |
a - нафтол b - нафтол
 Они обладают свойствами фенолов, растворяются в едких щелочах. Оба вещества трудно растворяются в воде, дают окрашенные cоединения с хлорным железом. Реакции замещения нафтолов идут сначала в том же ядре, где находится оксигруппа:
Они обладают свойствами фенолов, растворяются в едких щелочах. Оба вещества трудно растворяются в воде, дают окрашенные cоединения с хлорным железом. Реакции замещения нафтолов идут сначала в том же ядре, где находится оксигруппа:
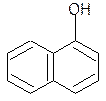 |
 + HNO3 + H2O
+ HNO3 + H2O
4-нитро-a-нафтол
 | |||
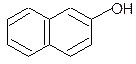 |
 + Br2 + HBr
+ Br2 + HBr
a-бром-b-нафтол
Нафтолы и их производные, особенно сульфопроизводные, широко используются в производстве азокрасителей.
Если гидроксильная группа удалена от ароматического ядра, то соединение относят к ароматическим спиртам. Гидролизом хлористого бензила может быть получен бензиловый спирт:
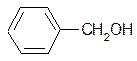
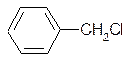
 +НОН
+НОН
+ HСl
ОНˉ
бензиловый спирт
Для них характерны как обычные реакции спиртового (но не фенольного гидроксила), так и реакции ароматического ядра (группа СН2ОН является заместителем первого рода, т.е. электронодонором). b-Фенилэтиловый спирт Н5С6-СН2-СН2-ОН является основным компонентом природного розового масла и широко используется в парфюмерии.
Тиолы
Подобно тому, как спирты и простые эфиры являются органическими аналогами воды, тиолы (тиоспирты, меркаптаны) (R-SH) и сульфиды (R-S-R) представляют собой органические аналоги сероводорода.
| Н-О-Н вода | Н-S-H сероводород |
| R – O-H спирт R-O-R простой эфир H-O-O-H пероксид водорода | R-S-H тиол R-S-R сульфид R-S-S-R -дисульфид |
Несколько типичных представителей подобных соединений:
СН3-SH метантиол (метил меркаптан)
C6H5-SH тиофенол
CH3-S-CH3 диметилсульфид
CH3-S-С6Н5 метилфенилсульфид
CH3-S-S-CH3 диметилдисульфид
Тиолы обладают характерным, очень неприятным запахом, более сильным, чем запах сероводорода. Для низших тиолов запах ощущается при концентрации 1 часть на 400 млн. частей воздуха. Добавкой к природному газу ничтожных количеств изопентантиола пользуются для лучшего обнаружения по запаху утечки газа в жилых помещениях. Тиолы и их производные встречаются в растительном и животном мире, например пропантиол С3Н7SH – в свеженарезанном луке, бутантиол C4H9SH – в выделениях скунса. Сера входит в состав некоторых белковых аминокислот (цистеин, цистин, метионин). Тиоспирты – жидкости с температурой кипения более низкой, чем у соответствующих спиртов. Это объясняется меньшей склонностью тиолов к образованию межмолекулярной водородной связи.
Меркаптаны плохо растворимы в воде.
Кислотность тиоспиртов выше, чем у спиртов, поэтому они в отличие от последних образуют соли не только со свободными металлами, но и со щелочами; соли их гидролизуются водой.
СH3-CH2-SH + KOH 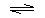 CH3-CH2-SK + H2O
CH3-CH2-SK + H2O
этилмеркаптан этилмеркаптид
калия
С тяжелыми металлами (ртуть, мышьяк, свинец, кадмий, цинк) и их окислами тиолы образуют нерастворимые соли – меркаптиды
 2 СН3-СН2-SH + HgO (CH3-CH2-S)2Hg
2 СН3-СН2-SH + HgO (CH3-CH2-S)2Hg
-H2O этилмеркаптид ртути
Способность тиолов связывать ионы тяжелых металлов позволяет использовать их как противоядия (антидоты) при отравлениях соединениями этих металлов. Одним из таких препаратов является отечественный препарат унитиол (димеркаптопропансульфонат натрия):
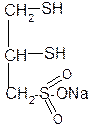
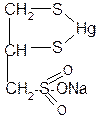
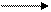 + HgCl2 + 2HCl
+ HgCl2 + 2HCl
Меркаптаны в отличие от спиртов окисляются даже на воздухе с образованием диалкилдисульфида:
[O]
 H3C-CH2-SH + CH3-CH2-SH CH3-CH2-S-S-CH2-CH3 + H2O
H3C-CH2-SH + CH3-CH2-SH CH3-CH2-S-S-CH2-CH3 + H2O
диэтилдисульфид
Дисульфиды легко восстанавливаются в тиолы. Процесс окисления тиолов и восстановления дисульфидов играет важную роль в химии белков и пептидов. При жестком окислении тиолов (азотной кислотой) образуются сульфокислоты:
[O]
 СH3SH CH3-SO3H
СH3SH CH3-SO3H
метантиол метансульфокислота
Аналогично спиртам тиолы реагируют с хлористыми ацилами, образуя тиоаналоги сложных эфиров:
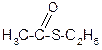
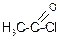
 + C2H5SH + HCl
+ C2H5SH + HCl
этилтиоацетат
К классу сульфидов относится боевое отравляющее вещество кожно-нарывного действия иприт (b, b1-дихлордиэтилсульфид). Это бесцветная жидкость с чесночным запахом. Для дегазации иприта используется хлорная известь или хлорамин. Дегазаторы превращают иприт в сульфоксид и другие вещества. Получают иприт при действии хлористой серы на этилен:
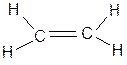
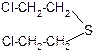 |
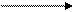 2 + S2Cl2 S +
2 + S2Cl2 S +
Глоссарий
Гидролиз - процесс расщепления молекулы с участием воды.
Кислоты Бренстеда – это нейтральные молекулы или йоны, способные отдавать протон (доноры протонов).
Основания Бренстеда - это нейтральные молекулы или йоны, способные присоединять протон (акцепторы протонов).
Кислоты Льюиса – это акцепторы электронной пары.
Основание Льюиса – это доноры электронной пары.
Реакции этерификации – образование сложного эфира при взаимодействии кислоты и спирта.
Комплексные соединения – это соединения, в которых есть хотя бы одна химическая связь, образованная по донорно-акцепторному механизму.
Лиганд – молекула - донор неподеленной электронной пары.
«Хелаты» - это комплексные соединения, в которых одна молекула лиганда образует с центральным атомом две химические связи, одна из которых донорно-акцепторная.
Электрофильные реагенты (электрофилы) – частицы с недостатком электронной плотности (нейтральные молекулы или катионы).
Нуклеофильные реагенты (нуклеофилы) – частицы с избытком электронной плотности (нейтральные молекулы или анионы).
Радикалы – это свободные атомы или частицы с неспаренным электроном (Cl·,
HO·, HOO·, R·,).
Тема 3. Альдегиды и кетоны
Цель занятия: рассмотреть закономерности химического поведения оксосоединений и особенности реакционной способности альдегидов и кетонов.
Конкретные задачи
1. Студент должен знать классификацию и номенклатуру оксосоединений, формулы и тривиальные названия важнейших представителей альдегидов и кетонов, электронное строение карбонильной группы и химические свойства альдегидов и кетонов, особенности поведения альдегидов в отличие от кетонов.
2. Студент должен уметь: обосновать направление химических реакций по карбонильной группе, писать уравнения реакций нуклеофильного присоединения по карбонильной группе, реакций альдольной конденсации и дисмутации альдегидов; проводить реакции по идентификации альдегидов и кетонов: серебряного зеркала, с нитропруссидом натрия, йодоформную пробу, специфическую реакцию дисмутации формальдегида.
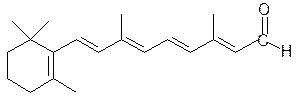
Мотивация. Альдегиды и кетоны широко используются в клинической медицине и санитарии, в фармацевтической и пищевой промышленности, в органическом синтезе. Карбонильную группу содержат многие природные соединения: углеводы, гормоны, витамины, оксокислоты. Все они играют исключительную роль в биохимических превращениях. Например, ретиналь относится к витаминам группы А, получается в организме окислением ретинола, участвует в процессе зрительного восприятия.
 |
Пиридоксаль (витамин В6) в виде пиридоксальфосфата участвует в обмене a-аминокислот:
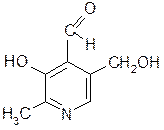
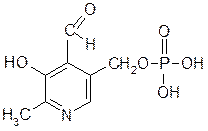
 2015-10-22
2015-10-22 2465
2465
