Одним из наиболее перспективных и широко используемых методов разделения РЗЭ является экстракция. Экстракция это процесс селективного извлечения целевого компонента из водной фазы в органическую, за счет образования либо комплексного соединения, либо сольвата с органическим реагентом (экстрагентом). По сравнению с традиционными методами экстракция имеет ряд преимуществ:
- простота аппаратурного оформления и возможность реализации непрерывного процесса;
- возможность создания замкнутого цикла за счет оборота экстрагента, что сокращает объем стоков;
- малая энергоемкость процесса.
Основной количественной характеристикой процесса экстракции является коэффициент распределения (D), который равен соотношению равновесных аналитических концентрация ценного компонента в органической и водной фазах:
 (ХХ)
(ХХ)
В том случае,если необходимо разделить два и более ценных компонента, для характеризации процесса используют коэффициент разделения (b):
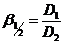 (ХХ)
(ХХ)
Величина коэффициента разделения определяет технологическую возможность разделения компонентов, для эффективного разделения b1/2 должна быть больше 3,5 - 4.
В технологии РЗЭ применяют различные экстракционные системы и используют экстрагенты практически всех основных классов – нейтральные экстрагенты, катионообменные (органические кислоты) и анионообменные экстрагенты (органические основания) [1–3].
Среди нейтральных экстрагентов наиболее широко применяют нейтральные фосфорорганические соединения (НФОС). Для решения некоторых специфических задач, например, глубокой очистки иттрия, используют НСО (нефтяные сульфоксиды). Из большой группы органических кислот наибольшее применение нашли моноосновные фосфорорганические кислоты. В более ограниченных масштабах применяют монокарбоновые кислоты как с радикалами нормального строения, так и с разветвленными радикалами преимущественно в α-положении. Среди органических оснований наилучшие результаты достигнуты для солей четвертичных аммониевых оснований. В последнее время много внимания уделяют смесям экстрагентов.
Нейтральные фосфорорганические соединения (НФОС). К ним относятся фосфаты (средние эфиры ортофосфорной кислоты) (RO)3РО; фосфонаты (RO)2(R)РО; фосфинаты (RO)(R)2РО; фосфиноксиды R3РО и бифункциональные экстрагенты типа (RO)2P(О)(CH2)nP(O)(OR)2; или R2Р(O)(СН2)nР(O)(ОR)2, где n ≥ 1 (табл. 7). Практически важные результаты получены для фосфатов, фосфонатов и фосфиноксидов.
Таблица 7. – Нейтральные фосфороорганические соединения
| Нейтральные фосфороорганические соединения | Структурная формула | Общая формула |
| Фосфаты (средние эфиры ортофосфорной кислоты) | 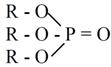 | (RO)3РО |
| Фосфонаты | 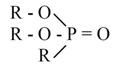 | (RO)2(R)РО |
| Фосфинаты | 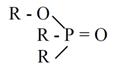 | (RO)(R)2РО |
| Фосфиноксиды |  | R3РО |
| Бифункциональные экстрагенты | 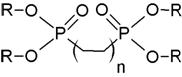 | (RO)2P(О)(CH2)nP(O)(OR)2 |
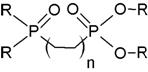 | R2Р(O)(СН2)nР(O)(ОR)2 |
Наибольшее применение в технологии разделения РЗЭ получил ТБФ (трибутилфосфат – (C4H9O)3PO4), который используют как в чистом виде, так и в смеси с инертными разбавителями (керосином и др.), ТБФ в достаточной степени извлекает РЗЭ из нитратных растворов как нейтральных, так и кислых, вплоть до сильно концентрированных по азотной кислоте растворов.
Экстракция РЗЭ из нейтральных и слабокислых нитратных растворов как ТБФ, так и другими нейтральными фосфорорганическими соединениями осуществляется в виде трисольватов согласно реакции
Ln3+вод + 3NO 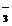 вод +3Sорг
вод +3Sорг 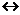 Ln(NO3)3S3 орг (20)
Ln(NO3)3S3 орг (20)
Константа данной реакции будет равна:
K= 
 (21)
(21)
А соответственно коэффициент распределения:
D=  (22)
(22)
Анализ уравнения (22) показывает, что извлечение на стадии экстракции будет зависеть от концентрации нитрат иона в водном растворе и от концентрации экстрагента. Концентрацию нитрат-иона в растворе складывается из концентрации нитрата металла, азотной кислоты и высаливателя. Рассмотрим действие каждого их них.
Для нейтральных и слабокислых растворов (0,001–0,5 моль/л HNO3) в процессе экстракции ТБФ концентрация нитрата металла в органической фазе возрастает по мере роста ее в водной фазе и достигает 150–180 г/л при содержании в водной фазе 300–400 г/л [5, 6]. Изотерма экстракции нитратов РЗЭ описывается характерной кривой с горизонтальным участком в области высоких концентраций (области насыщения органической фазы металлом) (рис. 17). Таким образом, высокие коэффициенты распределения РЗЭ при экстракции будут получены в области высоких концентраций нитратов РЗЭ.
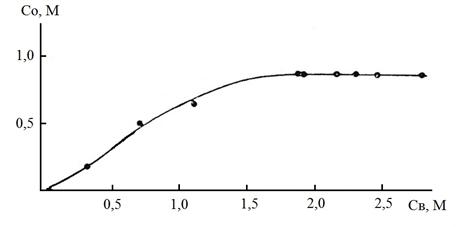
Рисунок 17. – Изотерма экстракции неодима ТБФ

Рисунок 18. – Зависимость коэффициента распределения РЗЭ от порядкового номера элемента при экстракции ТБФ
На рис. 18 приведены типичные кривые распределения РЗЭ при экстракции ТБФ, полученные для различных концентраций азотной кислоты. Кривая распределения металлов от порядкового номера элемента (lgD – ZLn) имеет излом в области Eu–Tb. С ростом концентрации нитратов РЗЭ в фазе экстрагента, при концентрации азотной кислоты 0,266М, крутизна кривой в области легких лантаноидов увеличивается, а в области тяжелых уменьшается, т.е. коэффициенты разделения легких лантаноидов увеличиваются, а тяжелых уменьшаются. Это процесс называется инверсия (обращение) закономерности распределения и представляет собой изменение коэффициентов распределения для ряда европий–лютеций, наблюдается в растворах с концентрацией HNO3 ниже 5 м/л. Это связано с увеличением энергии гидратацией[4], вклад которой особенно значителен при низких концентрациях азотной кислоты. У тяжелых РЗЭ из-за меньшего ионного радиуса гидратация проявляется значительно сильнее - затрудняет вытеснение молекул воды из гидратной оболочки иона молекулами ТБФ. В результате их коэффициенты распределения значительно меньше, чем у представителей легкой подгруппы. Поэтому отделение легких лантаноидов от средних и тяжелых, а также разделение смеси легких лантаноидов на индивидуальные элементы целесообразно проводить в экстракционной системе ТБФ – концентрированный раствор нитратов РЗЭ.
При введении в водную фазу высаливателей[5] коэффициенты распределения (уравнение 22) и факторы разделения РЗЭ существенно возрастают. По эффективности своего действия высаливающие соединения составляют следующую последовательность: LiNO3 (6 моль/л)≈ HNO3 (15,6 моль/л) > Al(NO3)3 (2,5 моль/л) > Ca(NO3)2 (2,5моль/л) > NH4NO3 (9 моль/л). В таблице 8 на примере разделения пары Pr–Nd показано закономерное изменение коэффициентов разделения для указанного ряда высаливателей. Введение высаливателей приводит к увеличению коэффициента разделения, однако при этом уменьшается концентрация металла в водной фазе. Кроме того, при осуществлении процесса в каскаде необходимо вводить операцию регенерации высаливателя с целью многократного использования его в разделительном цикле.
Таблица 8. – Факторы разделения при экстракции бинарной смеси Nd–Pr 100% ТБФ с использованием различных высаливателей
| Высаливатель | Концентрация высаливателя, моль/л | Концентрация РЗЭ в органической фазе, г/л | Концентрация РЗЭ в водной фазе, г/л | β Nd-Pr |
| LiNO3 | 6,5 | 182,7 | 141,1 | 1,95 |
| Al(NO3)3 | 2,5 | 177,4 | 132,4 | 1,68 |
| Ca(NO3)2 | 2,5 | 176,2 | 120,4 | 1,62 |
| NH4NO3 | 170,0 | 167,4 | 1,57 |
Концентрация ТБФ, как было отмечено ранее при анализе уравнения 22, оказывает влияние на коэффициенты распределения РЗЭ. В некоторых случаях ТБФ можно разбавлять инертными разбавителями (керосином и др.).
Введение разбавителя приводит к снижению содержания металла в органической фазе и вязкости экстрактов, а также увеличению скорости расслаивания фаз, однако коэффициенты разделения смежных лантаноидов при этом изменяются незначительно. Коэффициенты разделения смежных лантаноидов при экстракции нитратов РЗМ 50%-ным раствором ТБФ в углеводородном разбавителе приведены в таблице 8.
Таблица 8. – Коэффициенты разделения смежных лантаноидов при экстракции нитратов РЗМ 50 %-ным раствором ТБФ в углеводородном разбавителе
| Концентрация РЗМ, г/л | ||||||
| Пара | Коэффициент разделения (β) | |||||
| Sm–Nd | 2,26 | – | 2,04 | 1,55 | 1,58 | 1,40 |
| Gd–Sm | 1,01 | – | 1,07 | 0,99 | 0,82 | 0,78 |
| Dy–Gd | 1,45 | 1,20 | 1,17 | 1,08 | 0,92 | 0,82 |
| Ho–Dy | 0,92 | 0,96 | 0,94 | 0,89 | 0,83 | 0,77 |
| Er–Ho | 0,96 | 0,65 | 0,82 | 0,78 | 0,72 | 0,70 |
| Yb–Er | 0,81 | – | – | – | – | 0,63 |
Примечание: коэффициенты разделения смежных лантаноидов Ce–La, Pr–Ce и Nd–Pr при концентрации РЗМ в водной фазе 460 г/л соответственно равны 1,70; 1,75; и 1,50.
Приведенные данные иллюстрируют типичную картину изменения β (коэффициент разделения) в системе ТБФ – концентрированный раствор нитратов РЗЭ.
Экстракционное поведение РЗЭ при экстракции нейтральными экстрагентами, такими как ТБФ, отличается и зависит от исходной концентрации азотной кислоты (рис. 18). При концентрации азотной кислоты больше 7М она сама экстрагируется и конкурирует с РЗЭ за экстрагент:
H+вод + NO 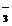 вод +Sорг
вод +Sорг 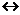 [HNO3·S]орг (23)
[HNO3·S]орг (23)
В условиях больших концентраций HNO3 (11–15 моль/л) ее конкурентная экстракция значительно ослабевает, поскольку образующиеся, в этих условиях, комплексные кислоты экстрагируются лучше, чем HNO3:
Hn[Ln(NO3)3+n]вод +qSорг 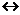 Hn[Ln(NO3)3+n]Sq орг, (24)
Hn[Ln(NO3)3+n]Sq орг, (24)
где n=1–3, q=2–3.
Значения коэффициентов распределения в системе ТБФ – HNO3 при высоких концентрациях HNO3 (11–15 моль/л) непрерывно возрастают с увеличением атомного номера лантаноида, поскольку представители тяжелой группы РЗЭ более склонны к образованию комплексных кислот (рис. 18).
При высокой кислотности (более 12 м/л) средняя величина коэффициента разделения для соседних элементов от лантана до тербия β = Dz+1/Dz = 1,9; для элементов от тербия до лютеция эта величина ниже. Поэтому для всей группы РЗЭ можно принять β = 1,5. Для легких РЗЭ (La, Ce(III), Рг, Nd, Pm) коэффициенты распределения мало изменяются при увеличении концентрации их в растворах от 5–10 до 70–100 г/л: для средних PЗЭ (Sm, Eu, Gd) и тяжелых элементов (иттриевая группа) коэффициенты распределения существенно зависят от концентрации РЗЭ в водной фазе.
При использовании экстракции ТБФ для разделения РЗЭ на подгруппы процесс ведут из нитратных растворов с концентрацией HNO3 7–10 моль/л. При этом иттрий попадает в подгруппу тяжелых РЗЭ (Dy–Lu).
Катионообменные экстрагенты. Для разделения РЗЭ широко применяются моноосновные фосфорорганические кислоты: (RО)2РООН – диалкилфосфорные (Д2ЭГФК), (RО)RРООН – диалкилфосфоновые и R2РООН – диалкилфосфиновые, где R – алкильный или арильный радикал, причем в одном и том же соединении R может быть различным; а также алифатические монокарбоновые кислоты с прямой или разветвленной цепью CnH2n+1COOH (табл. 9).
Таблица 9. – Органические кислоты, используемые в качестве экстрагентов
| Органические кислоты | Структурная формула | Общая формула |
| Диалкилфосфорная кислота |  | (RО)2РООН |
| Диалкилфосфоновая кислота | 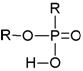 | (RО)RРООН |
| Диалкилфосфиновая кислота | 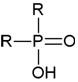 | R2РООН |
| Алифатические монокарбоновые кислоты с прямой цепью |  | CnH2n+1COOH |
| Алифатические монокарбоновые кислоты с разветвленной цепью |  | |
| Нафтеновые кислоты | 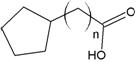 |
Экстракция РЗЭ из слабокислых растворов осуществляется согласно реакции обмена катиона экстрагируемого металла на протон (Н+) экстрагента:
Ln3+ вод + 3Н2A2орг ↔ Ln(НА2)3 орг + 3Н+вод (25)
Константа данной реакции будет равна:
K= 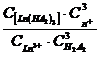 , (26)
, (26)
соответственно коэффициент распределения:
D=  (27)
(27)
Таким образом, уравнение (27) обусловливает следующую количественную связь: коэффициенты распределения РЗЭ прямо пропорциональны свободной концентрации экстрагента в третьей степени и обратно пропорциональны концентрации ионов водорода также в третьей степени.
Моноосновные фосфорорганические кислоты применяют обычно в виде растворов в неполярных растворителях (керосине, бензоле, октане и др.), что необходимо для снижения вязкости экстрагента. В этих растворителях молекулы кислот димеризованы.
В таблице 10 приведены коэффициенты разделения для бинарных смесей металлов. Коэффициенты разделения уменьшаются с повышением концентрации металлов и минеральной кислоты.
Таблица 10. – Факторы разделения РЗЭ при экстракции из бинарных смесей 1 моль/л Д2ЭГФК в додекане
| Смесь РЗЭ | СрзЭ, моль/л | С*, % | β |
| Соляная кислота | |||
| Еr–Но | 0,25—0,31 | >99,9 | 1,84 |
| 0,11–0,26 | < 0,1 | 3,52 | |
| Tm–Er | 0,19—0,26 | >99,9 | 2,36 |
| 0,20 | 70,0 | 2,79 | |
| 0,23 | 30,0 | 3,38 | |
| 0,19-0,32 | < 0,1 | 5,00 | |
| Yb–Tm | 0,037-0,11 | >99,9 | 2,50 |
| 0,15-0,27 | >99,9 | 2,29 | |
| 0,22 | 70,0 | 3,29 | |
| 0,21 | 30,0 | 3,58 | |
| 0,12-0,25 | < 0,1 | 5,50 | |
| (0,1-0,24) | (> 99,9) | (1,78) | |
| Lu–Yb | 0,13-0,16 | >99,9 | 1,53 |
| 0,12-0,20 | 0,1 | 2,61 | |
| (0,17-0,21) | (>99,9) | (1,23) | |
| Азотная кислота | |||
| Tm–Er | 0,13 | >99,9 | 2,14 |
| 0,20 | >99,9 | 2,05 | |
| Yb–Tm | 0,14 | >99,9 | 2,20 |
| 0,17 | >99,9 | 1,84 | |
| 0,21 | >99,9 | 1,78 | |
| 0,11-0,20 | < 0,1 | 4,26 |
Примечание. Концентрация кислоты в равновесной водной фазе составляла 5,0 моль/л, а для значений, приведенных в скобках, – 6 моль/л.
Концентрация более тяжелого лантаноида в бинарной смеси.
На практике фосфорорганические кислоты применяют в процессах выделения средних лантаноидов (Sm, Еu, Gd, Tb) из концентратов РЗЭ, приблизительно соответствующих по составу бастнезиту и лопариту.
Разделение легких лантаноидов экономически более выгодно проводить с применением экстрагентов другого класса, например, ранее рассмотренных НФОС (из-за значительно более высоких концентраций металлов в экстрактах и возможности осуществлять процесс в слабокислых средах). Тяжелые лантаноиды (Tb, Dy, Ho, Er, Tm, Yb, Lu) извлекаются фосфорорганическими кислотами с очень высокими коэффициентами распределения, однако это вызывает серьезные затруднения при реэкстракции металлов. Для успешного проведения реэкстракции требуется использовать сильно разбавленные растворы фосфорорганических кислот в неполярных растворителях на стадии экстракции и минеральные кислоты высокой концентрации при реэкстракции. К сожалению, это сопровождается снижением предельного содержания металлов в экстрактах (рабочий емкости).
Монокарбоновые кислоты с углеводородной цепью нормального строения (каприловая кислота – C7H15COOH, олеиновая кислота –C17H33COOH) обладают низкой селективностью при экстракции смесей РЗЭ. Их можно использовать на операциях концентрирования металлов, конверсии одних солей в другие (хлоридов в нитраты и др.) и для очистки всей группы РЗЭ от других металлов. Несколько большая селективность установлена для нафтеновых кислот. Наилучшие результаты среди монокарбоновых кислот получены для кислот с разветвленными углеводородными радикалами.
Анионообменные экстрагенты. Соли четвертичных аммониевых оснований (ЧАО) обладают наибольшей селективностью в ряду первичных, вторичных, третичных и четвертичных аминов при экстракции РЗЭ как из нитратных, так и из роданидных растворов [4].
Соли аминов и четвертичных аммониевых оснований извлекают РЗЭ из нитратных растворов в виде анионов вида Ln(NO3)3+qq-, где q=2–3. При этом нитратная группа координирована к металлу как бидентантный лиганд, катион четвертичного аммониевого основания располагается во внешней сфере центрального атома [7].
Экстракция РЗЭ из нитратных растворов солями четвертичных аммониевых оснований может быть представлена следующим уравнением:
Ln3+вод + 3NO3-вод + q[R3R´N·NO3]орг = [R3R´N]q+[Ln(NO3)3+q]q-орг (28)
Отличительной особенностью нитратных систем при использовании экстрагентов этого класс является уменьшение коэффициентов распределения с ростом порядкового номера лантаноида (рис. 20), что позволяет при сочетании ЧАО с комплексонами в водной фазе (например, этилендиаминтетрауксусной кислотой) достигнуть значительных факторов разделения даже для таких близких по свойствам элементов, как празеодим и неодим. Повышение селективности происходит за счет сложения факторов разделения, обусловленных ЧАО и комплексонами, которые совпадают по направленности разделения.
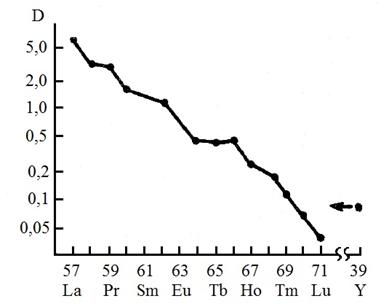
Рисунок 20. – Зависимость коэффициента распределения РЗЭ от порядкового номера элемента при экстракции нитратом бензилтриалкиламмония
(алкил С7-С9) в м -ксилоле.
Для экстракционного разделения РЗЭ могут быть использованы смеси экстрагентов различных классов, например, ТБФ и Д2ЭГФК, Д2ЭГФК и диизооктилфенилфосфорной кислоты (ДИОФФК); а также бинарные экстрагенты [8].
На практике в большинстве случаев процесс экстракционного разделения РЗЭ проводят в каскаде экстракторов типа смеситель – отстойник.
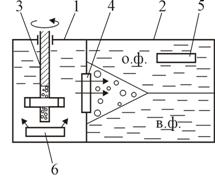
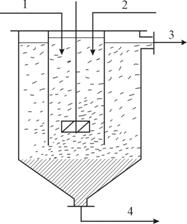
Смесители-отстойники состоят из смесительной и отстойной камер (рис. 21 а). В смесительной камере (1) водная и органическая фазы перемешиваются турбинной мешалкой (3), а затем смесь фаз передается в отстойную камеру (2). У внутреннего смеситель-отстойника обе камеры находятся в одном корпусе (рис. 21 б). Ряд смесителей-отстойников соединяется друг с другом, образуя каскад (рис. 22) так, что одна из фаз (чаще органическая) перетекает из одного аппарата в другой самотеком, а другая фаза насосами перекачивается противотоком к первой. В зависимости от операцию проводимой на каскаде, его так и называют - экстракционный, промывной, реэкстракционный и т.д.
 |  |
| а | б |
Рисунок 21. – а – Поперечный разрез экстрактора «ящичного типа». 1 – смесительная камера, 2 – отстойная камера, 3 – турбинная мешалка, 4 – жалюзийное окно, 5 – перелив органической фазы, 6 – перелив водной фазы;
б – Схема внутреннего смесителя-отстойника: 1 – исходный раствор; 2 – экстрагент;
3 – экстракт; 4 – рафинат.

Рисунок 22. – Каскад смесителей-отстойников. I – легкая фаза, II – тяжелая фаза
Перед экстракционным разделением раствор РЗЭ сначала направляют на очистную экстракцию, для очистки от различных примесей (Fe, Al, Ca и др).
В экстракционных каскадах при разделении РЗЭ используют систему полного противотока (водный раствор и органическая фаза движутся на встречу друг другу), которая состоит из секций[6] экстракции, промывки и реэкстаракции (рис. 21). Общее число ступеней каскада 50–90.
Исходный раствор, содержащий разделяемую смесь, поступает в среднюю часть каскада. Очевидно, что для разделения n элементов смеси потребуется проведение n-1 последовательных операций или n-1 экстракционных каскадов.
Первоначально в режиме полного противотока проводят разделение РЗЭ на подгруппы: легкие РЗЭ (La, Се, Pr, Nd), средние (Sm, Eu, Gd, Tb) и тяжелые (Dy–Lu + Y). Затем ведут дальнейшее разделение в каждой из подгрупп.
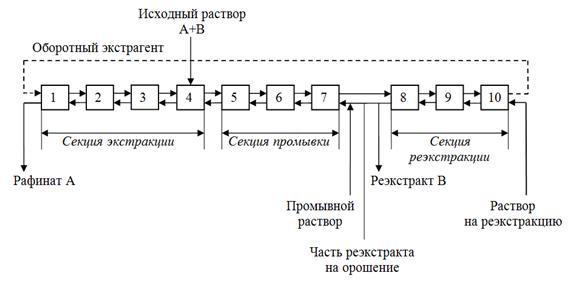
Рисунок 21. – Схема разделения РЗЭ экстракцией в системе полного противотока
В других вариантах разделения РЗЭ, в частности разделении бинарных смесей (А+В), например, неодима и самария, используют каскад с обменной промывкой. В этом случае в промывной каскад возвращают часть экстракта, содержащего лучше экстрагируемый компонент, например В. При этом в промывочном каскаде в результате контакта фаз компонент В вытесняет из органической фазы примесь компонента А. Это способствует получению более чистого компонента В, уменьшаются относительные расходы промывочного раствора и экстрагента.
В качестве примера использования групповой схемы разделения РЗЭ можно привести опыт освоения разделения концентрата РЗЭ, полученного из экстракционной фосфорной кислоты предприятия «ФосАгро-Череповец». Так полученный концентрат карбонатов РЗЭ, растворяют в азотной кислоте и упаривают для корректировки концентрации компонентов раствора. После этого раствор направляют на каскад очистной экстракции. Очистную экстракцию проводят на каскаде из 26 смесительно-отстойных экстракторов, для очистки от таких примесей как Ca, Al, Fe и др (рис. 22). В качестве экстрагента используют 100% трибутилфосфат. Промывку проводят раствором нитрата аммония с концентрацией ~600 г/л, подкисленным HNO3 до содержания 80–90 г/л. Реэкстрагирующий раствор – техническая оборотная вода, подкисленная до 5–15 г/л HNO3.
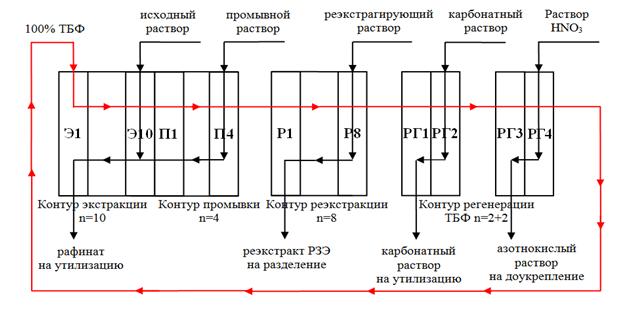
Рисунок 22. – Схема движения потоков в очистном экстракционном каскаде [9]
Для регенерации экстрагента используют карбонатно-бикарбонатный промывной раствор концентрацией ~100 г/л по сумме карбоната и бикарбоната аммония (85 и 15% соответственно) и азотнокислый раствор ~100 г/л по HNO3.
Реэкстракт очистной экстракции, перед разделительным каскадом, упаривают до 320–350 г/л (в пересчете на оксиды РЗ) и корректируют по HNO3 (до 20–35 г/л) и NH4NO3 (до 550–600 г/л). В качестве экстрагента на разделительном каскаде тоже используют 100% ТБФ, 44 смесительно-отстойных экстрактора. Схема движения потоков в разделительно экстракционном каскаде представлена на рисунке 23. Разделение проводят по линии Nd/Sm. Промывку осуществляют раствором нитрата самария с концентрацией 160–175 г/л по Sm2O3, 30–35 г/л HNO3, 500–550 г/л NH4NO3. Реэкстрагирующий раствор – техническая оборотная вода, подкисленная до 5 г/л азотной кислотой. Для регенерации экстрагента используется карбонатно-бикарбонатный промывной раствор, также как и в очистном каскаде. Реэкстракт представляет собой концентрат среднетяжелой группы, а рафинат – концентрат цериевой группы. Концентраты легкой и среднетяжелой групп, полученные в результате экстракционного разделения, перерабатываются путем осаждения карбонатов по традиционной методике.
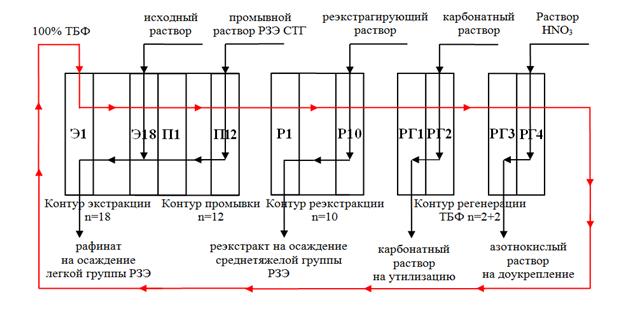
Рисунок 23. – Схема движения потоков в разделительном экстракционном каскаде [9]
Таким образом, в результате осуществления данной схемы получают два концентрата РЗЭ в виде влажных осадков карбонатов [9].
Еще один пример получения нескольких промежуточных концентратов иллюстрирует принципиальная схема, приведенная на рисунке 24. Схема экстракционного разделения РЗЭ из сернокислых растворов, полученных при переработке фосфатных минералов.
Экстракцию проводят Д2ЭГФК: в водной фазе остаются лантан, церий, празеодим и неодим; в органическую извлекаются: иттрий, все остальные РЗЭ и небольшое количество неодима. Дальнейшее получение промежуточных концентратов происходит на промывной части каскада. При промывке экстракта азотной кислотой с концентрацией 1,5 моль/л в водную фазу извлекаются диспрозий, гольмий, иттрий, эрбий и тулий; содержание иттрия в этом концентрате ≥ 75%. Наконец, иттербий и лютеций извлекаются 10% раствором NaOH. Полученные концентраты перерабатываются по своим схемам [10, 11].
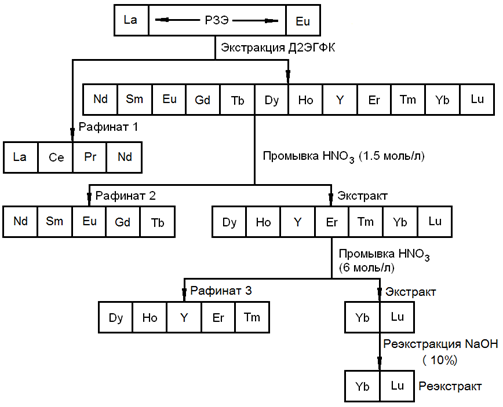
Рисунок 24. – Один из вариантов разделения РЗЭ из сульфатных растворов, образующихся при переработке фосфатных концентратов с получением групповых концентратов РЗЭ
Применяют различные схемы полного разделения РЗЭ, в которых сочетаются различные методы. Так эффективными методами является сочетание окислении-восстановления и экстракции. В качестве примера на рисунке 25 приведена схема разделения элементов цериевой группы. На разделение обычно поступает смесь гидроксидов, очищенная от примесей других элементов. Первоначально из смеси лантаноидов выделяют церий. Ce(IV) извлекается ТБФ значительно лучше Ce(III), его коэффициенты распределения на два порядка выше по сравнению с Ce(III) и другими лантаноидами (табл. 11). Окисление церия можно проводить различными методами: воздушным борбатитровнием; введением хлора, пероксида водорода или озона; электрохимическими методами (см. стр. 41 пособия). Затем из раствора содержащего РЗЭ методом противоточной экстракции получают три фракции: легкие РЗЭ (La, Се, Pr, Nd), средние РЗЭ (Pr, Nd, Sm, Eu) и фракцию, обогащенную гадолинием и элементами иттриевой группы (Nd, Sm, Eu, Gd+Yb). Из второй и третьей фракций можно выделить самарий и европий восстановлением амальгамой натрия. Разделение элементов в каждой из выделенных фракций проводят, используя методы экстракции и ионообменной хроматографии.
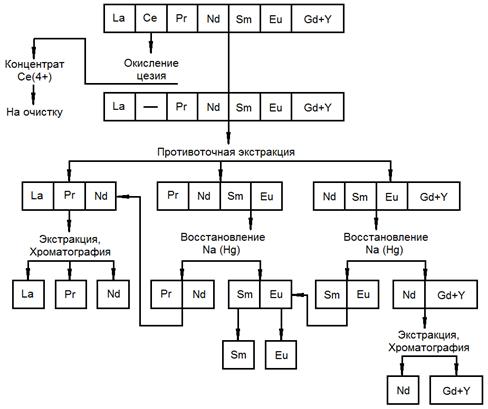
Рисунок 25. – Принципиальная схема разделения РЗЭ цериевой группы
Таблица 11. – Коэффициенты распределения церия (III), (IV) и лантана (III) при экстракции 100% ТБФ из азотнокислых растворов
| С(HNO3), М | DCe(IV) | С(HNO3), М | DCe(III) | С(HNO3), М | DLa(III) |
| 2,09 | 15,7 | 1,82 | 0,168 | 1,21 | 0,108 |
| 16,4 | 2,38 | 0,172 | 2,15 | 0,123 | |
| 3,76 | 23,3 | 3,64 | 0,169 | 3,17 | 0,124 |
| 4,69 | 45,7 | 5,2 | 0,133 | 4,27 | 0,102 |
| 5,21 | 47,5 | 0,11 | 6,10 | 0,076 | |
| 5,67 | 39,3 | 6,85 | 0,098 | 8,05 | 0,057 |
| 6,5 | 28,7 | 8,15 | 0,09 | 10,2 | 0,060 |
| 7,25 | 25,1 | 8,95 | 0,096 | 12,1 | 0,088 |
| 8,27 | 24,3 | 9,88 | 0,108 | 13,8 | 0,142 |
| 9,15 | 19,5 | 11,3 | 0,133 | 15,0 | 0,22 |
| 9,95 | 17,8 | 0,137 | – | – | |
| 10,65 | 7,3 | 12,9 | 0,195 | – | – |
| 12,2 | 5,7 | 13,9 | 0,28 | – | – |
При разделении элементов иттриевой подгруппы методом экстракции выделяют иттрий (например, используя экстракцию в хлоридно-роданидной системе) и две фракции: Gd, Tb, Dy, и Но, Er, Tu, Tb, Lu. Дальнейшее разделение ведут с использованием экстракции (методы полного противотока или полупротивотока) и ионообменной хроматографии. Иттербий выделяют восстановлением из нитратных растворов амальгамой натрия.
Необходимо отметить, что состав редкоземельных концентратов, поступающих на разделения, достаточно разнообразен, поэтому классические схемы разделения не всегда подходят. Примером такого нетрадиционного подхода разделения РЗЭ и отделения их от сопутствующих примесей может послужить принципиальная схема, приведенная на рисунке 26. Это схема экстракционного разделения редкоземельных и сопутствующих им металлов при переработке эвдиалитовых концентратов [13].
Исходный водный раствор (табл. 12) поступает на экстракцию раствором 0,5 М олеиновой кислоты (С18H34O2) с целью извлечения железа (III). Процесс экстракции ведут при рН = 4,0 в 4 ступени, при этом извлечение железа составляет 99 %. Экстракт железа может быть направлен на реэкстракцию растворами соляной или серной кислот с целью получения препаратов железа (III). Очищенный от железа (III) раствор направляется на следующую стадию экстракции 0,5 М раствором олеиновой кислоты, на которой получают коллективный экстракт церия и эрбия. Процесс ведут в четыре ступени при рН = 4,5, степени извлечения церия и эрбия равны 92% и 94% соответственно. Далее рафинат, содержащий алюминий, марганец, самарий, иттрий и лантан, отправляют на экстракцию 0,5 М раствором олеиновой кислоты при рН=5,0 в 3 ступени. В коллективный экстракт переходят иттрий и самарий, при этом степени извлечения иттрия и самария равны 90% и 96% соответственно. Полученный рафинат направляется на последнюю стадию экстракции с целью извлечения лантана. Процесс экстракции ведут в 4 ступени 0,5 М раствором нафтеновых кислот при рН = 5,5. Лантан фактически полностью переходит в экстракт, а в рафинате остаются марганец и алюминий. Извлечение лантана составляет 94%.
Таблица 12. – Содержание компонентов, направляемых на первый передел экстракции
| Элемент | Ce | La | Y | Sm | Er | Fe | Al | Mn |
| Концентрация, г/кг раствора | 3,15 | 0,95 | 0,81 | 0,26 | 0,062 | 5,5 | 7,3 | 8,25 |
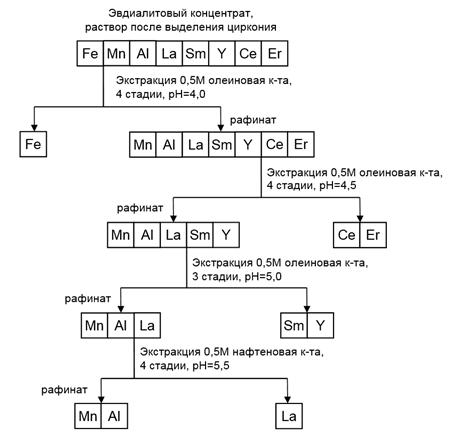
Рисунок 26. – Принципиальная технологическая схема экстракционного разделения железа, алюминия, марганца и некоторых РЗМ с применением растворов олеиновой и нафтеновых кислот в керосине при отношении объемов фаз О:В = 1:10 на каждой стадии.
Полученные экстракты РЗЭ отправляются на реэкстракцию с получением чистых реэкстрактов. Далее эти растворы, содержащие только ионы РЗЭ, отправляются на экстракцию растворами олеиновой кислоты с целью получения индивидуальных экстрактов, из которых получают товарные оксиды РЗЭ в соответствии с ТУ-48-4-524-90. Рафинат, содержащий ионы алюминия и марганца, может быть направлен на утилизацию или переработан на соединения, которые могут быть направлены на соответствующие металлургические предприятия.
 2017-12-14
2017-12-14 6674
6674








