При растворении в воде ионные комплексные соединения участвуют в первичной и вторичной диссоциации. При первичной диссоциации комплексные соединения распадаются по типу сильного электролита на ионы внешней и внутренней сферы (комплексные ионы):
K[Al(OH)4 → K+ + [Al(OH)4]−, [Cu(NH3)4]Cl2 → [Cu(NH3)4]2+ + 2Cl-.
Во вторичной диссоциации участвуют образовавшиеся комплексные ионы.
Вторичная диссоциация – многоступенчатый обратимый процесс, протекающий по типу слабого электролита с постепенным отщеплением лигандов от центрального атома:
Диссоциация иона [Al(OH)4]−:
1) [Al(OH)4]− ↔ OH+ + [Al(OH)3]0,
2) [Al(OH)3]0 ↔ OH− + [Al(OH)2]+,
3) [Al(OH)2]+ ↔ OH− + [Al(OH)]2+,
4) [Al(OH)]2+ ↔ OH− + Al3+.
Σ: [Al(OH)4]− ↔ 4OH− + Al3+
При обратимой вторичной диссоциации комплексного иона в растворе появляются ионы (атомы) центрального атома.
Нужно помнить: если при диссоциации комплексного иона отщепляется отрицательно заряженный лиганд, то заряд образующейся при диссоциации комплексной частицы изменяется на единицу.
Диссоциация иона [Cu(NH3)4]2+:
1) [Cu(NH3)4]2+ ↔ NH30 + [Cu(NH3)3]2+,
2) [Cu(NH3)3]2+ ↔ NH30 + [Cu(NH3)2]2+,
3) [Cu(NH3)2]2+ ↔ NH30 + [Cu(NH3)]2+,
4) [Cu(NH3)]2+ ↔ NH30 + Cu2+___
Σ: [Cu(NH3)4]2+ ↔ 4NH30 + Cu2+
Нужно помнить: если при диссоциации комплексного иона отщепляется электронейтральный лиганд, то заряд образующейся комплексной частицы не изменяется.
Так как каждая ступень вторичной диссоциации – обратимый процесс, то для любого из этих процессов на основании закона действующих масс можно вывести константу равновесия, которая имеет свое собственное название – константа нестойкости (неустойчивости) комплексного соединения (Кн.). Константу нестойкости комплексного соединения можно вывести для суммарного уравнения диссоциации комплексного иона (общая константа нестойкости).
Алгоритм вывода общей константы нестойкости
1. Провести анализ системы:
ν 1
[Al(OH)4]− ↔ 4OH− + Al3+
ж ν 2 ж ж
2. Указать условия существования химического равновесия: ν 1 = ν 2
3. На основании закона действующих масс записать значения скоростей реакции ν 1 и ν 2:
ν 1 = [Al(OH)4−] K1,
ν 2 = [OH−]4[Al3+] K2, где K1, K2 – постоянные величины.
4. Подставить полученные значения скоростей реакций в математическое выражение ν 1 = ν 2: [Al(OH)4−]K1= [OH−]4 [Al3+]K2.
5. Преобразовать уравнение, полученное в п.4 относительно постоянных величин K1, K2 :
K1 = [OH−]4 [Al3+].
K2 [Al(OH)4−]
6. Т.к. K1, K2 – постоянные величины, то частное от их деления – величина постоянная Кр или Кн: Кр = Кн = K1
K2
7. Записать значение Кн:
Кн = [OH−]4 [Al3+].
[Al(OH)4−]
8. Определить величину Кн. по справочнику (таблица 4): Кн. = 10-33.
По значениям констант нестойкости устанавливают устойчивость комплексных соединений. Чем меньше значения константы нестойкости комплексного соединения, тем устойчивее комплексное соединение, тем легче оно образуется при протекании химической реакции в растворе, тем труднее диссоциирует комплексный ион.
Константы нестойкости соединений К[Al(OH)4] и [Cu(NH3)4]Cl2 соответственно равны 1,0 ∙ 10-33 и 2,0 ∙ 10-13. Следовательно, более устойчивым является комплексное соединение алюминия.
Кроме значений констант нестойкости для установления устойчивости комплексных соединений используют значения констант устойчивости комплексных соединений (Куст.).
Константа устойчивости – обратная величина константы нестойкости: Куст. = 1/Кн. Она может быть выведена на основании частных уравнений ступенчатого образования комплексного иона или общего уравнения его образования: Al3+ + 4OH− ↔ [Al(OH)4]−
(по алгоритму вывода константы любого химического равновесия).
Реакционная способность комплексных соединений зависит от значений констант нестойкости (устойчивости). Комплексные соединения могут участвовать в реакциях обмена ионов внешней сферы, лигандов и ионов центрального атома.
Строение атома
Задание 1
Составить электронную формулу атома фосфора и её графическое изображение в нормальном и возбуждённом состояниях. Указать все возможные степени окисления атома и его окислительно-восстановительные свойства. Привести примеры соединений элемента в устойчивых степенях окисления.
Решение:
Для составления электронной формулы атома элемента необходимо знать порядковый номер элемента в периодической системе Д.И. Менделеева (он указывает на заряд ядра атома и число электронов в атоме) и реальную схему распределения электронов в многоэлектронном атоме (она имеет следующий вид: 1s2 → 2s2 → 2p6 → 3s2 → 3p6 → 4s2 →3d10 → 4p6 →5s2 →4d10 → 5p6 → 6s2 → 5d1 → 4f14 → 5d9 → 6p6 → 7s2....., где цифра перед буквой указывает номер энергетического уровня, заполняемого электронами, буква после цифры - название подуровня в уровне, число над буквой – максимальное число электронов в данном подуровне). Порядковый номер атома фосфора в периодической системе 15, следовательно, в атоме фосфора 15 электронов, которые в соответствии с реальной схемой нужно распределить по энергетическим уровням и подуровням, составив электронную формулу. Она имеет следующий вид:
Р15е 1s2 2s2 2p6 3s2 3p3
Так как в электронной формуле последним электронами заполняется р-подуровень, то фосфор относится к семейству р-элементов. У р-элементов валентные электроны находятся в s- и р-подуровнях последнего энергетического уровня, следовательно, валентными электронами у фосфора будут пять электронов, находящихся в 3s2 3p3-подуровнях. Для этого уровня составляем схему графического изображения электронной формулы и распределяем в ней валентные электроны атома в нормальном состоянии (номер уровня указывает на число подуровней в уровне):
Р 








 3d
3d
 3p
3p
3s
Если в последнем уровне у атома любого элемента есть непарные электроны, то он последовательно может их отдавать, проявляя положительные степени окисления и являясь восстановителем:
Р0 – 1е → Р+1
Р0 – 2е → Р+2
Р0 – 3е → Р+3
восстановитель
Следовательно, атом фосфора может иметь положительные степени окисления равные +1, +2, +3. Последняя степень окисления атома фосфора является устойчивой. Нужно помнить, что р-элементы четвёртой-седьмой групп могут не только отдавать электроны, но и принимать их.
Если у атома р-элемента валентных электронов в последнем уровне больше 3, то он может принимать электроны для построения устойчивого 8-электронного состояния последнего валентного уровня. Поэтому, чтобы узнать сколько электронов принимает элемент, нужно из 8 вычесть число валентных электронов атомов р-элементов 4-7-ой групп. У атома фосфора 5 валентных электронов, следовательно, для построения устойчивого 8-электронного состояния он должен принять 3 электрона (8-5=3):
Р0 + 1е → Р-1
Р0 + 2е → Р-2
Р0 + 3е → Р-3
Окислитель
Принимая электроны, элемент проявляет отрицательные степени окисления и является окислителем. Следовательно, в нормальном состоянии атом фосфора может иметь следующие отрицательные степени окисления: -1, -2, -3. Последняя степень окисления будет устойчивой. Любой элемент может образовывать простое вещество, в котором атом элемента имеет нулевую степень окисления, она является устойчивой.
Таким образом, атом фосфора в нормальном состоянии имеет следующие устойчивые степени окисления: -3, 0, +3 и может быть как окислителем, так и восстановителем. В устойчивых состояниях атом фосфора входит в состав следующих соединений:
Р-3Н3, Р0, Р+32О3, Н3Р+3О3, Р+3Сl3.
Если у атома, находящегося в нормальном состоянии, в последнем уровне есть парные электроны и свободные атомные орбитали, то такой атом может возбуждаться. При возбуждении атома (связанного с получением энергии извне) происходит перемещение одного из парных электронов последнего энергетического уровня в ближайшую свободную атомную орбиталь этого уровня. Возбуждённое состояние атома фосфора имеет вид:
Р* 
















 3d
3d
 3p
3p
3s
В возбуждённом состоянии у атома увеличивается число непарных электронов, которые атом последовательно может отдавать, принимая положительные степени окисления и являясь восстановителем. Таким образом, атом фосфора в возбуждённом состоянии может отдавать последовательно 5 электронов и иметь следующие степени окисления: +1, +2, +3, +4, +5. Последняя степень окисления атома фосфора является устойчивой. В этой устойчивой степени окисления атом фосфора входит в состав оксида Р2О5, гидроксидов НРО3, Н3РО4, Н4Р2О7 и солей КН2РО4, К2НРО4, К3РО4.
Задание 2
Составить электронную формулу атома железа и её графическое изображение в нормальном и возбуждённом состояниях атома. Указать возможные степени окисления атома железа и его окислительно-восстановительные свойства. Привести примеры соединений железа в устойчивых степенях окисления.
Решение:
Так как порядковый номер железа в периодической системе 26, то его электронная формула имеет вид:
Fe26е 1s2 2s2 2p6 3s2 3p6 4s2 3d6
Последним в атоме железа заполняется d-подуровень, поэтому атом железа относится к семейству d-элементов. У d-элементов валентные электроны находятся в s-подуровне последнего энергетического уровня и d-подуровне предпоследнего энергетического уровня, поэтому у атома железа 8 валентных электронов: 4s2, 3d6.
Графическое изображение электронной формулы (валентных уровней) атома железа в нормальном состоянии имеет вид:
 |
Fe 






 4p
4p
4s
3d
Так как в последнем энергетическом уровне у атома железа нет непарных электронов, то он в нормальном состоянии не может отдавать электроны (запомните: d-элементы не принимают электроны), не вступает в химические реакции, имеет нулевую (устойчивую) степень окисления и образует простое вещество: Fe0.
В последнем уровне у атома железа есть пара электронов и свободные валентные атомные орбитали, поэтому атом железа может находиться в возбуждённом состоянии:
Fe 



* 






 4p
4p
4s
Нужно помнить, что при возбуждении атома возможен переход электронов только в последнем валентном уровне. Студенты часто допускают грубейшие ошибки, перенося один из парных валентных электронов d-подуровня предпоследнего уровня в s- или р-подуровни последнего уровня.
В возбуждённом состоянии атом может отдавать все непарные валентные электроны, проявляя положительные степени окисления и являясь восстановителем (запомните: d-элементы только отдают электроны, имеют только положительные степени окисления и в свободном состоянии являются только восстановителями). Так как у атома железа в возбуждённом состоянии 6 непарных валентных электронов, то он может иметь следующие положительные степени окисления: +1, +2, +3, +4, +5, +6. Последняя степень окисления является устойчивой. Кроме степени окисления +6, у железа устойчивыми в соединениях являются степени окисления +2 и +3 (для каждого d-элемента нужно запомнить устойчивые степени окисления). В экзаменационных билетах из d-элементов могут быть следующие: Cr, Fe, Mn, Co, Ni, Mo, Cu, Zn. Примерами соединений железа в устойчивых степенях окисления могут быть простое вещество Fe0, оксиды FeO, Fe2O3, гидроксиды Fe(OH)2, Fe(OH)3, соли FeCl2, FeCl3, K2FeO4.
Задание 3
Составить электронную формулу атома меди и её графическое изображение в основном (нормальном) и возбуждённом состояниях. Указать возможные степени окисления атома и его окислительно-восстановительные свойства в каждом из состояний. Привести примеры соединений в устойчивых степенях окисления.
Решение:
При составлении электронных формул атомов d-элементов наблюдается явление проскока (провала) электронов – самопроизвольный переход электронов с s-подуровня последнего уровня в d-подуровень предпоследнего уровня. К таким d-элементам относится атом меди (явление провала электронов наблюдается в атомах следующих d-элементов: Cu, Ag, Au, Cr, Mo, Nb, Ru, Rh, Pd, Pt). В результате провала электронов в s-подуровне последнего энергетического уровня атома меди остаётся один электрон, т. к. один электрон из 4s-подуровня в результате провала переходит в 3d-подуровень. В связи с этим электронная формула атома меди имеет следующий вид:
Cu29e 1s2 2s2 2p6 3s2 3p6 4s1 3d10.
В атоме меди 11 валентных электронов: 4s1 3d10.
Графическое изображение атома меди в основном состоянии:


 Cu
Cu


4s 4p








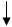

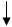

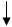
3d
Возможные степени окисления: 0, +1. Атом Cu в основном состоянии проявляет свойства восстановителя, т. к. может отдать один электрон:
Cu0 – 1e → Cu+1.
Нужно помнить: если в результате провала электрона в d-подуровне предпоследнего энергетического уровня образуется пара электронов, то при сообщении атому такого элемента энергии происходит возвращение проскочившего электрона из d-подуровня предпоследнего уровня в s-подуровень последнего энергетического уровня, а затем переход этого электрона в р-подуровень последнего энергетического уровня, т. е. атом может возбуждаться:
Cu*

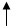



 4p
4p









 4s
4s
3d
В возбуждённом состоянии у атома меди появляется три непарных валентных электрона, которые он может отдавать, проявляя положительные степени окисления +1, +2, +3 и являясь восстановителем.
Примеры соединений меди: Cu0, Cu+12O, Cu+2SO4, KСu+3O2.
Задание 4
Составить электронную формулу атома азота и её графическое изображение. Указать возможные степени окисления и окислительно-восстановительные свойства атома азота в основном (нормальном) состоянии. Показать, каким образом у атома азота появляются степени окисления +4, +5. Привести примеры соединений азота в устойчивых степенях окисления.
Решение:
В атоме азота 7 электронов. Электронная формула: 1s2 2s2 2p3. Азот р-элемент, валентных электронов 5, неметалл.
N







2p
2s
Так как р-элементы IV-VII групп могут как отдавать электроны так и принимать электроны, то атом азота в основном (нормальном)состоянии может как отдавать, так и принимать электроны, проявляя свойства и окислителя, и восстановителя. Имея три непарных электрона в последнем энергетическом уровне атом азота может последовательно их отдавать, приобретая положительные степени окисления и являясь восстановителем: 0, +1, +2, +3 – восстановитель.
Имея 5 валентных электронов в последнем уровне атом азота может последовательно принимать (8-5=3) три электрона для достройки 8-и электронного состояния последнего валентного уровня. При этом атом будет приобретать отрицательные степени окисления, являясь окислителем: -1, -2, -3 – окислитель. Таким образом, атом азота в основном состоянии и окислитель, и восстановитель.
В учебниках рассматриваются соединения азота в степенях окисления -3, 0, +1, +2, +3, +4, +5.
В валентном уровне атома азота есть пара электронов в 2s-подуровне, однако нет валентных свободных орбиталей. Поэтому возбуждение атома азота невозможно.
Одним из вариантов объяснения появления степеней окисления +4, +5 у атома азота является следующий. Атом азота, имея три непарных валентных электрона в последнем уровне является очень активным и легко отдаёт один электрон, превращаясь в атом со степенью окисления +1, который имеет пару валентных электронов и свободную валентную орбиталь в 2р-подуровне:
N0










 – 1е N+1
– 1е N+1



2p 2p
2s 2s
Такой атом может легко возбуждаться:
N+1* 






2p
2s
В возбуждённом состоянии атом азота N+1 имеет четыре непарных электрона, последовательно их отдаёт, приобретая степени окисления +2, +3,+4, +5 и являясь восстановителем. -3 -3 +1 +2 +3 +4 +5
Примеры соединений азота: NH3, NH4OH, N20, N2O, NO, KNO2, NO2, KNO3.
 2017-11-01
2017-11-01 1331
1331
