Электрохимические устройства и процессы
Так как окислительно-восстановительные реакции сопровождаются переносом заряда, то их можно осуществлять действием электрического тока, и наоборот, - получать электрический ток за счет их протекания. В соответствующих процессах и устройствах используются электроды и электродные потенциалы.
Понятие об электродном потенциале.
Если металлическую пластинку опустить в воду или раствор, содержащий ионы этого металла, то на границе раздела металл-раствор за счет процессов растворения-осаждения металла возникает разность или скачок потенциала, который зависит от природы металла, концентрации раствора, а также от температуры. Этот скачок называется электродным потенциалом данного металла. Указанное равновесие выражается уравнением, учитывающим гидратацию иона:
 Ме + mH2O Me n+(H2O)m + ne.
Ме + mH2O Me n+(H2O)m + ne.
в растворе на металле
Потенциал, соответствующий данному равновесию, называется равновесным электродным потенциалом.
Значение j нельзя определить по абсолютной величине. Поэтому потенциалы всех электродов определяют по отношению к стандартному водородному полуэлементу (электроду) (рис. 7.1), потенциал которого принимают равным нулю: jо298 (2Н+ ® Н2) = 0. Стандартный водородный электрод состоит из сосуда с 1н. раствором кислоты, в которую опущен платиновый электрод, контактирующий с газообразным водородом, находящимся под давлением Р = 101,3 кПа.
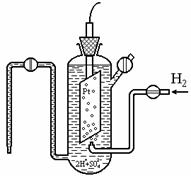
Рис. 7.1. Стандартный водородный электрод
 На электроде устанавливается равновесие 2Н+р + 2? Н2 (г). Нулевое значение jо для этого электрода определяется и тем, что DG0f (Н+) = DG0f (Н2) = 0. Платина используется вследствие ее инертности, а также потому, что она является катализатором переноса электрона (процесс установления равновесия ускоряется, но само состояние равновесия, то есть функции DН, DU, DG, DS, остается неизменными при постоянной температуре).
На электроде устанавливается равновесие 2Н+р + 2? Н2 (г). Нулевое значение jо для этого электрода определяется и тем, что DG0f (Н+) = DG0f (Н2) = 0. Платина используется вследствие ее инертности, а также потому, что она является катализатором переноса электрона (процесс установления равновесия ускоряется, но само состояние равновесия, то есть функции DН, DU, DG, DS, остается неизменными при постоянной температуре).
Потенциалы, определенные относительно стандартного электрода в стандартных условиях (то есть jо298) табулированы. Для металлов по химическим данным (Н.Н. Бекетовым), а затем путем измерения jо298 установлен ряд активности металлов, который в настоящее время имеет назавание электрохимический ряд напряжения металлов (табл.12.1).
Таблица 12.1
Стандартные электродные потенциалы j0 некоторых металлов
(ряд напряжения)
| Электрод | j 0, В | Электрод | j 0, В | Электрод | j 0,В |
| Li+/Li | -3,045 | Mn2+/Mn | -1,18 | 2H+/H2 | 0,000 |
| Rb+/Rb | -2,925 | Cr2+/Cr | -0,913 | Sb3+/Sb | +0,20 |
| K+/K | -2,924 | Zn2+/Zn | -0,763 | Bi3+/Bi | +0,215 |
| Сs+/Cs | -2,923 | Cr3+/Cr | -0,74 | Cu2+/Cu | +0,34 |
| Ba2+/Ba | -2,90 | Fe2+/Fe | -0,44 | Сu+/Cu | +0,52 |
| Ca2+/Ca | -2,87 | Сd2+/Cd | -0,403 | Hg22+/2Hg | +0,79 |
| Na+/Na | -2,714 | Сo2+/Co | -0,27 | Ag+/Ag | +0,80 |
| Mg2+/Mg | -2,37 | Ni2+/Ni | -0,25 | Hg2+/Hg | +0,85 |
| Al3+/Al | -1,70 | Sn2+/Sn | -0,136 | Pt2+/Pt | +1,19 |
| Ti2+/Ti | -1,603 | Pb2+/Pb | -0,127 | Au3+/Au | +1,50 |
| Zr4+/Zr | -1,58 | Fe3+/Fe | -0,037 | Au+/Au | +1,70 |
Электродный потенциал, измеренный при стандартных условиях
(Т = 298К; [Mеn+] = 1моль/л) относительно стандартного водородного электрода, называется стандартным электродным потенциалом металла и обозначается j0. Стандартный электродный потенциал является количественной характеристикой химической активности металла, т.е. его способности отдавать свои валентные электроны и переходить в раствор в виде ионов.
Основные свойства ряда напряжения.
Чем меньше величина j, тем сильнее выражена восстановительная активность металла.
Если условия отличаются от стандартных, то для расчета электродного потенциала используется формула Нернста:

где j 0 - стандартный электродный потенциал металла,
n - число электронов, принимающих участие в процессе,
F - постоянная Фарадея (96500 Кл/моль),
R - универсальная газовая постоянная (8,31 Дж·моль-1·К-1),
Т – абсолютная температура (К).
Если в приведенном уравнении заменить постоянные числовыми значениями, то оно примет следующий вид:
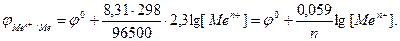
Из формулы Нернста видно, что при стандартной концентрации катионов, равной 1М φ = j 0, т.е. равновесный электродный потенциал металла равен его стандартному потенциалу.
 2014-02-02
2014-02-02 8732
8732
