Скорость химической реакции равна изменению концентрации реагирующего вещества в единицу времени.
Различают среднюю скорость 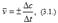 где Δс=с2-с1 – изменение концентрации вещества за промежуток времени Δt=t2-t1. Знак (+) означает, что вещество образуется, а знак (-) – что вещество расходуется в ходе реакции.
где Δс=с2-с1 – изменение концентрации вещества за промежуток времени Δt=t2-t1. Знак (+) означает, что вещество образуется, а знак (-) – что вещество расходуется в ходе реакции.
Основными факторами, определяющими скорость реакции, являются концентрация, температура и катализатор. Скорость реакций с участием газообразных реагентов зависит также от давления.
Зависимость скорости реакции от температуры. Для большинства реакций справедливо правило Вант-Гоффа: Повышение температуры на 10К увеличивает скорость большинства реакций в 2-4 раза: 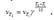 (3.9) где
(3.9) где 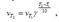 - скорости реакции при Т1 и Т2; γ – термический коэффициент скорости химической реакции
- скорости реакции при Т1 и Т2; γ – термический коэффициент скорости химической реакции 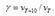
Молекулы газов и жидкостей испытывают ежесекундно огромное число столкновений. Только очень малая доля столкновений заканчивается химическими превращениями. Такие столкновения называются эффективными соударениями. Молекулы - активными молекулами с большей энергией. Избыточная энергия необходима молекулам для преодоления сил отталкивания внешних электронных оболочек и для образования активированного комплекса, т.е. промежуточного соединения между исходными веществами и конечными продуктами. В активированном комплексе старые связи еще не полностью разрушены, а новые еще не полностью образовались.
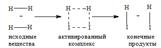

Изменение энергии в ходе химической реакции показано схемой процесса активации (рис.3.2). По оси ординат отложена потенциальная энергия системы. Абсцисса - координата реакции или реакционного пути. В процессе химического превращения переход системы из начального состояния с энергией ΣНi в конечное состояние с ΣНf происходит через энергетический барьер.
Энергия активации (Е*) - это энергия, необходимая для перевода в состояние активированного комплекса 1 моль реагирующих веществ. Разность ΣНf - ΣНi составляет тепловой эффект реакции (ΔrH). Для обратной реакции тепловой эффект будет иметь ту же величину, но противоположный знак. Для обратной реакции энергия активации составит величину.
Зависимость константы скорости химической реакции от температуры описывается уравнением Аррениуса: 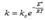 (3.10)
(3.10)
где k – константа скорости реакции; ko – константа, зависящая от природы реагирующих веществ; Е* - энергия активации; R – универсальная газовая постоянная; Т – температура, К- константа скорости, а следовательно и скорость химической реакции экспоненциально растет с увеличением температуры.
19.Необратимые и обратимые процессы. Химическое равновесие. Константа равновесия. Смещение химического равновесия. Принцип Ле Шателье.
ОБРАТИМЫЕ И НЕОБРАТИМЫЕ ПРОЦЕССЫ, пути изменения состояния термодинамич. системы. Процесс наз. обратимым, если он допускает возвращение рассматриваемой системы из конечного состояния в исходное через ту же последовательность промежут. состояний, что и в прямом процессе, но проходимую в обратном порядке. При этом в исходное состояние возвращается не только система, но и среда. Обратимый процесс возможен, если и в системе, и в окружающей среде он протекает равновесно. При этом предполагается, что равновесие существует между отдельными частями рассматриваемой системы и на границе с окружающей средой. Обратимый процесс - идеализир. случай, достижимый лишь при бесконечно медленном изменении термодинамич. параметров. Скорость установления равновесия должна быть больше, чем скорость рассматриваемого процесса. Если невозможно найти способ вернуть и систему, и тела в окружающей среде в исходное состояние, процесс изменения состояния системы наз. необратимым.
Необратимые процессы могут протекать самопроизвольно только в одном направлении; таковы диффузия, теплопроводность, вязкое течение и др. Для хим. р-ции применяют понятия термодинамич. и кинетич. обратимости, к-рые совпадают только в непосредств. близости к состоянию равновесия. Р-ция А + В 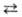 С + D наз. кинетически обратимой или двусторонней, если в данных условиях продукты С и D могут реагировать друг с другом с образованием исходных в-в А и В. При этом скорости прямой и обратной р-ций, соотв.
С + D наз. кинетически обратимой или двусторонней, если в данных условиях продукты С и D могут реагировать друг с другом с образованием исходных в-в А и В. При этом скорости прямой и обратной р-ций, соотв. 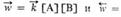
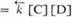 , где
, где 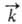 и
и 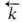 -константы скорости, [А], [В], [С], [D]- текущие концентрации (активности), с течением времени становятся равными и наступает химическое равновесие, в к-ром
-константы скорости, [А], [В], [С], [D]- текущие концентрации (активности), с течением времени становятся равными и наступает химическое равновесие, в к-ром 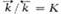 -константа равновесия., зависящая от т-ры. Кинетически необратимыми (односторонними) являются обычно такие р-ции, в ходе к-рых хотя бы один из продуктов удаляется из зоны р-ции (выпадает в осадок, улетучивается или выделяется в виде малодиссоциированного соед.), а также р-ции, сопровождающиеся выделением большого кол-ва тепла.
-константа равновесия., зависящая от т-ры. Кинетически необратимыми (односторонними) являются обычно такие р-ции, в ходе к-рых хотя бы один из продуктов удаляется из зоны р-ции (выпадает в осадок, улетучивается или выделяется в виде малодиссоциированного соед.), а также р-ции, сопровождающиеся выделением большого кол-ва тепла.
Химическое равновесие — состояние химической системы, в котором обратимо протекает одна или несколько химических реакций, причём скорости в каждой паре прямая-обратная реакция равны между собой. Для системы, находящейся в химическом равновесии, концентрации реагентов, температура и другие параметры системы не изменяются со временем. А2 + В2 ⇄ 2AB
В состоянии равновесия скорости прямой и обратной реакции становятся равными.
Смещение химического равновесия
Положение химического равновесия зависит от следующих параметров реакции: температуры, давления и концентрации. Влияние, которое оказывают эти факторы на химическую реакцию, подчиняются закономерности, которая была высказана в общем виде в 1885 году французским ученым Ле-Шателье.
Факторы влияющие на химическое равновесие:
1.температура
При увеличении температуры химическое равновесие смещается в сторону эндотермической (поглощение) реакции, а при понижении в сторону экзотермической (выделение) реакции.
CaCO3=CaO+CO2 -Q t↑ →, t↓ ←
N2+3H2↔2NH3 +Q t↑ ←, t↓ →
2.давление
При увеличении давления химическое равновесие смещается в сторону меньшего объёма веществ, а при понижении в сторону большего объёма. Этот принцип действует только на газы, т.е. если в реакции участвуют твердые вещества, то они в расчет не берутся.
CaCO3=CaO+CO2 P↑ ←, P↓ →
1моль=1моль+1моль
3.концентрация исходных веществ и продуктов реакции
При увеличении концентрации одного из исходных веществ химическое равновесие смещается в сторону продуктов реакции, а при увеличении концентрации продуктов реакции-в сторону исходных веществ.
S2+2O2=2SO2 [S],[O]↑ →, [SO2]↑ ←
Катализаторы не влияют на смещение химического равновесия!
Конста́нта равнове́сия — величина, определяющая для данной химической реакции соотношение между термодинамическими активностями (либо, в зависимости от условий протекания реакции, парциальными давлениями, концентрациями или фугитивностями) исходных веществ и продуктов в состоянии химического равновесия (в соответствии с законом действующих масс). Зная константу равновесия реакции, можно рассчитать равновесный состав реагирующей смеси, предельный выход продуктов, определить направление протекания реакции.
Принцип Ле Шателье
Чтобы легче понять принцип Ле Шателье, рассмотрим простую химическую реакцию. Два вещества (реактивы) взаимодействуют друг с другом, в результате взаимодействия образуется третье вещество (продукт), которое стремится к расщеплению на исходные вещества. Это можно изобразить в виде следующего уравнения: A + B <—> C
Двойная стрелка обозначает обратимую реакцию. При протекании прямой реакции слева направо происходит образование вещества C из веществ A и B. В случае обратной реакции (справа налево) вещество C расщепляется на вещества A и B. Когда эта система находится в химическом равновесии, скорости прямой и обратной реакций одинаковы — в одной точке данной системы образуется молекула вещества C, а где-то в другом месте другая молекула вещества С распадается.
Если в систему добавить избыток вещества A, равновесие временно нарушится, так как вырастет скорость образования вещества C. Но чем быстрее будет расти концентрация вещества C, тем быстрее оно будет расщепляться — пока снова не будет достигнуто равновесие между прямой и обратной реакциями. Тогда скорость образования вещества C из веществ A и B сравняется со скоростью расщепления вещества С на вещества A и B.
20.Жидкие растворы. Энтальпия растворения. Сольваты (гидраты). Кристаллогидраты. Кристаллизационная вода.
Жидкий раствор — раствор веществ в жидкой агрегатной фазе.
Жидкие растворы, как и жидкие вещества, обладают внутренней структурой ближнего порядка. При этом структура разбавленных растворов ближе к структуре растворителя, а концентрированных — к структуре растворенного вещества.
Стандартная энтальпия растворения — Δ H раство, тепловой эффект процесса растворения 1 моля вещества в бесконечно большом количестве растворителя. Складывается из теплоты разрушения кристаллической решетки и теплоты гидратации (или теплоты сольватации для неводных растворов), выделяющейся в результате взаимодействия молекул растворителя с молекулами или ионами растворяемого вещества с образованием соединений переменного состава — гидратов (сольватов).
СОЛЬВАТЫ - продукты присоединения растворителя к растворенным веществам. Частный случай сольваты -гидраты (р-ритель-вода). Обычно сольваты образуются в растворе, но нередко (при охлаждении раствора, испарении растворителя и др.) м. б. получены в виде кристаллич. фаз-кристаллосольватов.
Кристаллогидраты — кристаллы, содержащие молекулы воды и образующиеся, если в кристаллической решётке катионы образуют более прочную связь с молекулами воды, чем связь между катионами и анионами в кристалле безводной соли. При низких температурах вода в кристаллогидратах может быть связана как с катионами, так и с анионами солей. Многие соли, а также кислоты и основания выпадают из водных растворов в виде кристаллогидратов.
Кристаллизационная вода принимает участие в строении кристаллических решеток различных минералов. Кристаллизационная вода входит в состав минералов типа CaSO4•2H2O (гипс). Кристаллизационная вода, участвуя в построении кристаллической решетки минералов, сохраняет свою молекулярную форму.
 2015-01-13
2015-01-13 1893
1893
