Термодинамическая энтропия S, часто просто именуемая энтропия, в химии и термодинамике является функцией состояния термодинамической системы.
Термодинамическое определение энтропии
Понятие энтропии было впервые введено в 1865 году Рудольфом Клаузиусом. Он определил изменение энтропии термодинамической системы при обратимом процессе как отношение изменения общего количества тепла ΔQ к величине абсолютной температуры T: 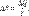
Рудольф Клаузиус дал величине S имя «энтропия», происходящее от греческого слова τρoπή, «изменение» (изменение, превращение, преобразование). Данное равенство относится к изменению энтропии, не определяя полностью саму энтропию.
Эта формула применима только для изотермического процесса (происходящего при постоянной температуре). Её обобщение на случай произвольного квазистатического процесса выглядит так: 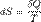 , где dS - приращение (дифференциал) энтропии, а δQ - бесконечно малое приращение количества теплоты.
, где dS - приращение (дифференциал) энтропии, а δQ - бесконечно малое приращение количества теплоты.
Необходимо обратить внимание на то, что рассматриваемое термодинамическое определение применимо только к квазистатическим процессам (состоящим из непрерывно следующих друг за другом состояний равновесия).
Поскольку энтропия является функцией состояния, в левой части равенства стоит её полный дифференциал. Напротив, количество теплоты является функцией процесса, в котором эта теплота была передана, поэтому δQ считать полным дифференциалом нельзя.
Энтропия, таким образом, согласно вышеописанному, определена вплоть до произвольной аддитивной постоянной. Третье начало термодинамики позволяет определить её точнее: предел величины энтропии равновесной системы при стремлении температуры к абсолютному нулю полагают равным нулю.
Статистическое определение энтропии: принцип Больцмана
В 1877 году Людвиг Больцман нашёл, что энтропия системы может относиться к количеству возможных «микросостояний» (микроскопических состояний), согласующихся с их термодинамическими свойствами. Рассмотрим, например, идеальный газ в сосуде. Микросостояние определено как позиции и импульсы (моменты движения) каждого составляющего систему атома. Связность предъявляет к нам требования рассматривать только те микросостояния, для которых: (I) месторасположения всех частей расположены в рамках сосуда, (II) для получения общей энергии газа кинетические энергии атомов суммируются. Больцман постулировал, что: 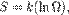 где константу k=1,38•10–23 Дж/К мы знаем теперь как постоянную Больцмана, а Ω является числом микросостояний, которые возможны в имеющемся макроскопическом состоянии (статистический вес состояния). Этот постулат, известный как принцип Больцмана, может быть оценен как начало статистической механики, которая описывает термодинамические системы, используя статистическое поведение составляющих их компонентов. Принцип Больцмана связывает микроскопические свойства системы (Ω) с одним из её термодинамических свойств (S).
где константу k=1,38•10–23 Дж/К мы знаем теперь как постоянную Больцмана, а Ω является числом микросостояний, которые возможны в имеющемся макроскопическом состоянии (статистический вес состояния). Этот постулат, известный как принцип Больцмана, может быть оценен как начало статистической механики, которая описывает термодинамические системы, используя статистическое поведение составляющих их компонентов. Принцип Больцмана связывает микроскопические свойства системы (Ω) с одним из её термодинамических свойств (S).
Согласно определению Больцмана, энтропия является просто функцией состояния. Так как Ω может быть только натуральным числом (1,2,3,…), то энтропия Больцмана должна быть положительной — исходя из свойств логарифма.
16.Энергия Гиббса системы. Направленность химических процессов. Энергия Гиббса образования вещества. Расчет энергии Гиббса реакции в стандартных условиях и температурах отличных от стандартных.
Свободная энергия Гиббса (или просто энергия Гиббса, или потенциал Гиббса, или термодинамический потенциал в узком смысле) — это величина, показывающая изменение энергии в ходе химической реакции и дающая таким образом ответ на принципиальную возможность протекания химической реакции; это термодинамический потенциал следующего вида:G=U+PV-TS
Энергию Гиббса можно понимать как полную химическую энергию системы (кристалла, жидкости и т. д.)Понятие энергии Гиббса широко используется в термодинамике и химии. Самопроизвольное протекание изобарно-изотермического процесса определяется двумя факторами: энтальпийным, связанным с уменьшением энтальпии системы (ΔH), и энтропийным T ΔS, обусловленным увеличением беспорядка в системе вследствие роста ее энтропии. Разность этих термодинамических факторов является функцией состояния системы, называемой изобарно-изотермическим потенциалом или свободной энергией Гиббса (G, кДж)
Энергия Гиббса и направление протекания реакции
В химических процессах одновременно действуют два противоположных фактора — энтропийный (TΔS) и энтальпийный (ΔH). Суммарный эффект этих противоположных факторов в процессах, протекающих при постоянном давлении и температуре, определяет изменение энергии Гиббса (G): 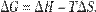 Из этого выражения следует, что
Из этого выражения следует, что 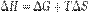 , то есть некоторое количество теплоты расходуется на увеличение энтропии (TΔS), эта часть энергии потеряна для совершения полезной работы, её часто называют связанной энергией. Другая часть теплоты (ΔG) может быть использована для совершения работы, поэтому энергию Гиббса часто называют также свободной энергией.Характер изменения энергии Гиббса позволяет судить о принципиальной возможности осуществления процесса. При ΔG < 0 процесс может протекать, при ΔG > 0 процесс протекать не может (иными словами, если энергия Гиббса в исходном состоянии системы больше, чем в конечном, то процесс принципиально может протекать, если наоборот — то не может). Если же ΔG = 0, то система находится в состоянии химического равновесия.Обратите внимание, что речь идёт исключительно о принципиальной возможности протекания реакции. В реальных же условиях реакция может не начинаться и при соблюдении неравенстваΔG < 0 (по кинетическим причинам).Существует полезное соотношение, связывающее изменение свободной энергии Гиббса
, то есть некоторое количество теплоты расходуется на увеличение энтропии (TΔS), эта часть энергии потеряна для совершения полезной работы, её часто называют связанной энергией. Другая часть теплоты (ΔG) может быть использована для совершения работы, поэтому энергию Гиббса часто называют также свободной энергией.Характер изменения энергии Гиббса позволяет судить о принципиальной возможности осуществления процесса. При ΔG < 0 процесс может протекать, при ΔG > 0 процесс протекать не может (иными словами, если энергия Гиббса в исходном состоянии системы больше, чем в конечном, то процесс принципиально может протекать, если наоборот — то не может). Если же ΔG = 0, то система находится в состоянии химического равновесия.Обратите внимание, что речь идёт исключительно о принципиальной возможности протекания реакции. В реальных же условиях реакция может не начинаться и при соблюдении неравенстваΔG < 0 (по кинетическим причинам).Существует полезное соотношение, связывающее изменение свободной энергии Гиббса 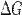 в ходе химической реакции с её константой равновесия
в ходе химической реакции с её константой равновесия 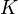 :
: 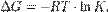
Вообще говоря, любая реакция может быть рассмотрена как обратимая (даже если на практике она таковой не является). При этом константа равновесия определяется как 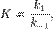 где
где 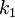 — константа скорости прямой реакции,
— константа скорости прямой реакции, 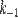 — константа скорости обратной реакции.
— константа скорости обратной реакции.
В закрытой системе знак изменения энергии Гиббса является критерием направленности самопроизвольного процесса при проведении его в изобарно-изотермических условиях:
- при dG = 0 (G=Gmin, энергия Гиббса имеет минимальное значение) система находится в состоянии термодинамического равновесия;
- при dG < 0 (Ga Gmin, энергия Гиббса убывает) процесс самопроизвольно протекает в прямом направлении, т.е. термодинамически возможен;
- при dG > 0 (Ga Gmin, энергия Гиббса возрастает) самопроизвольно протекает только обратный процесс, прямой процесс термодинамически невозможен.
Стандартную энергию Гиббса химической реакции при Т = 298К можно рассчитать двумя способами: используя уравнение Гиббса-Гельмгольца: drGТ0 = dr НТ0 - ТdrSТ0, в которое нужно подставить указанное значение Т, и по стандартным энергиям Гиббса образования исходных веществ и продуктов реакции dfG2980.
Стандартную энтальпию реакции dr Н2980 находят по первому
drН298О = Sn'i dfН' 298i О -Sni dfН 298 i О
или второму следствию из закона Гесса
drН298О = Sn'i dсН' 298i О -Sni dсН 298 i О
а стандартную энтропию реакции
drS298О = Sn' i S' 298 О -Sni S298 О.
При расчете необходимо учитывать, что единицей измерения энтальпии является килоджоуль, а энтропии Дж\К.
Энергия Гиббса является функцией состояния системы, поэтому ее можно рассчитать с использованием табличных значений стандартных энергий Гиббса образования исходных веществ и продуктов реакции
drG298О = Sn'i dfG' 298i О -Sni dfG 298 i О
Стандартной энергией Гиббса образования вещества dfG298 О называют стандартную энергию Гиббса реакции образования 1 моль данного соединения из простых веществ, находящихся в термодинамически устойчивых модификациях, которая проведена в стандартных термодинамических условиях.
В отсутствие справочных данных по dfG298 О какого-либо сложного вещества эту величину можно вычислить по уравнению dfG298О = dfН298 О - 298 df S 298 О, где dfН298 О и df S 298 О – стандартные энтальпия и энтропия соответственно реакции образования 1 моль этого соединения из простых веществ, находящихся в термодинамически устойчивых состояниях, проведенной при стандартных термодинамических условиях.Энергия Гиббса(G)- называемая также изобарно-термическим потенциалом или свободной порцией при постоянном давлении. G связана с H,S,T: G=H-TS. Если реакция осуществляется при постоянн08щых P и Т, то ∆G=∆H-T∆S. При постоянстве температуры и давления хим.реакции могут самопроизвольно протекать только в таком направлении, при котором энергия Гиббса системы уменьшается. При низких температурах самопроизвольно могут протекать экзотермические реакции, а при высоких – рекции сопровождающиеся влечение энтропии.
| Знак изменения ф-ии | Самопроизвольное протекание | ||
| ∆Н | ∆S | ∆G | |
| - + - + | + - - + | - + +/- +/- | Возможно при любых температурах Невозможно при любых температурах Возможно при достаточно низких температурах Возможно при достаточно высоких температурах |
 2015-01-13
2015-01-13 5563
5563
