Алкенами называют углеводороды, содержащие в своем составе двойную связь, представляющую собой сочетание d- и p- связи. Атомы углерода при двойной связи находятся в состоянии sp2-гибридизации. Общая формула алкенов CnH2n.
Изомерия. В ряду алкенов имеет место структурная и геометрическая изомерия.
Структурная изомерия в алкенах обусловлена не только различным характером соединения атомов углерода в углеводородном скелете, но и различным положением двойной связи:
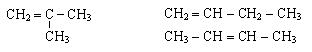
Геометрическая изомерия (цис-, транс-изомерия) в алкенах обусловлена затруднением вращения алкильных групп вокруг d-связи. Этому вращению препятствует π-связь.
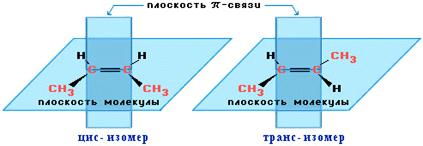
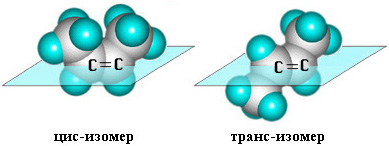
Номенклатура. Для названияэтиленовых углеводородов используют тривиальные названия, рациональную и систематическую номенклатуры.
Тривиальные названия (этилен, пропилен, бутилен и т.д.).
По рациональной номенклатуре углеводороды рассматриваются как замещенные этилена: называются алкильные радикалы и добавляется слово этилен.
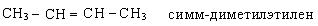
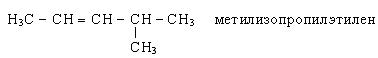

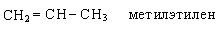
По систематической номенклатуре название алкенов дается от соответствующих алканов с заменой окончания «ан» на «ен». Нумерацию углеводородной цепочки начинают с того конца, где ближе двойная связь. Остальные принципы составления названий остаются теми же, что и для предельных углеводородов.
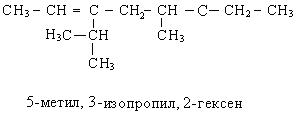
Способы получения алкенов. Существует несколько способов получения алкенов:
1. Алкены выделяют из газов крекинга нефти.
2. Дегидрирование алканов:
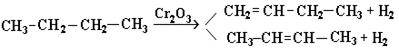
3. Дегидратация спиртов:
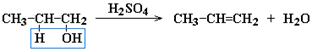
Механизм реакции:
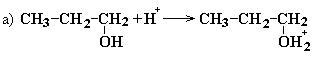
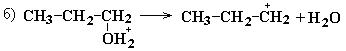
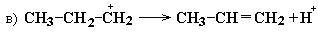
Легче всего в реакцию дегидратации вступают третичные спирты, затем вторичные и только потом первичные. Этот вывод согласуется с величинами энергии активации, необходимой для образования промежуточной структуры карбкатиона:
третичные ñ вторичные ñ первичные
Кроме того, этот вывод находится в соответствии с теорией устойчивости карбкатионов, согласно которой третичный карбкатион наиболее устойчив, а любая реакция преимущественно протекает через стадию образования наиболее устойчивого карбкатиона. Стабильность третичного карбкатиона обусловлена высокой степенью делокализации заряда в карбкатионе.
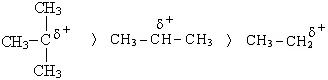
В случае дегидратации сложных спиртов следует руководствоваться правилом Зайцева, согласно которому при дегидратации с гидроксилом отщепляется атом водорода от соседнего наименее гидрогенезированного атома углерода:
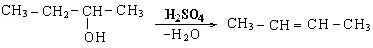
3. Дегидрогалогенирование галогеналканов:
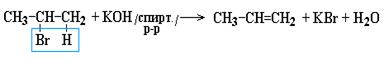
При этом соблюдается следующая последовательность в реакционной способности галогеналканов:
третичные ñ вторичные ñ первичные
4. Взаимодействие дигалогенпроизводных с металлами:
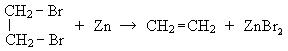
Химические свойства алкенов. В этиленовых углеводородах p-связь обладает меньшей энергией, чем d-связь, поэтому p-связь легко разрывается и присоединяет реакционные частицы. p-связь представляет собой зону повышенной электронной плотности, поэтому к ней будут стремиться присоединиться электрофильные частицы, следовательно, типичными реакциями алкенов являются реакции электрофильного присоединения (АdE). Кроме этого, алкены вступают в реакции окисления, полимеризации, замещения.
Реакции электрофильного присоединения (АdЕ):
1. Гидрогалогенирование:
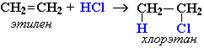
Механизм реакции:
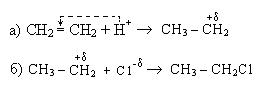
При гидрогалогенировании несимметричных алкенов следует руководствоваться правилом Морковникова, согласно которому электрофильная частица направляется к более гидрогенизированному по двойной связи атому углерода. Такой порядок присоединения объясняется электронными эффектами, действующими в молекуле:
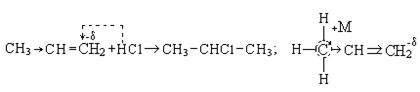
Положительный индукционный эффект алкильной группы приводит к смещению электронной плотности к последнему углеродному атому, вследствие чего электрофильная частица к нему и стремится. Электронная плотность на этом углеродном атоме больше также за счет эффекта сопряжения (+М) в алкильной группе.
Правило Морковникова можно объяснить и с точки зрения стабильности образовавшихся карбкатионов:
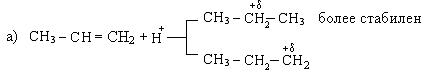
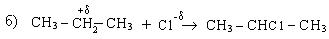
2. Гидратация алкенов также протекает по правилу Морковникова:
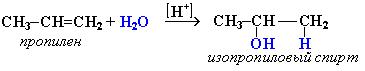

Механизм реакции:
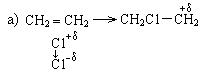
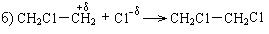
Реакции окисления. Алкены окисляются кислородом воздуха или другими окислителями. Направление окисления зависит от условий реакции и выбора окислителя.
1. При окислении алкенов кислородом воздуха без катализатора образуются спирты и карбонильные соединения:
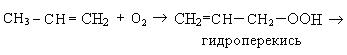
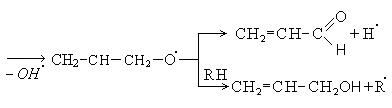
Возможен и другой механизм образования гидроперекиси, которая распадается до карбонильных соединений и кислот:
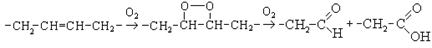
Этот процесс происходит при порче жиров и масел.
2. Окисление разбавленными растворами окислителей в нейтральной среде приводит к образованию гликолей (реакция Вагнера):
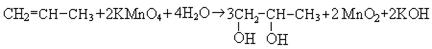
3. Окисление концентрированными растворами сильных окислителей (HNO3, KMnO4, хромовая кислота) приводит к разрыву углеводородной цепочки и образованию карбонильных соединений и кислот:
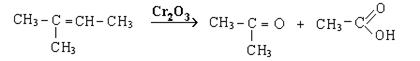
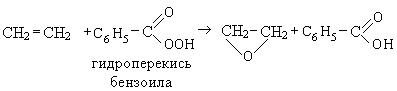
4. Окисление надкислотами (реакция Прилежаева):
5. Окисление кислородом воздуха в присутствии серебряного катализатора:
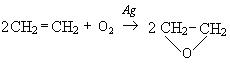
Реакции полимеризации. Полимеризацией называется процесс образования молекул высокомолекулярного вещества (полимера) путем соединения друг с другом по месту главных валентных связей молекул исходного вещества (мономера). Если в этой реакции участвуют смеси мономеров, то это реакция называется реакцией сополимеризации. Если в качестве побочного продукта в реакции полимеризации образуется вода, то такая реакция называется поликонденсацией. В зависимости от механизма реакции полимеризации делятся на: реакции радикальной полимеризации и реакции ионной полимеризации.
Реакция полимеризации может быть также линейная (цепная) и ступенчатая (миграционная). В случае линейной полимеризации происходит быстрое нарастание массы полимера и промежуточные продукты выделить невозможно. Во втором случае происходит медленное нарастание молекулярной массы и возможно образование димеров, тримеров, которые можно выделить:
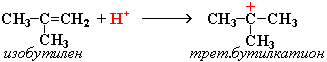
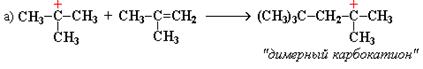
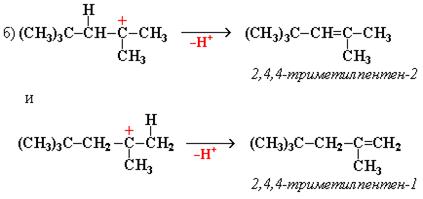
Общая схема классификации реакций полимеризации имеет вид:
 | |||||
 |  |
1. Радикальная полимеризация. Инициаторами реакции выступают радикалы. Полимеризация этилена в этом случае протекает при давлении 1000 атм и температуре 100°С. В этих условиях образуется полиэтилен высокого давления (ПВД).
Механизм реакции:
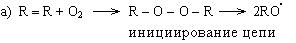
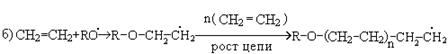
в) обрыв цепи происходит двумя путями:
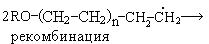
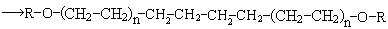
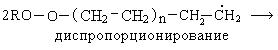
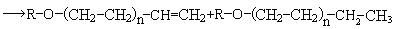
Полиэтилен, полученный в этих условиях, имеет разветвленную, неупорядоченную структуру, что обусловлено образованием разветвленных полимерных цепей вдоль основной линейной:
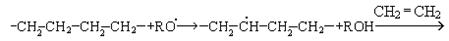
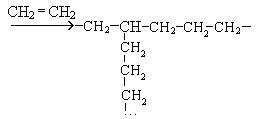
Полиэтилен высокого давления обладает низкими качественными характеристиками и используется для изготовления деталей, получаемых литьем и штамповкой, для изготовления пленки, используемой в пищевой промышленности, а также пищевых открытых емкостей.
В условиях радикальной полимеризации легко полимеризуются мономеры, содержащие акцентарные группы:
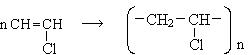
винилхлорид поливинилхлорид (ПВХ)
Поливинилхлорид в смеси с нитрильным каучуком (40%) используются для изготовления пакетов для молока, оберточной пленки.
Полимеризация тетрафторэтилена позволяет получить политетрафторэтилен (тефлон):
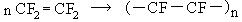
тетрафторэтилен политетрафторэтилен
2. Катионная полимеризация. Инициаторами реакции выступают электрофильные частицы (Н2SO4, HF, BF3· Н2O):
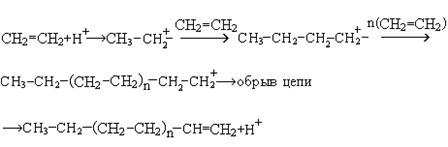
В реакцию катионной полимеризации этилен вступает с большим трудом, легче полимеризуются мономеры, содержащие донорные заместители (изобутилен).
В условиях катионной полимеризации также получаются полимеры атактической структуры.
3.Анионная полимеризация.Инициатором анионной полимеризации выступает анион или нуклеофильная частица (Z-). Процесс протекает по схеме:
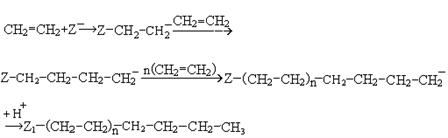
Обрыв цепи происходит с присоединением электрофильной частицы.
В условиях анионной полимеризации также получаются полимеры атактической структуры.
До 1953 года осуществляли в основном радикальную и ионную полимеризацию, которая проходила с образованием атактических полимеров. В 1953 году были открыты особые катализаторы, позволяющие осуществлять стереохимический контроль над процессами полимеризации. Эти комплексные катализаторы называются катализаторами Цинглера-Натта, по имени ученых, предложивших их:
TiCl4 + Me(C2H5)3 + Li
Механизм реакции полимеризации с использованием катализаторов следующий:
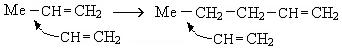
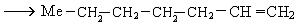
и так далее.
Аналогично проходит полимеризация пропилена, при этом возможно образование двух пространственных структур полимера – изотактической и синдиотактической:
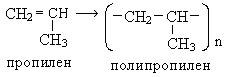
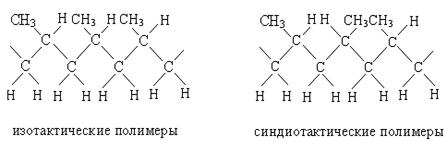
Полипропилен, полученный в этих условиях, имеет высокие качественные характеристики ― кристаллическую структуру, твердый, прочен. Применяется при изготовлении канатов, лески, рыболовецкой снасти, ковровых изделий.
Реакции замещения. Кроме реакций электрофильного присоединения, в ряду алкенов возможны и реакции замещения, протекающие по радикально-цепному механизму (SR):
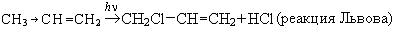
Применение. Этилен используется как сырье в органическом синтезе. Кроме того, этилен — это известный фитогормон, ускоряет созревание плодов, всхожесть семян.
 2015-03-20
2015-03-20 8000
8000








