Диеновыми называются углеводороды, которые содержат в своем составе две двойные связи. Общая формула алкадиенов СnH2n – 2. Атомы углерода по двойной связи находятся в состоянии sp2-гибридизации.
Диеновые углеводороды в зависимости от расположения двойных связей делятся на:
- углеводороды с кумулированными двойными связями:
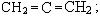
- углеводороды с сопряженными двойными связями:
СН2 = СН – СН = СН2;
- углеводороды с изолированными двойными связями:
СН2 = СН – СН2 – СН = СН2.
Номенклатура. Существуют тривиальные названия диеновых углеводородов (ален, дивинил, изопрен) и систематическая номенклатура. По систематической номенклатуре соблюдаются те же правила, что и в названии алкенов, только окончание «ен» заменяется на «-диен»:

Особый интерес среди диеновых углеводородов представляют углеводороды с сопряженными двойными связями. Наибольшее практическое значение имеют дивинил, или 1, 3 - бутадиен (легко сжижающийся газ, т. кип = – 4,5 °C), и изопрен, или 2 - метил - 1, 3 - бутадиен (жидкость с т. кип = 34 °С). По химическим свойствам диеновые углеводороды подобны алкенам. Они легко вступают в реакции присоединения и окисления. Однако сопряженные диены отличаются некоторыми особенностями, которые обусловлены делокализацией (рассредоточением) p-электронов. Молекула 1, 3 - бутадиена СН2 = СН - СН = СН2 содержит четыре атома углерода, которые находятся в состоянии sp2 - гибридизации, и имеет плоское строение.
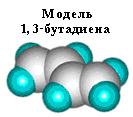
p-электроны двойных связей образуют единое p-электронное облако (сопряженную систему) и делокализованы между всеми атомами углерода.
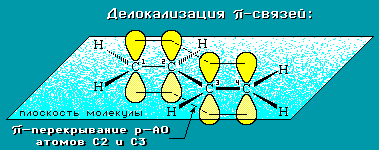
Порядок связей между атомами углерода имеет промежуточное значение между одинарной и двойной, т.е. нет чисто одинарной и чисто двойных связей.
Получение диеновых углеводородов. Общие способы получения диенов аналогичны способам получения алкенов.
1. Дегидрирование алканов.
Этим путем получают в промышленности дивинил из бутана:
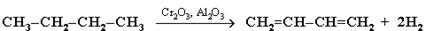
Каталитическим дегидрированием изопентана (2-метилбутана) получают изопрен:
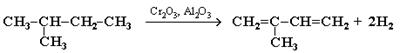
2. Синтез дивинила по Лебедеву:
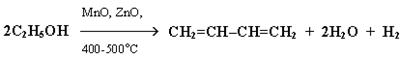
3. Дегидратация гликолей (двухатомных спиртов, или алкандиолов):
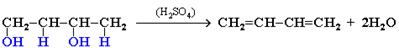
4. Действие спиртового раствора щелочи на дигалогеналканы:
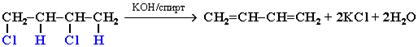
5. Получение из отходов бродильных производств:
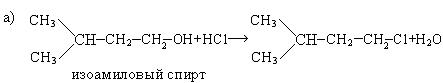
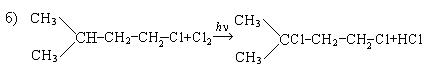
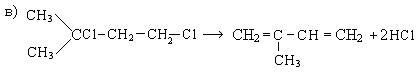
Химические свойства. Типичными реакциями диеновых углеводородов, так же как и алкенов, являются реакции электрофильного присоединения и полимеризации.
Реакции электрофильного присоединения (АdЕ). Электронные особенности сопряженных диенов приводят к тому, что реакции АdE протекают в 1, 2- и 1, 4 - положениях:
1. Галогенирование:
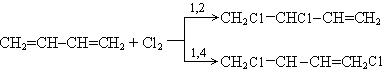
Механизм реакции:
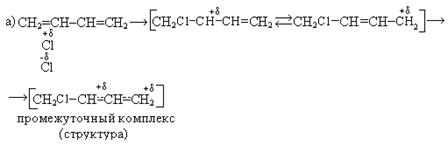
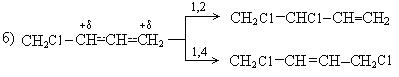
В зависимости от изменения условий реакции мы можем регулировать выходы продуктов 1, 2- и 1, 4 - присоединения.
Бромирование диеновых углеводородов проходит аналогично:
1, 2 - присоединение:
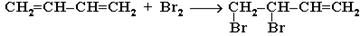
1, 4 - присоединение:
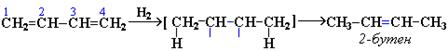
При избытке брома присоединяется еще одна его молекула по месту оставшейся двойной связи с образованием 1, 2, 3, 4 - тетрабромбутана.
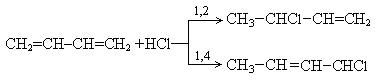
2. Гидрогалогенирование. Реакция также протекает в 1, 2- и 1, 4 - положениях:
3. Гидрирование. При гидрировании 1, 3 - бутадиена преимущественно получается 2 - бутен, т.е. происходит 1, 4 - присоединение. При этом двойные связи разрываются, к крайним атомам углерода С1 и С4 присоединяются атомы водорода, а свободные валентности образуют двойную связь между атомами С2 и С3:
В присутствии катализатора Ni получается продукт полного гидрирования:
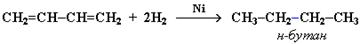
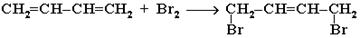
Присоединение галогенов, галогенводородов, воды и других полярных реагентов происходит, как уже сказано, по механизму электрофильного присоединения. К реакциям присоединения можно также отнести реакции д имеризации, характерные для диенов. Подобные конденсации получили название диеновых синтезов.
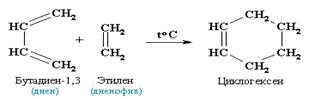
4. Диеновый синтез (реакция Дильса-Альдера). В органическом синтезе широко применяется реакция присоединения к сопряженным диенам соединений, содержащих кратные связи (так называемых диенофилов). Реакция идет как 1, 4 - присоединение и приводит к образованию циклических продуктов:
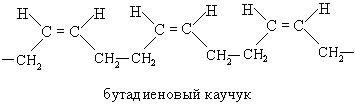
Реакции полимеризации. Диеновые углеводороды с сопряженными связями способны полимеризоваться с образованием каучуков. Важнейшими мономерами для получения каучуков являются дивинил, изопрен и 2, 3 - диметилбутадиен.
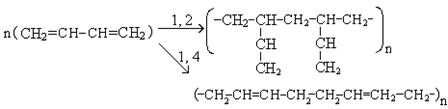
До 1950 года полимеризацию диенов проводили в условиях радикального механизма. При этом получались атактические структуры, далекие от свойств натурального каучука.
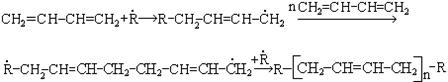
Использование катализаторов Цинглера-Натта позволило получать каучук с упорядоченной структурой:
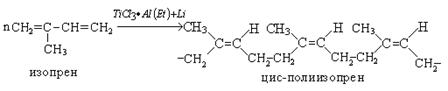
Основу полимерной структуры натурального каучука составляет цис-полиизопрен. Аналог натурального каучука был получен синтетически с использованием катализаторов Цинглера-Натта:
Транс-полиизопрен называется гуттаперчей:
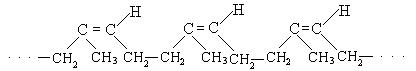
транс-полиизопрен (гуттаперча)
Для практического использования каучуки превращают в резину. Резина – это вулканизованный каучук, где в качестве наполнителя используется сажа. Суть процесса вулканизации заключается в том, что нагревание смеси каучука и серы приводит к образованию трехмерной сетчатой структуры из линейных макромолекул каучука, придавая ему повышенную прочность. Атомы серы присоединяются по двойным связям макромолекул и образуют между ними сшивающие дисульфидные мостики:
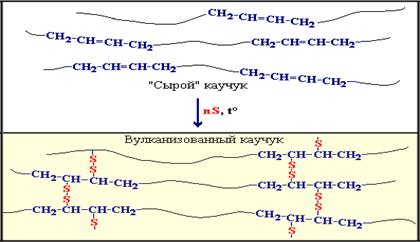
Сетчатый полимер более прочен и проявляет повышенную упругость – высокоэластичность (способность к высоким обратимым деформациям). В зависимости от количества сшивающего агента (серы) можно получать сетки с различной частотой сшивки. Предельно сшитый натуральный каучук – эбонит – не обладает эластичностью и представляет собой твердый материал. Вулканизация устраняет липкость полимеров, повышает эластичность. Резина используется для изготовления шин.
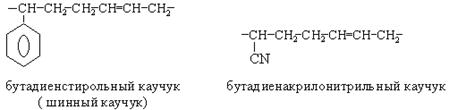
Большое значение имеет сополимеризация диеновых углеводородов с другими мономерами – стиролом, акрилонитрилом:
 2015-03-20
2015-03-20 26444
26444








