Эхокардиографическое исследование клапанного аппарата при инфекционном эндокардите имеет важное практическое значение, поскольку во многих случаях оно позволяет выявить прямые признаки этого заболевания — вегетации на клапанах, если их размеры превышают 2–3 мм. Большей информативностью (около 70–80%) в данном случае обладает М-модальное исследование. Отличаясь более высокой разрешающей способностью, оно позволяет обнаружить низкоамплитудные высокочастотные систолические вибрации, связанные с повреждением створок клапанов. Вегетации обнаруживаются в виде множества дополнительных эхосигналов, как бы «размывающих» изображение движущихся створок клапана («лохматые» створки) (рис. 9.8, а).
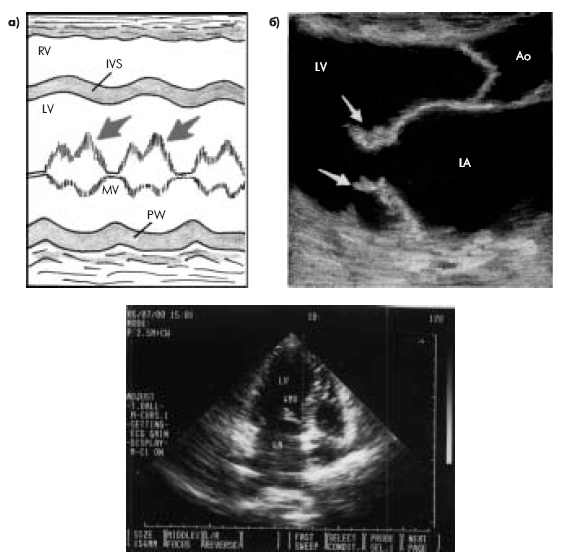 |
| Рис. 9.8. Эхокардиографические признаки вегетаций на створках митрального клапана: а-одномерная эхокардиограмма(схема); б-двухмерная эхокардиограмма (фрагмент); в-двухмерная эхокардиограмма из апикальной позиции четырехкамерного сердца |
Двухмерная эхокардиография позволяет не только визуализировать вегетации, но и оценить их форму, величину и подвижность (рис. 9.8, б, в). Подвижные вегетации имеют обычно несколько вытянутую форму. Одним своим концом они прикрепляются к створкам, а другой конец свободно перемещается с током крови, как бы независимо от движения самих створок. Например, при поражении трехстворчатого клапана вегетации то всплывают в полости ПП (в систолу), то появляются в полости ПЖ (в диастолу) (рис. 9.9).
Неподвижные вегетации представляют собой небольшие утолщения на створках клапана, которые относительно прочно связаны с ними и полностью повторяют движения створок.
Одним из тяжелых осложнений инфекционного эндокардита является разрыв сухожильных нитей митрального клапана, что вызывает патологическое движение соответствующей створки. Разрыв хорд задней или передней створки сопровождается хаотичными крупноамплитудными колебаниями створок и систолическим пролабированием их в полость ЛП. При двухмерной эхокардиографии иногда можно непосредственно визуализировать разорванные хорды, свободно перемещающиеся в полости ЛЖ.
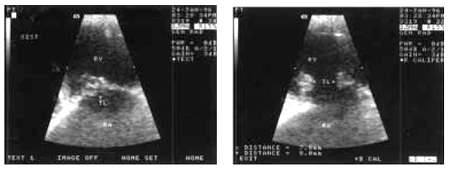 |
| Рис. 9.9. Подвижные вегетации на створках трикуспидального клапана: а-систола; б-диастола (вегетации обращены в полость правого желудочка) |
| 9.5. Критерии диагностики инфекционного эндокардита |
Диагноз инфекционного эндокардита основывается на выявлении нескольких ведущих признаков:
· лихорадка выше 38°C;
· относительно быстрое формирование недостаточности аортального, митрального или трикуспидального клапанов;
· наличие сопутствующих иммунных поражений (гломерулонефрит, миокардит, узелки Ослера, геморрагии, пятна Лукина и др.);
· эхокардиографическое выявление вегетаций на створках клапанов или признаки «нового» порока сердца;
· положительные результаты посева крови на стерильность;
· анемия, лейкоцитоз с нейтрофилезом, увеличение СОЭ;
· увеличение селезенки и др.
Диагностическое значение каждого из перечисленных признаков неодинаково. Поэтому для правильной и своевременной диагностики инфекционного эндокардита необходим анализ всей клинической картины заболевания, анамнестических данных, результатов лабораторных и инструментальных методов исследования.
В прошлом классическими признаками инфекционного эндокардита считалась триада симптомов: лихорадка, анемия, шум. В настоящее время наибольшее распространение в клинической практике получили так называемые Duke -критерии диагностики инфекционного эндокардита, отражающие современные возможности диагностики этого заболевания (табл. 9.2).
Таблица 9.2
Duke -критерии диагностики инфекционного эндокардита (в модификации)
| Большие критерии |
| 1. Положительные результаты посева крови А. Наличие в двух отдельных пробах крови одного из типичных возбудителей инфекционного эндокардита: · S. viridans · S. bovis · Группы HACEK · S. aureus · Энтерококки Б. Стойкая бактериемия (независимо от выявленного возбудителя), определяемая: · или в двух и более пробах крови, взятых с интервалом 12 ч, · или в трех и более пробах крови, взятых с интервалом не менее 1 ч между первой и последней пробами |
| 2. Эхокардиографические признаки поражения эндокарда А. ЭхоКГ-изменения, характерные для инфекционного эндокардита: · подвижные вегетации · абсцесс фиброзного кольца · новое повреждение искусственного клапана Б. Развитие недостаточности клапана (по данным ЭхоКГ) |
| Малые критерии |
| 1. Наличие заболевания сердца, предрасполагающего к развитию инфекционного эндокардита, или внутривенное введение наркотиков 2. Лихорадка выше 38°С 3. Сосудистые осложнения (эмболии крупных артерий, септический инфаркт легкого, микотические аневризмы, внутричерепное кровоизлияние, кровоизлияния в конъюнктиву) 4. Иммунные проявления (гломерулонефрит, узелки Ослера, пятна Рота, ревматоидный фактор) 5. Микробиологические данные (положительные результаты посева крови, не соответствующие основному критерию, или серологические признаки активной инфекции микроорганизмом, способным вызвать инфекционный эндокардит) 6. Эхокардиографические данные (соответствующие диагнозу инфекционного эндокардита, но не отвечающие основному критерию) |
Диагноз инфекционного эндокардита считается установленным, если присутствуют:
· 2 больших критерия или
· 1 большой и 3 малых критерия или
· 5 малых критериев.
| 9.6. Лечение |
Лечение больных инфекционным эндокардитом проводится в стационаре с соблюдением следующих основных принципов (М.А. Гуревич с соавт.):
1. Лечение должно быть этиотропным, т.е. направленным на конкретного возбудителя.
2. Для лечения следует применять только такие антибактериальные препараты, которые обладают бактерицидным действием.
3. Терапия инфекционного эндокардита должна быть непрерывной и продолжительной:
· при стрептококковой инфекции — не менее 4-х недель;
· при стафилококковой инфекции — не менее 6 недель;
· при грамотрицательной флоре — не менее 8 недель.
4. Лечение должно предусматривать создание высокой концентрации антибиотиков в сосудистом русле и вегетациях (предпочтительно внутривенное капельное введение антибиотиков).
5. Критериями прекращения лечения антибиотиками следует считать сочетание нескольких эффектов:
· полная нормализация температуры тела;
· нормализация лабораторных показателей (исчезновение лейкоцитоза, нейтрофилеза, анемии, отчетливая тенденция к снижению СОЭ);
· отрицательные результаты бактериального исследования крови;
· исчезновение клинических проявлений активности заболевания.
6. При нарастании признаков иммунопатологических реакций (гломерулонефрит, артриты, миокардит, васкулит) целесообразно применение:
· глюкокортикоидов (преднизолон не более 15–20 мг в сутки);
· антиагрегантов;
· гипериммунной плазмы;
· иммуноглобулина человека;
· плазмафереза и др.
7. При неэффективности консервативного лечения в течение 4-х недель и/или наличия других показаний (см. ниже) показано хирургическое лечение.
| 9.6.1. Антибактериальная терапия |
Несмотря на создание в последние годы большого количества высокоэффективных антибиотиков и химиопрепаратов, лечение инфекционного эндокардита остается чрезвычайно сложной задачей. Это обусловлено увеличивающейся частотой высевания высоковирулентных штаммов возбудителей (стафилококк, синегнойная палочка, грамотрицательные микроорганизмы группы НАСЕК), резистентных к антибактериальной терапии, снижением иммунологической резистентности большинства больных, увеличением числа больных пожилого и старческого возраста и другими причинами.
Кроме того, эффект антибактериальной терапии во многом определяется тем, насколько создаваемая в крови концентрация антибиотиков достаточна для того, чтобы воздействовать на возбудителя, локализующегося в глубине очага воспаления (вегетаций) и окруженного тромбин-фибриновым «защитным» сгустком.
К наиболее часто используемым для лечения инфекционного эндокардита антибиотикам с бактерицидным действием относятся:
· ингибиторы синтеза клеточной стенки бактерий — b-лактамы (пенициллины, цефалоспорины, карбопенемы);
· ингибиторы синтеза белка (аминогликозиды, рифампицин);
· ингибиторы синтеза нуклеиновых кислот (фторхинолоны).
В табл. 9.3 представлены ориентировочные схемы применения антибиотиков в зависимости от возбудителя и его чувствительности (В.П. Тюрин, А.А. Демина, В.П. Дробышева, М.А. Гуревич с соавт.).
Таблица 9.3
Схемы антибактериальной терапии больных инфекционным эндокардитом
| Антибиотики | Дозы и кратность введения | Длительность лечения |
| Пенициллинчувствительные стрептококки(S. viridans, S. bovis, S. pneumoniae, S. pyogenes и др.) | ||
| 1. Бензилпенициллин | 2–4 млн ЕД каждые 4 ч | 4 нед |
| 2. Цефтриаксон | 2 г внутривенно 1 раз в сутки | 4 нед |
| 3. Бензилпенициллин + + Гентамицин | 2–4 млн ЕД каждые 4 ч 1 мг/кг каждые 12 ч | 2 нед |
| 4. Цефтриаксон + +Гентамицин | 2 г внутривенно 1 раз в сутки 1 мг/кг каждые 12 ч | 2 нед |
| 5. Ванкомицин | 15 мг/кг каждые 12 ч | 4 нед |
| Относительно пенициллинустойчивые стрептококки | ||
| 1. Бензилпенициллин + + Гентамицин | 4 млн ЕД каждые 4 ч 1 мг/кг каждые 12 ч | 4–6 нед |
| 2. Цефтриаксон + +Гентамицин | 2 г внутривенно 1 раз в сутки 1 мг/кг каждые 12 ч | 4–6 нед |
| 3. Ванкомицин | 15 мг/кг каждые 12 ч | 4–6 нед |
| Энтерококки (E. fecalis, E. faecium и др.) и пенициллинустойчивые стрептококки | ||
| 1. Бензилпенициллин+ + Гентамицин | 2–4 млн ЕД каждые 4 ч 1 мг/кг каждые 8 ч | 4–6 нед |
| 2. Ампициллин + + Гентамицин | 2 г каждые 4 ч 1 мг/кг каждые 8 ч | 4–6 нед |
| 3. Ванкомицин + + Гентамицин | 15 мг/кг каждые 12 ч 1 мг/кг каждые 8 ч | 4–6 нед |
| Стафилококки (S. aureus, S. epidermidis и др.) | ||
| 1. Оксациллин + + Гентамицин | 2 г каждые 4 ч 1 мг/кг каждые 8 ч | 4–6 нед 10–14 дней |
| 2. Цефазолин + + Гентамицин | 2 г каждые 8 ч 1 мг/кг каждые 8 ч | 4–6 нед 10–14 дней |
| 3. Ванкомицин | 15 мг/кг каждые 12 ч | 4–6 нед |
| Грамотрицательные бактерии (E. coli, Proteus spp., Pseudomonas spp., Klebsiella spp., Enterobacter spp., Serratia spp.) | ||
| 1. Цефепим + + Гентамицин | 2 г каждые 12 ч 1 мг/кг каждые 8 ч | 4 нед 10–14 дней |
| 2. Цефепим + + Амикациин | 2 г каждые 12 ч 1 мг/кг каждые 8 ч | 4 нед. 10–14 дней |
| 3. Имипенем | 0,5 г каждые 6 ч | 4 нед |
| Грибы Candida spp., Aspergillus spp. | ||
| Амфотерицин В + + Флуконазол | 1 мг/кг 1 раз в сутки 400 мг 1 раз в сутки | 4–6 нед 4–6 нед |
| 9.6.2. Хирургическое лечение |
Сущность оперативного вмешательства при инфекционном эндокардите заключается в санации камер сердца и радикальной коррекции внутрисердечной гемодинамики (Ю.Л. Шевченко, 1995). С этой целью проводится механическое удаление инфицированных тканей с последующей рациональной антибиотикотерапией. При необходимости осуществляют протезирование пораженного клапана.
Лучшие результаты отмечаются у пациентов, оперированных в ранние сроки инфекционного эндокардита, при сохраненном миокардиальном резерве (М.А. Гуревич). Основными показаниями к хирургическому лечению являются:
1. Перфорация или отрыв створок клапана с развитием острой сердечной недостаточности.
2. Артериальные тромбоэмболии. Оперативное вмешательство показано после первого эпизода тромбоэмболии, поскольку риск повторных тромбоэмболий достаточно высок (около 54%).
3. Абсцессы миокарда, клапанного фиброзного кольца, поскольку дальнейшее консервативное лечение бесперспективно и неизбежен летальный исход.
4. Грибковый эндокардит, который в 100% случаев приводит к смертельному исходу, если не осуществляется своевременное оперативное вмешательство.
5. Инфекционный эндокардит клапанного протеза, обусловленный особо вирулентной флорой. Летальность при продолжении консервативной терапии достигает 35–55%.
6. Неэффективность этиотропной терапии в течение 3–4 недель (сохранение лихорадки, прогрессирующая деструкция клапана и т.д.).
Глава 10. Кардиомиопатии
| 10.1. Дилатационная кардиомиопатия |
 |
Дилатационная кардиомиопатия (ДКМП) — это первичное поражение миокарда, характеризующееся выраженной дилатацией полостей и нарушением систолической функции желудочков. Термин ДКМП применим только к тем случаям поражения сердца, при которых значительная дилатация полостей не является следствием нарушения коронарного кровообращения (ИБС), врожденных аномалий развития, клапанных пороков сердца, системной и легочной артериальной гипертензии и заболеваний перикарда.
Распространенность ДКМП неизвестна, поскольку до сих пор отсутствуют четкие критерии ее диагностики, что затрудняет проведение эпидемиологических исследований. Заболеваемость по данным разных авторов колеблется от 5 до 10 человек на 100 тысяч населения в год. ДКМП в 2–3 раза чаще встречается у мужчин, особенно в возрасте 30–50 лет.
| 10.1.1. Этиология |
 |
В большинстве случаев этиология ДКМП неизвестна (идиопатическая форма ДКМП). Примерно у 20% больных заболевание ассоциируется с перенесенным ранее инфекционным миокардитом. Считают, что воздействие на миофибриллы персистирующих в организме инфекционных агентов (в первую очередь энтеровирусов), в том числе включение вирусной РНК в генетический аппарат кардиомиоцитов или влияние “запущенного” вирусами аутоиммунного процесса, ведет к повреждению митохондрий и нарушению энергетического метаболизма клеток.
При использовании современных молекулярно-биологических технологий, в том числе полимеразной цепной реакции (ПЦР) у части больных удается выявить присутствие энтеровирусов, в частности вирусов Коксаки В, вируса гепатита С, герпеса, цитомегаловируса и др.
У части больных обнаруживаются также высокие титры кардиоспецифических аутоантител к миозину тяжелых цепей, актину, тропомиозину и митохондриальной мембране кардиомиоцитов, а также увеличение цитокинов в крови, что подчеркивает роль аутоиммунных нарушений. Вероятно, именно больные с исходным аутоиммунным дефицитом в большей степени подвержены повреждающему воздействию вирусов и развитию ДКМП.
В происхождении ДКМП большое значение имеет также генетическая предрасположенность к возникновению заболевания. Семейные ДКМП встречаются примерно в  случаев заболевания. Для них характерно, главным образом, аутосомно-доминантное наследование. У части больных ДКМП обнаруживаются также гаплотипы НLА В27 и НLА DR4.
случаев заболевания. Для них характерно, главным образом, аутосомно-доминантное наследование. У части больных ДКМП обнаруживаются также гаплотипы НLА В27 и НLА DR4.
Наконец, имеются данные о неблагоприятном воздействии алкоголя на миокард, что может приводить к нарушению синтеза сократительных белков кардиомиоцитов, повреждению митохондрий, нарушению энергетического метаболизма клеток и, в конечном счете, к критическому снижению сократимости сердечной мышцы и расширению полостей сердца, т.е. к формированию ДКМП.
Таким образом, в генезе ДКМП имеет значение взаимодействие нескольких факторов:
- генетической предрасположенности к возникновению заболевания;
- воздействия экзогенных факторов (вирусная инфекция, алкоголь) и
- аутоиммунных нарушений.
Если на начальных стадиях развития ДКМП в ряде случаев удается подтвердить вторичную природу поражения сердца (например, наличие вирусной инфекции), то на поздних стадиях клиническая картина уже мало зависит от возможных пусковых механизмов болезни (А.В. Сумароков). Поэтому на практике в подавляющем большинстве случаев конкретные причины остаются невыясненными и ДКМП трактуется как идиопатическая форма заболевания, удовлетворяющая традиционным критериям КМП по J. Goodwin.
 Запомните 1. Возникновение ДКМП связывают с взаимодействием нескольких патогенетических факторов: · генетической предрасположенности к возникновению заболевания; · воздействия экзогенных факторов (вирусная инфекция, злоупотребление алкоголем); · аутоиммунных нарушений. 2. Семейная (генетически детерминированная) ДКМП встречается примерно в Запомните 1. Возникновение ДКМП связывают с взаимодействием нескольких патогенетических факторов: · генетической предрасположенности к возникновению заболевания; · воздействия экзогенных факторов (вирусная инфекция, злоупотребление алкоголем); · аутоиммунных нарушений. 2. Семейная (генетически детерминированная) ДКМП встречается примерно в  случаев заболевания. Примерно у 20% больных ДКМП ассоциируется с вирусной инфекцией. Однако в большинстве случаев диагностируется идиопатическая форма ДКМП, когда взаимодействие перечисленных этиологических факторов становится настолько неопределенным, что выделить один из них в качестве основного не представляется возможным. случаев заболевания. Примерно у 20% больных ДКМП ассоциируется с вирусной инфекцией. Однако в большинстве случаев диагностируется идиопатическая форма ДКМП, когда взаимодействие перечисленных этиологических факторов становится настолько неопределенным, что выделить один из них в качестве основного не представляется возможным. | ||
| 10.1.2. Патогенез | ||
 | ||
В результате воздействия перечисленных выше и некоторых других (в том числе пока неизвестных) этиологических факторов происходит первичное повреждение кардиомиоцитов, снижение энергетического метаболизма клеток и уменьшение количества нормально функционирующих миофибрилл. Это ведет к прогрессирующему уменьшению сократительной способности миокарда и насосной функции сердца. В результате снижения инотропной функции миокарда происходит дилатация полостей сердца, которая, согласно механизму Старлинга, в течение некоторого времени поддерживает УО и ФВ на достаточном уровне. Одновременно развивающаяся тахикардия (активация САС) также способствует сохранению сердечного выброса (МО, СИ).
Однако такая компенсация весьма невыгодна с энергетической точки зрения, поскольку согласно закону Лапласа, для создания адекватного давления в полости желудочка дилатированная стенка ЛЖ должна развивать значительно большее внутримиокардиальное напряжение (рис. 10.2). Следствиями такого прогрессирующего увеличения постнагрузки являются:
- развитие компенсаторной гипертрофии миокарда желудочков, которая способствует некоторому снижению внутримиокардиального напряжения;
- увеличение потребности миокарда в кислороде, которое со временем ведет к развитию относительной коронарной недостаточности и ишемии миокарда;
- дальнейшее повреждение кардиомиоцитов и еще большее снижение сократимости;
- развитие диффузного и очагового кардиофиброза.
В результате происходит критическое падение насосной функции сердца, повышается КДД в желудочках и развивается выраженная миогенная дилатация полостей сердца.
Эти явления усугубляются развитием относительной недостаточности митрального и трехстворчатого клапанов, что способствует еще большей дилатации предсердий и желудочков. Иными словами, формируется и быстро прогрессирует хроническая сердечная недостаточность (ХСН) с преимущественным нарушением систолической функции желудочков, застоем крови в малом и большом кругах кровообращения, падением сердечного выброса и нарушением перфузии периферических органов и тканей.
Следует отметить, что значительное увеличение массы сердца за счет гипертрофии миокарда обычно не сопровождается заметным утолщением стенки желудочков, поскольку при ДКМП всегда преобладает выраженная дилатация камер сердца, которая как бы нивелирует увеличение мышечной массы (см. рис. 10.1).
Так же как и при других формах ХСН, важное значение в ремоделировании сердечной мышцы и развитии сердечной декомпенсации имеет чрезмерная активация нейрогормональных систем организма, в том числе САС, РААС, АДГ, тканевых РАС и эндотелиальных факторов. В результате активации этих систем происходит задержка Nа+ и воды в организме, что усугубляет застойные явления в малом и большом кругах кровообращения. Повышенное содержание катехоламинов, АII, цитокинов, фактора роста опухолей a, тромбоксана АIII приводит к еще большему повреждению миокарда, периферической вазоконстрикции, а также к значительным нарушениям свертывающей и фибринолитической систем крови.
 Запомните 1. В основе формирования ДКМП лежит первичное повреждение и гибель кардиомиоцитов, гемодинамическими следствиями которых являются: · прогрессирующее снижение сократительной способности; · выраженная дилатация полостей сердца; · развитие компенсаторной гипертрофии миокарда и увеличение массы сердца (без утолщения стенок желудочков); · развитие в тяжелых случаях заболевания относительной недостаточности митрального и трикуспидального клапанов; · застой крови в малом и большом кругах кровообращения; · относительная коронарная недостаточность и развитие ишемии сердечной мышцы; · развитие диффузного и очагового фиброза в миокарде; · периферическая вазоконстрикция и нарушение перфузии периферических органов и тканей. 2. Процесс ремоделирования сердца, а также описанные гемодинамические расстройства во многом обусловлены чрезмерной активацией нейрогормональных систем организма (САС, РААС, АДГ, эндотелиальных факторов, тканевых РАС и др.). 3. Прогрессирующее повреждение сердечной мышцы и нейрогормональная активация способствуют частому развитию у больных ДКМП: · нарушений сердечного ритма и проводимости; · внутрисердечных тромбозов и тромбоэмболических осложнений. Запомните 1. В основе формирования ДКМП лежит первичное повреждение и гибель кардиомиоцитов, гемодинамическими следствиями которых являются: · прогрессирующее снижение сократительной способности; · выраженная дилатация полостей сердца; · развитие компенсаторной гипертрофии миокарда и увеличение массы сердца (без утолщения стенок желудочков); · развитие в тяжелых случаях заболевания относительной недостаточности митрального и трикуспидального клапанов; · застой крови в малом и большом кругах кровообращения; · относительная коронарная недостаточность и развитие ишемии сердечной мышцы; · развитие диффузного и очагового фиброза в миокарде; · периферическая вазоконстрикция и нарушение перфузии периферических органов и тканей. 2. Процесс ремоделирования сердца, а также описанные гемодинамические расстройства во многом обусловлены чрезмерной активацией нейрогормональных систем организма (САС, РААС, АДГ, эндотелиальных факторов, тканевых РАС и др.). 3. Прогрессирующее повреждение сердечной мышцы и нейрогормональная активация способствуют частому развитию у больных ДКМП: · нарушений сердечного ритма и проводимости; · внутрисердечных тромбозов и тромбоэмболических осложнений. | ||
| 10.1.3. Клиническая картина | ||
 | ||
Клинически ДКМП проявляется тремя основными синдромами:
1. Систолической ХСН (левожелудочковой или бивентрикулярной) с признаками застоя крови в малом и большом кругах кровообращения.
2. Частым возникновением нарушений ритма и проводимости (желудочковые аритмии, фибрилляция предсердий, АВ-блокады и блокады ножек пучка Гиса).
3. Тромбоэмболическими осложнениями (ТЭЛА и эмболия в артерии большого круга кровообращения).
Таким образом, клинические проявления ДКМП, так же как результаты инструментального и лабораторного исследований, весьма неспецифичны, что затрудняет дифференциальный диагноз. Поэтому диагноз ДКМП ставится, как правило, путем исключения других заболеваний сердца с систолической дисфункцией желудочков (ИБС, АГ, миокардит, легочное сердце и др.).
Жалобы
Заболевание длительное время может протекать бессимптомно, несмотря на наличие объективных (эхокардиографических) признаков дилатации желудочков и нарушения их функции. Обычно первые клинические проявления болезни связаны с сердечной декомпенсацией, застоем крови в малом, а затем и в большом кругах кровообращения и снижением сердечного выброса. Больные жалуются на одышку при физической нагрузке и в покое, усиливающуюся в горизонтальном положении больного (ортопноэ). В далеко зашедших случаях возникают приступы удушья, чаще развивающегося по ночам (сердечная астма и отек легких). Очень характерна быстрая утомляемость, мышечная слабость, тяжесть в ногах при выполнении физических нагрузок. Признаки правожелудочковой недостаточности (отеки ног, тяжесть в правом подреберье, увеличение живота в объеме, диспептические явления) появляются позже.
 Запомните Наиболее важной клинической особенностью ДКМП является быстрое и неуклонное прогрессирование заболевания и признаков декомпенсации, а также рефрактерность к традиционному лечению ХСН. Запомните Наиболее важной клинической особенностью ДКМП является быстрое и неуклонное прогрессирование заболевания и признаков декомпенсации, а также рефрактерность к традиционному лечению ХСН. |
Примерно у  больных развиваются разнообразные нарушения ритма и проводимости, часть из которых вызывает у больных ДКМП неприятные ощущения (сердцебиения, перебои в работе сердца, приступы пароксизмальной тахикардии и мерцательной аритмии).
больных развиваются разнообразные нарушения ритма и проводимости, часть из которых вызывает у больных ДКМП неприятные ощущения (сердцебиения, перебои в работе сердца, приступы пароксизмальной тахикардии и мерцательной аритмии).
Наиболее тяжелыми осложнениями являются тромбозы и тромбоэмболии, развивающиеся у 20% больных ДКМП. Наиболее часто эти осложнения возникают у больных с фибрилляцией предсердий.
Иногда больные ДКМП отмечают боли в области сердца, которые в большинстве случаев отличаются от типичных приступов стенокардии. Боли часто имеют атипичную локализацию и, как правило, не связаны с физической нагрузкой.
Физикальное исследование
Физикальные данные, получаемые у больных ДКМП, также весьма неспецифичны. При общем осмотре выявляются известные признаки сердечной недостаточности (см. главу 2): акроцианоз, отеки ног, положение ортопноэ, увеличение живота в объеме, набухание шейных вен, иногда положительный венный пульс и др.
При исследовании легких в нижних отделах могут выслушиваться влажные мелкопузырчатые хрипы. Отмечается увеличение печени. В далеко зашедших случаях появляются признаки сердечной кахексии.
Осмотр, пальпация и перкуссия сердца
Верхушечный толчок, как правило, усилен, разлитой и смещен влево и вниз. Чаще всего можно выявить также усиленный и разлитой сердечный толчок и эпигастральную пульсацию, что указывает на наличие гипертрофии и дилатации ПЖ.
Обычно выявляется смещение влево левой границы относительной тупости сердца и вправо — правой границы. Дилатация ЛП сопровождается смещением вверх верхней границы сердца и сглаживанием “талии” сердца. Абсолютная тупость сердца обычно расширена за счет дилатации ПЖ (рис. 10.3).
I тон на верхушке ослаблен. При развитии легочной гипертензии определяется акцент и расщепление II тона. Нередко на верхушке выслушивается протодиастолический ритм галопа (за счет появления III патологического тона), что связано с выраженной объемной перегрузкой желудочков.
Характерны систолические шумы на верхушке и в точке выслушивания трехстворчатого клапана, которые указывают на формирование относительной недостаточности митрального и трикуспидального клапанов.
При возникновении фибрилляции предсердий или экстрасистолии тоны сердца аритмичные.
Специфических изменений артериального пульса нет. При значительном снижении сердечного выброса отмечается снижение систолического и пульсового АД, а в тяжелых случаях — уменьшение наполнения и напряжения пульса. При возникновении фибрилляции предсердий пульс аритмичный. Тахисистолическая форма мерцательной аритмии сопровождается дефицитом пульса.
Внезапная смерть при ДКМП может наступить в результате фибрилляции, асистолии или тромбоэмболии в легочный ствол или мозговые сосуды. К числу частых осложнений относятся также тромбоэмболии в легочную артерию и артерии большого круга кровообращения (мозговые, почечные, мезентериальные, артерии верхних и нижних конечностей и др.), сопровождающиеся характерной клинической картиной.
| 10.1.4. Лабораторные и инструментальные исследования |
 |
Электрокардиографическое исследование не позволяет выявить специфические особенности электрического поля сердца, характерные для ДКМП. На ЭКГ обычно определяются:
- признаки гипертрофии ЛЖ и ЛП, иногда в сочетании с гипертрофией ПЖ. Особенно характерна депрессия сегмента RS–Т в левых грудных отведениях (V5 и V6) и отведениях I и аVL;
- признаки блокады левой ножки пучка Гиса (частая находка);
- фибрилляция предсердий и/или другие нарушения ритма сердца;
- удлинение интервала Q–Т.
Следует подчеркнуть, что в ряде случаев на ЭКГ можно выявить признаки крупноочагового или трансмурального рубца миокарда в виде патологических зубцов Q и комплекса QS. Эти изменения отражают характерное для ДКМП развитие очагового фиброза миокарда ЛЖ.
Эхокардиография
ЭхоКГ является наиболее информативным неинвазивным методом исследования больных ДКМП. Во многих случаях эхокардиографическое исследование позволяет впервые выдвинуть диагностическую концепцию ДКМП, оценить степень нарушений систолической и диастолической функций желудочков, а также доказать отсутствие клапанных поражений, заболеваний перикарда и т.д.
Наиболее характерными эхокардиографическими признаками ДКМП являются значительная дилатация ЛЖ при нормальной или уменьшенной толщине его стенок (рис. 10.4) и снижение ФВ (ниже 30–20%). Часто отмечается расширение других камер сердца (ПЖ, ЛП). Как правило, развиваются тотальная гипокинезия стенок ЛЖ, а также значительное снижение скорости кровотока в восходящем отделе аорты и выносящем тракте ЛЖ и в ЛА (допплеровский режим). Нередко визуализируются внутрисердечные пристеночные тромбы.
Следует, однако, помнить, что в некоторых случаях при ДКМП можно обнаружить региональные нарушения сократимости ЛЖ и даже аневризму верхушки ЛЖ, что затрудняет дифференциальную диагностику этого заболевания с ИБС.
Кроме того, исследование в двухмерном и допплеровском режимах позволяет выявить характерные признаки относительной недостаточности митрального и трехстворчатого клапанов без деформации их створок.
Рентгенография
Рентгенологическое исследование позволяет выявить следующие изменения (рис. 10.5):
- признаки кардиомегалии;
- сглаженность контуров левых отделов сердца;
- шаровидную форму сердца за счет дилатации всех полостей (в тяжелых случаях);
- признаки венозной и артериальной легочной гипертензии и расширение корней легких.
Коронароангиография и вентрикулография
Эти инвазивные методы исследования используются обычно в тех случаях, когда возникает необходимость проведения дифференциальной диагностики ДКМП и ИБС, в частности, при решении вопроса о хирургическом лечении. У больных ДКМП отсутствует гемодинамически значимое сужение КА, определяются повышение показателей КДО и резкое снижение ФВ. Иногда можно выявить нарушения локальной сократимости миокарда ЛЖ.
Эндомиокардиальная биопсия
Эндомиокардиальная биопсия проводится в специализированных научных центрах. Метод позволяет оценить степень разрушения мышечных филаментов в биоптате, что имеет определенное прогностическое значение.
| 10.1.5. Лечение |
 |
Лечение больных ДКМП представляет собой весьма трудную задачу. Поскольку причину заболевания в подавляющем большинстве случаев установить не удается, патогенетическая терапия больных должна быть направлена на:
- коррекцию ХСН;
- лечение и профилактику аритмий;
- лечение и профилактику тромбоэмболических осложнений.
Больные ДКМП, как правило, рефрактерны к лечению традиционными инотропными средствами, которые не только не приводят к уменьшению клинических проявлений ХСН, но нередко способствуют возникновению сердечных аритмий. Современное лечение ХСН у больных ДКМП основано на следующих принципах:
1. Ограничение физических нагрузок, а также потребления поваренной соли, особенно при наличии отечного синдрома.
2. Ингибиторы АПФ являются средством первого выбора в лечении больных ДКМП. Назначение этих препаратов (при отсутствии противопоказаний) целесообразно на всех стадиях развития болезни, даже при отсутствии выраженных клинических проявлений ХСН. Ингибиторы АПФ способны предупреждать некроз кардиомиоцитов, развитие кардиофиброза; способствуют обратному развитию гипертрофии, снижают величину постнагрузки (внутримиокардиальное напряжение), уменьшают степень митральной регургитации, давление в ЛП и секрецию ПНУФ. Под влиянием длительного регулярного приема ингибиторов АПФ улучшается качество жизни больных ДКМП. Доказано, что применение ингибиторов АПФ достоверно увеличивает продолжительность жизни больных ДКМП.
Эффект ингибиторов АПФ при этом заболевании объясняется угнетением чрезмерной активации РААС, САС и других, в том числе тканевых, нейрогормональных систем, ответственных за неуклонное прогрессирование болезни.
Применять ингибиторы АПФ у больных ДКМП следует с осторожностью, главным образом, из-за возможности гипотензивной реакции и возникновения ортостатической гипотонии. Начальная доза препарата должна быть минимальной:
- эналаприл 2,5 мг 2 раза в сутки;
- рамиприл 1,25 мг 1 раз в сутки;
- периндоприл 2 мг 1 раз в сутки и т.д.
При хорошей переносимости дозы должны быть увеличены (соответственно, до 20–40 мг в сутки для эналаприла, 10 мг для рамиприла и 4 мг для периндоприла и т.д.).
3. b-адреноблокаторы целесообразно комбинировать с ингибиторами АПФ. Особенно показаны b-адреноблокаторы у больных со стойкой синусовой тахикардией, а также у пациентов с мерцательной аритмией (возможно в сочетании с сердечными гликозидами).
У больных ДКМП b-адреноблокаторы используются не только как средство профилактики и лечения нарушений сердечного ритма и контроля ЧСС, но и как препараты, оказывающие влияние на гиперактивированные САС и РААС. Их действие на эти системы сопровождается улучшением гемодинамики, уменьшением ишемии миокарда и повреждения кардиомиоцитов. Так же как и ингибиторы АПФ, b-адреноблокаторы улучшают качество жизни, прогноз и выживаемость больных ДКМП.
Используют любые b-адреноблокаторы (метопролол, бисопролол, атенолол, карведилол и др.). Лечение также начинают с малых доз препаратов, постепенно увеличивая их до максимально переносимых.
Следует помнить, что у части больных в первые 2–3 недели лечения b-адреноблокаторами могут наблюдаться уменьшение ФВ, УО и некоторое ухудшение состояния, что связано преимущественно с отрицательным инотропным действием этих препаратов. Однако у большинства таких больных со временем начинают преобладать положительные эффекты b-адреноблокаторов, обусловленные стабилизацией нейрогормональной регуляции кровообращения, восстановлением плотности b-адренорецепторов на клеточных мембранах кардиомиоцитов и уменьшением кардиотоксического действия катехоламинов. Постепенно возрастает ФВ и уменьшаются клинические проявления ХСН.
Применение b-адреноблокаторов при ДКМП требует осторожности, особенно у больных ХСН III–IV ФК по NYHА, хотя принципиально они не противопоказаны и при тяжелой декомпенсации.
4. Диуретики применяют при наличии застоя крови в легких или/и в большом круге кровообращения. Применяют тиазидовые, тиазидоподобные и петлевые мочегонные по обычной схеме (см. главу 2). При наличии выраженного отечного синдрома целесообразно перечисленные диуретики комбинировать с назначением антагонистов альдостерона (альдактон, верошпирон).
5. Нитраты. Для лечения больных с хронической левожелудочковой недостаточностью в качестве дополнительного лекарственного средства можно использовать нитраты — изосорбид-динатраты или изосорбид-5-мононитраты. Последние отличаются высокой биодоступностью и предсказуемостью действия (оликард, имдур, моночинкве-ретард и др.). Эти лекарственные средства способствуют депонированию крови в венозном русле большого круга кровообращения, уменьшают величину преднагрузки и признаки застоя крови в легких.
6. Сердечные гликозиды. Эти препараты несомненно показаны больным с постоянной формой мерцательной аритмии. В этих случаях положительные эффекты сердечных гликозидов (уменьшение ЧСС) объясняются, главным образом, не положительным инотропным действием этих препаратов, а их ваготропным действием, проявляющимся увеличением рефрактерных периодов АВ-узла и замедлением проведения электрического импульса по АВ-соединению. В результате тахисистолическую форму мерцательной аритмии удается перевести в нормосистолическую, что улучшает процессы диастолического наполнения ЛЖ, снижает давление в ЛП и венах малого круга кровообращения и способствует уменьшению одышки и других проявлений застоя крови в легких.
Дискуссионным остается вопрос о целесообразности применения сердечных гликозидов у больных ДКМП с синусовым ритмом и выраженной систолической дисфункцией ЛЖ (ФВ 25–30%). Монотерапия сердечными гликозидами, как правило, бывает неэффективной, поскольку в большистве случаев отсутствует морфологический субстрат для действия этих инотропных лекарственных средств, а именно: имеется значительное и распространенное повреждение кардиомиоцитов, уменьшение количества миофибрилл, нарушения клеточного метаболизма и выраженный кардиофиброз. С другой стороны, именно у больных ДКМП терапия дигоксином очень быстро приводит к развитию гликозидной интоксикации и возникновению жизнеопасных желудочковых аритмий и нарушений проводимости.
Риск побочных эффектов сердечных гликозидов еще больше увеличивается при наличии гипокалиемии, гипомагниемии, ХПН, а также у пожилых больных.
Таким образом, применение сердечных гликозидов у тяжелых больных с выраженной систолической дисфункцией ЛЖ и синусовым ритмом, хотя и возможно, но только в комбинации с ингибиторами АПФ, диуретиками и обязательно под контролем содержания электролитов и мониторинга ЭКГ.
Длительное применение негликозидных инотропных средств у больных ДКМП и ХСН не рекомендуется, так как достоверно увеличивает смертность этих больных. Кратковременное применение негликозидных инотропных лекарственных средств (леводопа, добутамин, милринон, амринон и др.) оправдано лишь в некоторых случаях, например, при подготовке больных к операции трансплантации сердца.
7. Применение антиагрегантов показано у всех больных ДКМП, поскольку в 30% случаев течение заболевания осложняется внутрисердечным тромбозом и развитием тромбоэмболий. С этой целью используется постоянный прием ацетилсалициловой кислоты в дозе 0,25–0,3 г в сутки или применение других антиагрегантов по схемам (трентал, дипиридамол, вазобрал, тонакан, Вессель Дуэ Ф и др.).
У больных с мерцательной аритмией показано назначение непрямых антикоагулянтов (варфарин) под строгим контролем показателей коагулограммы. Дозы препарата подбираются таким образом, чтобы величина МНО составляла 2,0–3,0 ед.
Многие специалисты считают показанием для назначения непрямых антикоагулянтов эхокардиографическое выявление у больных ДКМП внутрисердечных тромбов.
8. Трансплантация сердца. Эта операция является высокоэффективным способом лечения больных ДКМП, рефрактерных к медикаментозной терапии. Показаниями для операции трансплантации являются:
- быстрое прогрессирование сердечной недостаточности у больных ДКМП и отсутствие эффекта от проводимой терапии;
- возникновение жизнеопасных нарушений сердечного ритма;
- высокий риск тромбоэмболических осложнений.
10-летняя выживаемость больных ДКМП, перенесших операцию трансплантации сердца, достигает 70%. Понятно, что серьезной проблемой, ограничивающей распространение этого метода лечения, является, прежде всего, высокая стоимость оперативного вмешательства и некоторые организационные проблемы.
9. Двухкамерная электростимуляция сердца с помощью имплантируемого электрокардиостимулятора типа DDD (см. главу 3) в некоторых случаях позволяет добиться улучшения внутрисердечной гемодинамики, повышая систолическую функцию желудочков, и предупредить развитие некоторых осложнений заболевания.
| 10.1.6. Прогноз |
 |
В целом ДКМП характеризуется весьма неблагоприятным прогнозом. В течение 5 лет умирает до 50% больных, большинство из них — внезапно вследствие фибрилляции желудочков. К другим причинам летальных исходов относятся прогрессирующая сердечная недостаточность и тромбоэмболические осложнения.
 Запомните Предикторами неблагоприятного исхода ДКМП являются: · высокий функциональный класс ХСН (ФК IV по NYHА); · КДР больше 7,6 см (по данным одномерной ЭхоКГ); · ФВ меньше 35%; · возникновение блокады левой ножки пучка Гиса; · появление при суточном мониторировании ЭКГ высоких градаций желудочковых аритмий; · наличие постоянной формы мерцательной аритмии. Запомните Предикторами неблагоприятного исхода ДКМП являются: · высокий функциональный класс ХСН (ФК IV по NYHА); · КДР больше 7,6 см (по данным одномерной ЭхоКГ); · ФВ меньше 35%; · возникновение блокады левой ножки пучка Гиса; · появление при суточном мониторировании ЭКГ высоких градаций желудочковых аритмий; · наличие постоянной формы мерцательной аритмии. |
Следует отметить, что в последние годы контингент больных ДКМП существенно изменился, возросло число больных с доклиническими и субклиническими проявлениями болезни. Это связано с широким внедрением в клиническую практику эхокардиографического метода исследования, позволяющего осуществлять раннюю диагностику заболевания. По данным 1995 г., 5-летняя выживаемость такого контингента больных ДКМП составляет 76% (Gavazzi А. et al.). Операция трансплантации сердца существенно улучшает прогноз больных ДКМП: 10-летняя выживаемость достигает 70%.
| 10.2. Гипертрофическая кардиомиопатия |
 |
Гипертрофическая кардиомиопатия (ГКМП) — это первичное поражение миокарда, характеризующееся выраженной гипертрофией миокарда ЛЖ (реже ПЖ), нормальными или уменьшенными размерами полости ЛЖ, значительным нарушением диастолической функции желудочка и частым возникновением нарушений сердечного ритма.
Различают асимметричную и симметричную формы ГКМП. Чаще встречается асимметричная форма с преимущественной гипертрофией верхней, средней или нижней трети МЖП, толщина которой может быть в 1,5–3 раза больше толщины задней стенки ЛЖ и превышает 15 мм (рис. 10.6, б, в). Иногда толщина МЖП достигает 50–60 мм. В части случаев гипертрофия МЖП сочетается с увеличением мышечной массы передней или переднебоковой стенки ЛЖ, тогда как толщина задней стенки остается почти нормальной (рис. 10.6, г). Наконец, в некоторых случаях преобладает гипертрофия верхушки (апикальная форма ГКМП) с возможным переходом на нижнюю часть МЖП (рис. 10.6, д) или переднюю стенку ЛЖ.
Для симметричной формы ГКМП (рис. 10.6, е) характерно почти одинаковое утолщение передней, задней стенки ЛЖ и МЖП (концентрическая гипертрофия ЛЖ). Кроме того, в некоторых случаях, наряду с описанными изменениями ЛЖ, может гипертрофироваться миокард ПЖ.
Масса сердца резко увеличивается, достигая в отдельных случаях 800–1000 г. Полость ЛЖ обычно сужена. Особый интерес представляют случаи так называемой обструктивной формы ГКМП с асимметричным (или тотальным) поражением МЖП и обструкцией выходного тракта ЛЖ (рис. 10.6, б, в). В этих случаях говорят о наличии у больного идиопатического субаортального подклапанного (мышечного) стеноза, который приводит к наиболее выраженным изменениям внутрисердечной гемодинамики.
При гистологическом исследовании миокарда больных ГКМП обнаруживают несколько специфичных для этого заболевания признаков:
- дезориентированное хаотичное расположение кардиомиоцитов;
- фиброз миокарда в виде диффузного или очагового развития соединительной ткани в сердечной мышце, причем во многих случаях с образованием обширных и даже трансмуральных рубцовых полей;
- утолщение стенок мелких коронарных артерий за счет гипертрофии гладкомышечных клеток и увеличения содержания фиброзной ткани в сосудистой стенке.
Заболеваемость ГКМП составляет 2–5 человек на 100 тысяч населения или 2–3 случая на 1000 человек молодого возраста (20–35 лет). Преобладают необструктивные формы ГКМП, частота обнаружения которых примерно в 2–3 раза больше чем обструктивных. Мужчины заболевают чаще женщин. Первые клинические проявления болезни, как правило, возникают в молодом возрасте (20–35 лет).
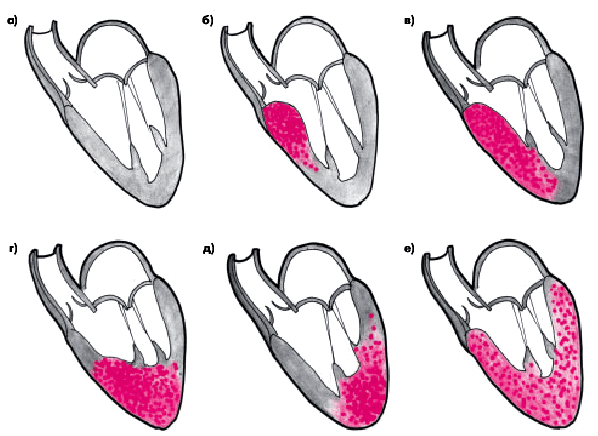 | ||
| Рис. 10.6. Схематическое изображение различных форм асимметричной (б–д) и симметричной (е) ГКМП: а — норма; б — преимущественная гипертрофия верхней части МЖП; в — гипертрофия верхней, средней и нижней частей МЖП; г — гипертрофия нижней части МЖП и верхушки ЛЖ; д — преимущественная гипертрофия верхушки с переходом на переднюю стенку ЛЖ; е — симметричная форма ГКМП. Красным цветом обозначены участки преимущественной гипертрофии миокарда | ||
| 10.2.1. Этиология | ||
 | ||
В настоящее время можно лишь условно говорить о ГКМП как о заболевании неизвестной этиологии. Благодаря достижениям современной генетики установлено, что в основе возникновения ГКМП лежат генетические факторы, а именно: передающиеся по наследству аномалии или спонтанные мутации в локусах нескольких генов, контролирующих структуру и функцию сократительных белков миокарда (b-миозина тяжелых цепей, тропонина Т, тропонина I, a-тропомиозина и миозинсвязывающего белка С). Гены располагаются в хромосомах 1, 2, 7, 11, 14 и 15. Генный дефект заключается в изменении последовательности аминокислот.
В большинстве случаев известные мутации генов приводят к синтезу аномальной тяжелой цепи b-миозина, реже — тропонина Т и a-тропомиозина. Аномальные белки как бы запускают процесс дезорганизации саркомера и приводят к нарушению его структуры и функции. Таким образом, примерно в половине случаев ГКМП носит семейный характер, и наследование аномалий генов происходит по аутосомно-доминантному типу. Примерно у половины близких родственников больных семейной ГКМП (родителей, родных братьев и сестер) выявляются эхокардиографические признаки гипертрофии МЖП. В других случаях не удается доказать семейный характер ГКМП и заболевание связывают со спонтанными мутациями названных генов, возможно, происходящими под действием неблагоприятных факторов среды (спорадические формы ГКМП). Дифференциация семейных и спорадических форм ГКМП затруднена.
Определенное значение в формировании заболевания придается действию нейрогормональных факторов: катехоламинов, инсулина, соматотропного гормона, нарушениям функции щитовидной и паращитовидной желез.
| 10.2.2. Патогенез изменений гемодинамики |
 |
Формирование выраженной асимметричной или симметричной гипертрофии ЛЖ, наряду с фиброзом миокарда и аномальным утолщением стенки мелких КА, приводит к выраженным изменениям внутрисердечной гемодинамики и коронарного кровообращения, которые объясняют практически все клинические проявления ГКМП.
1. Диастолическая дисфункция ЛЖ составляет основу гемодинамических нарушений при любых формах ГКМП (обструктивных и необструктивных). Диастолическая дисфункция вызвана увеличением ригидности гипертрофированной и склерозированной сердечной мышцы и нарушением процесса активного диастолического расслабления желудочков. Закономерными следствиями нарушения диастолического наполнения ЛЖ являются:
- возрастание конечно-диастолического давления в ЛЖ;
- повышение давления в ЛП и в венах малого круга кровообращения;
- расширение ЛП (при отсутствии дилатации ЛЖ);
- застой крови в малом круге кровообращения (диастолическая форма ХСН);
- уменьшение сердечного выброса (на более поздних стадиях развития заболевания) в результате затруднения диастолического наполнения желудочка и снижения КДО (уменьшения полости ЛЖ).
2. Систолическая функция желудочка у больных ГКМП, как правило, не нарушена или даже повышена: сила сокращения гипертрофированного ЛЖ и скорость изгнания крови в аорту обычно резко возрастают. Увеличивается и ФВ. Однако это вовсе не противоречит отмеченному выше снижению ударного объема и сердечного выброса, поскольку и высокие значения ФВ, и низкие значения УО объясняются резким уменьшением КДО и КСО. Вспомните:
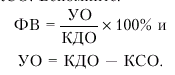 |
Поэтому при снижении КДО увеличивается ФВ и уменьшается УО.
3. Относительная коронарная недостаточность — один из характерных признаков ГКМП. Нарушения коронарного кровотока обусловлены:
- сужением мелких коронарных артерий за счет гипертрофии гладкомышечных клеток и развития соединительной ткани в стенке артерий (“болезнь мелких КА”);
- повышением КДД в ЛЖ, что приводит к падению градиента давления между аортой и полостью ЛЖ и, соответственно, уменьшению коронарного кровотока (см. главу 5);
- высоким внутримиокардиальным напряжением стенки сердца, что способствует сдавлению мелких субэндокардиальных коронарных сосудов;
- несоответствием значительно увеличенной мышечной массы ЛЖ и капиллярного русла сердца;
- повышением потребности миокарда в кислороде на фоне гиперконтрактильности сердечной мышцы.
4. Высокий риск желудочковых и наджелудочковых аритмий, а также риск внезапной смерти, обусловлен преимущественно выраженной электрической негомогенностью и нестабильностью миокарда желудочков и предсердий, которые у больных ГКМП возникают в результате очагового мозаичного расположения участков миокарда, обладающих различными электрофизиологическими свойствами (гипертрофия, очаговый фиброз, локальная ишемия). Определенное значение в возникновении аритмий имеет растяжение стенки дилатированного ЛП, а также токсическое воздействие катехоламинов на миокард желудочков.
Динамическая обструкция выносящего тракта ЛЖ при идиопатическом субаортальном мышечном стенозе развивается у больных с обструктивной формой ГКМП преимущественно при асимметричной гипертрофии МЖП (рис. 10.7). Как известно, выносящий тракт ЛЖ образован проксимальным отделом МЖП и передней створкой митрального клапана. При выраженной гипертрофии проксимальной части МЖП происходит сужение выносящего тракта. В результате во время изгнания крови в этом отделе резко возрастает линейная скорость кровотока и, согласно феномену Бернулли, значительно уменьшается боковое давление, которое оказывает поток крови на структуры, образующие выносящий тракт (рис. 10.7, а).
Иными словами, в области сужения выносящего тракта образуется зона низкого давления, которая оказывает присасывающее действие на переднюю створку митрального клапана (эффект насоса Вентури). Эта створка сближается с МЖП и в течение некоторого времени даже полностью смыкается с ней, создавая препятствие на пути изгнания крови в аорту. Такое препятствие может сохраняться в течение 60–80 мс, т.е. на протяжении  продолжительности всего периода изгнания (рис. 10.7, б).
продолжительности всего периода изгнания (рис. 10.7, б).
Патологическое движение передней створки митрального клапана навстречу МЖП усугубляется при аномальном расположении папиллярных мышц, неспособных удерживать створки митрального клапана в сомкнутом состоянии. В результате относительно продолжительного смыкания передней створки МЖП создается внутрижелудочковый градиент давления, величина которого характеризует степень обструкции выносящего тракта ЛЖ. В тяжелых случаях внутрижелудочковый градиент давления может достигать 80–100 мм рт. ст.
На величину градиента давления и степень обструкции выносящего тракта оказывают существенное влияние 3 основных фактора:
1. Сократимость миокарда ЛЖ.
2. Величина преднагрузки.
3. Величина постнагрузки.
Чем выше сократимость ЛЖ, тем больше линейная скорость кровотока в суженном участке выносящего тракта и выше присасывающий эффект Вентури. Поэтому все факторы, увеличивающие сократимость желудочка, усиливают обструкцию выносящего тракта (физическая нагрузка, тахикардия, психоэмоциональное напряжение, введение сердечных гликозидов и других инотропных средств, любая активация САС, гиперкатехоламинемия). Наоборот, брадикардия или введение лекарственных средств, обладающих отрицательным инотропным действием (b-адреноблокаторы, блокаторы медленных кальциевых каналов, дизопирамида и др.), способствуют уменьшению обструкции.
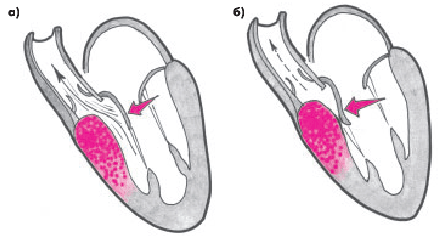 |
| Рис. 10.7. Возникновение динамической обструкции выносящего тракта ЛЖ при асимметричной обструктивной форме ГКМП: а — патологическое движение передней створки митрального клапана в сторону гипертрофированной верхней части МЖП (эффект Вентури); б — смыкание передней створки митрального клапана и МЖП и кратковременное прекращение изгнания крови в аорту. Объяснение в тексте |
Снижение преднагрузки приводит к дальнейшему уменьшению объема желудочка и, соответственно, размеров выносящего тракта и сопровождается усугублением его обструкции. Поэтому степень обструкции возрастает при внезапном переходе больного из горизонтального в вертикальное положение, при пробе Вальсальвы, приеме нитратов, при тахикардии. Наоборот, горизонтальное положение больного, любое увеличение ОЦК уменьшают степень обструкции.
Наконец, уменьшение постнагрузки (например, снижение АД при приеме артериальных вазодилататоров) приводит к увеличению обструкции выносящего тракта ЛЖ, тогда как ее увеличение (подъем АД, длительная статическая нагрузка, воздействие холода, введение мезатона, норадреналина и т.п.) способствует уменьшению внутрижелудочкового градиента давления и степени обструкции.
В табл. 10.2 суммированы сведения о факторах, влияющих на степень обструкции выносящего тракта ЛЖ у больных с обструктивной ГКМП.
Таблица 10.2
Факторы, влияющие на степень динамической обструкции выносящего тракта левого желудочка у больных с обструктивной ГКМП
| Факторы, увеличивающие степень обструкции | Факторы, уменьшающие степень обструкции |
| Изменения сократимости | |
| Физическая нагрузка | Введение b-адреноблокаторов |
| Психоэмоциональное напряжение | Введение блокаторов медленных кальциевых каналов (без резкого снижения АД) |
| Введение инотропных лекарственных средств | Введение дизопирамида |
| Прием симпатомиметиков | |
| Тахикардия | |
| Изменение преднагрузки | |
| Переход в вертикальное положение | Горизонтальное положение |
| Проба Вальсальвы | Увеличение ОЦК |
| Прием нитратов | |
| Гиповолемия | |
| Изменение постнагрузки | |
| Снижение ОПСС и АД | Подъем АД |
| Длительная статическая нагрузка | |
| Воздействие холода | |
| Введение мезатона, норадреналина |
 Запомните 1. В отличие от фиксированной обструкции при клапанном стенозе устья аорты, при ГКМП обструкция выносящего тракта ЛЖ носит динамический характер. 2. Степень обструкции увеличивается при: Запомните 1. В отличие от фиксированной обструкции при клапанном стенозе устья аорты, при ГКМП обструкция выносящего тракта ЛЖ носит динамический характер. 2. Степень обструкции увеличивается при:
|
Динамический характер обструкции выносящего тракта у больных ГКМП объясняет тот факт, что величина внутрижелудочкового градиента давления постоянно меняется у одного и того же больного, в том числе под действием перечисленных выше факторов.
Следует отметить, что внутрижелудочковая обструкция может развиваться не только при гипертрофии МЖП, но и при поражении других отделов ЛЖ. В редких случаях возможна также обструкция выносящего тракта ПЖ.
 Запомните При ГКМП наблюдаются следующие изменения внутрисердечной гемодинамики: 1. Выраженная гипертрофия ЛЖ и уменьшение размеров его полости. 2. Диастолическая дисфункция ЛЖ, ведущая к повышению давления в полости ЛП, венах малого круга кровообращения и застою крови в легких. 3. Дилатация ЛП, обусловленная повышением давления наполнения ЛЖ и среднего давления в ЛП. 4. Снижение сердечного выброса при относительно нормальной или возросшей контрактильности миокарда и систолической функции ЛЖ. 5. Относительная коронарная недостаточность. 6. Электрическая негомогенность и нестабильность миокарда желудочков и предсердий, что способствует возникновению аритмий и внезапной сердечной смерти. 7. Динамическая обструкция выносящего тракта ЛЖ (при обструктивной форме ГКМП). Запомните При ГКМП наблюдаются следующие изменения внутрисердечной гемодинамики: 1. Выраженная гипертрофия ЛЖ и уменьшение размеров его полости. 2. Диастолическая дисфункция ЛЖ, ведущая к повышению давления в полости ЛП, венах малого круга кровообращения и застою крови в легких. 3. Дилатация ЛП, обусловленная повышением давления наполнения ЛЖ и среднего давления в ЛП. 4. Снижение сердечного выброса при относительно нормальной или возросшей контрактильности миокарда и систолической функции ЛЖ. 5. Относительная коронарная недостаточность. 6. Электрическая негомогенность и нестабильность миокарда желудочков и предсердий, что способствует возникновению аритмий и внезапной сердечной смерти. 7. Динамическая обструкция выносящего тракта ЛЖ (при обструктивной форме ГКМП). | ||
| 10.2.3. Клиническая картина | ||
 | ||
Жалобы
Клинические проявления ГКМП определяются, в основном, описанными в предыдущем разделе нарушениями внутрисердечной гемодинамики. Длительное время заболевание может протекать бессимптомно, и объективные признаки ГКМП выявляются случайно. Первые клинические проявления чаще возникают в возрасте 25–40 лет.
Одышка вначале появляется при физической нагрузке, а затем и в покое. Она обусловлена повышением КДД ЛЖ, давления в ЛП и легочных венах и является следствием диастолической дисфункции ЛЖ. В некоторых случаях одышка может усиливаться при переходе больного в вертикальное положение, особенно у пациентов с обструктивной формой ГКМП, что связано с уменьшением венозного притока крови к сердцу и еще бульшим снижением наполнения ЛЖ.
Головокружения и обмороки объясняются преходящим нарушением перфузии головного мозга и обусловлены снижением сердечного выброса и наличием обструкции выносящего тракта ЛЖ (см. выше). Головокружения и обмороки возможны при быстром переходе больного из горизонтального в вертикальное положение, что снижает величину преднагрузки и также увеличивает обструкцию выносящего тракта. Обмороки провоцируются также физической нагрузкой, натуживанием и даже приемом пищи. В последнем случае нередко возникает вазодилатация, снижение постнагрузки и увеличение обструкции выносящего тракта.
Приступы стенокардии у больных ГКМП возникают в результате сужения мелких коронарных артерий и изменений внутрисердечной гемодинамики, описанных выше. Чаще стенокардия появляется у больных во время выполнения физической нагрузки или психоэмоционального напряжения. Интересно, что прием нитратов не купирует стенокардию, а, наоборот, может ухудшить состояние больного, поскольку усиливает степень обструкции и способствует усугублению диастолической дисфункции ЛЖ.
Сердцебиения и перебои вработе сердца могут быть связаны с возникновением фибрилляции предсердий, наджелудочковой и желудочковой экстрасистолии и пароксизмальной тахикардии.
Следует подчеркнуть, что иногда первым и последним проявлением ГКМП может быть внезапная сердечная смерть.
Физикальное исследование
У больных с необструктивной формой ГКМП объективные признаки заболевания могут отсутствовать в течение длительного времени, пока не разовьется выраженный застой крови в малом круге кровообращения. У больных с обструктивной ГКМП объективные признаки заболевания выявляются достаточно рано при обследовании сердечно-сосудистой системы.
Пальпация и перкуссия сердца
Верхушечный толчок в большинстве случаев усилен за счет гипертрофии ЛЖ. Нередко пальпируется так называемый двойной верхушечный толчок, что связано с усиленным сокращением ЛП, а затем ЛЖ (рис. 10.8, б). В более редких случаях можно пропальпировать тройной верхушечный толчок, обусловленный наличием усиленного сокращения ЛП (“волна a”), а затем — временным прекращением изгнания крови в аорту вследствие полного смыкания передней створки митрального клапана и МЖП, что создает своеобразный “провал” на основной систолической волне верхушечной кардиограммы (рис. 10.8, в).
Иногда вдоль левого края грудины определяется систолическое дрожание.
Границы сердца могут быть несколько смещены влево, “талия” сердца сглажена за счет дилатированного ЛП.
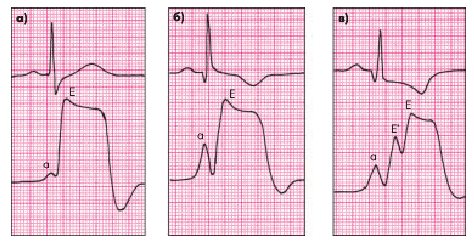 |
| Рис. 10.8. Изменение формы верхушечной кардиограммы при обструктивной асимметричной ГКМП: а — норма; б — «двойной верхушечный толчок»; в — «тройной верхушечный толчок». «а» — предсердная волна; Е — основная систолическая волна верхушечной кардиограммы |
Аускультация сердца позволяет выявить наиболее специфичные признаки обструктивной формы ГКМП. Основные тоны сердца часто не изменены, возможно расщепление I тона в связи с несинхронным сокращением левого и правого желудочков.
Акцент II тона на легочной артерии появляется при значительном повышении давления в легочной артерии. Часто на верхушке выслушивается пресистолический ритм галопа за счет появления патологического IV тона сердца (усиление сокращения ЛП и высокое КДД в ЛЖ). У части больных отмечается парадоксальное расщепление II тона на аорте.
Систолический шум является основным аускультативным признаком обструктивной ГКМП. Он отражает возникновение динамического градиента давления между ЛЖ и аортой. Шум громкий, грубый, выслушивается обычно вдоль левого края грудины и не проводится на сосуды шеи (рис. 10.9). Харак
 2015-10-13
2015-10-13 2761
2761