На практике для описания процессов, происходящих в газах, используют макроскопические параметры – давление р, объем V итемпературу Т. Эти величины характеризуют состояние газа и легко измеряются различными приборами. Между ними устанавливаются соотношения в виде газовых законов, которые мы рассмотрим позже.
Понятие температуры тесно связано с понятием теплового равновесия. Тепловое равновесие – это такое состояние системы тел, находящихся в тепловом контакте, при котором не происходит теплопередачи от одного тела к другому, и все макроскопические параметры тел остаются неизменными. Температура – это физический параметр, одинаковый для всех тел, находящихся в тепловом равновесии.
Для измерения температуры используются физические приборы – термометры, в которых о величине температуры судят по изменению какого-либо физического параметра. В различных конструкциях термометров используются разнообразные физические свойства вещества (например, изменение линейных размеров твердых тел или изменение электрического сопротивления проводников при нагревании). Термометры должны быть откалиброваны. Для этого их приводят в тепловой контакт с телами, температуры которых считаются известными. По температурной шкале Цельсия точке плавления льда приписывается температура 0 °С, а точке кипения воды – 100 °С.
Английский физик У. Кельвин в 1848 г. предложил использовать точку нулевого давления газа для построения новой температурной шкалы – шкалы Кельвина. В этой шкале единица измерения температуры такая же, как и в шкале Цельсия, но нулевая точка сдвинута:
T = t + 273,15. (7.10)
В системе СИ принято единицу измерения температуры по шкале Кельвина называть кельвином и обозначать буквой K.
Температурная шкала Кельвина называется абсолютной шкалой температур. Она оказывается наиболее удобной при построении физических теорий.
Экспериментально доказано, что давление разреженного газа в сосуде постоянного объема V изменяется прямо пропорционально его абсолютной температуре: p ~ T. С другой стороны, опыт показывает, что при неизменных объеме V и температуре T давление газа изменяется прямо пропорционально концентрации n молекул газа, т.е. числу молекул газа в единице объема. Для любого разреженного газа справедливо соотношение:
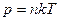 , (7.11)
, (7.11)
где k – некоторая универсальная для всех газов постоянная величина. Ее называют постоянной Больцмана, в честь австрийского физика Л. Больцмана, одного из создателей молекулярно-кинетической теории. Постоянная Больцмана – одна из фундаментальных физических констант. Ее численное значение в СИ равно:
k = 1,38·10–23 Дж/К. (7.12)
Сравнивая соотношения (7.11) и (7.9), можно получить:
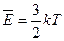 . (7.13)
. (7.13)
Средняя кинетическая энергия хаотического движения молекул газа прямо пропорциональна абсолютной температуре. Таким образом, температура есть мера средней кинетической энергии поступательного движения молекул.
Следует обратить внимание на то, что средняя кинетическая энергия поступательного движения молекулы не зависит от ее массы. Броуновская частица, взвешенная в жидкости или газе, обладает такой же средней кинетической энергией, как и отдельная молекула, масса которой на много порядков меньше массы броуновской частицы. Этот вывод распространяется и на случай, когда в сосуде находится смесь химически невзаимодействующих газов, молекулы которых имеют разные массы. В состоянии равновесия молекулы разных газов будут иметь одинаковые средние кинетические энергии теплового движения, определяемые только температурой смеси. Давление смеси газов на стенки сосуда будет складываться из парциальных давлений каждого газа:
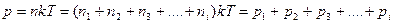 . (7.14)
. (7.14)
В этом соотношении n1, n2, n3, … – концентрации молекул различных газов в смеси. Это соотношение выражает на языке молекулярно-кинетической теории экспериментально установленный в начале XIX столетия закон Дальтона: давление в смеси химически невзаимодействующих газов равно сумме их парциальных давлений.
 2014-02-02
2014-02-02 17543
17543
