1.Каковы основные положения термодинамического и моле кул ярно-кинетического (статистического) методов изучения макроскопических систем? Назовите основные параметры термодинамической системы. Дайте определение единицы термодинамической температуры.
2.Запишите уравнение состояния идеального газа (уравнение Менделеева-Клапейрона). Каковы физический смысл, размерность и численное значение универсальной газовой постоянной R? Сформулируйте газовые законы.
3.Дайте определение единицы вещества 1 моль. Сколько молекул содержится в моле любого вещества? Как можно рассчитать линейные размеры одной молекулы?
4.На чем основан вывод уравнения молекулярно-кинетической теории идеальных газов для давления? Сравните это уравнение с уравнением Менделеева—Клапейрона.
5.Получите соотношения р = nkT и <W> = 3/2 kT. Каковы физический смысл, численное значение и единицы измерения постоянной Больцмана k?
6.Каково содержание одного из основных положений статистической физики о равнораспределении энергии по степеням свободы? Считая, что средняя энергия молекулы идеального газа <W> = ikT/2, где i – сумма поступательных, вращательных и удвоенного числа колебательных степеней свободы молекулы, получите выражение для внутренней энергии произвольной массы идеального газа: 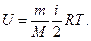
7.При каких условиях выполняется закон распределения молекул газа по скоростям? Напишите аналитическое выражение этого закона иизобразите его графически.
8.Получите соотношения для следующих скоростей молекул: а) наиболее вероятной vв, б) средней арифметической <v>; в) средней квадратичной 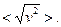
9.Проанализируйте выражение зависимости атмосферного давления от высоты (барометрическая формула): 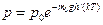 , где m0gh – потенциальная энергия молекулы газа на высоте h, считая температуру постоянной.
, где m0gh – потенциальная энергия молекулы газа на высоте h, считая температуру постоянной.
10.Исходя из барометрической формулы, получите выражение 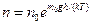 Сформулируйте закон распределения Больцмана.
Сформулируйте закон распределения Больцмана.
11.Что называется эффективным диаметром молекулы d? Объясните выражения: а) среднее число соударений молекул газа в единице объема за единицу времени: 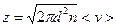 ; б) средняя длина пробега молекулы газа: λ = 1/(2πd2n), где n – концентрация молекулы.
; б) средняя длина пробега молекулы газа: λ = 1/(2πd2n), где n – концентрация молекулы.
12.Каковы закономерности явлений переноса в газах? Получите: а) выражение для динамической вязкости 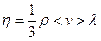 (ρ – плотность газа); б) выражение для теплопроводности
(ρ – плотность газа); б) выражение для теплопроводности 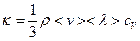 (CV – удельная теплоемкость газа при постоянном объеме); выражение для коэффициента диффузии
(CV – удельная теплоемкость газа при постоянном объеме); выражение для коэффициента диффузии 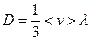 .
.
ЗАДАЧИ
8.1.Плотность некоторого газа при температуре t = 14° С и давлении р = 4·105 Па равна 0,68 кг/м3. Определить молярную массу М этого газа.
8.2.В баллоне объемом V = 20 л находится газ под массой m = 6 г при температуре Т = 300 К. Найти плотность ρ и давление р водорода.
8.3.Определить наименьший объем Vmin баллона, вмещающего m = 6кг кислорода, если его стенки при температуре t = 27° С выдерживают давление р = 15 МПа.
8.4.В сосуде А объемом V1 = 2 л находится газ под давлением р1 = 3·105 Па, а в сосуде В объемом V2 = 4 л находится тот же газ под давлением Р2 = 1·105 Па. Температура обоих сосудов одинакова и постоянна. Под каким давлением р будет находиться газ после соединения сосудов А и В трубкой. Объемом соединительной трубки пренебречь.
8.5.В баллоне находится m1 = 8 г водорода и m2 = 12 г азота при температуре t = 17° С и под давлением р = 1,8·105 Па. Определить молярную массу М смеси и объем V баллона.
8.6.Определить удельный объем V0 смеси углекислого газа массой m1 = 10 г и азота массой m2 = 15 г при давлении р = 0,15 МПа и температуре Т = 300 К.
8.7.Определить концентрацию n молекул кислорода и его плотность ρ при давлении р = 5 нПа и температуре t = 20 °С.
8.8.Определить плотность ρ водорода и концентрацию n его молекул при температуре t = 17°С и давлении р = 0,29 МПа.
8.9.Молекулярный пучок падает перпендикулярно на стенку, от которой молекулы отражаются по закону абсолютно упругого удара. Концентрация молекул в пучке n, масса молекулы m0, скорость каждой молекулы v. Найти давление р, испытываемое стенкой, если: а) стенка неподвижна; б) стенка движется в направлении своей нормали со скоростью u.
8.10.Молекулярный пучок падает на стенку под углом α к ее нормали. Концентрация молекул в пучке n, масса каждой молекулы m0, скорость молекулы v. Молекулы отражаются от стенки по закону абсолютно упругого удара. Найти давление р, испытываемое стенкой, если: а) стенка неподвижна; б) стенка движется в направлении своей нормали со скоростью u.
8.11.В сосуде находится m1 = 3,2·10-12 кг кислорода m2 = 2,8·10-10 кг азота. Температура смеси Т = 300 К. Давление в сосуде р = 0,15 Па. Определить объем V сосуда и концентрацию n молекул смеси в нем.
8.12.Найти давление р смеси газа в сосуде объемом V = 5 л,если в нем находится N1 = 2·1015 молекул кислорода, N2 = 8·1015 молекул азота и m = 1,0 нкг аргона. Температура смеси t = 17° С.
8.13.В сосуде находится m1 = 2 г водорода и т2 = 12 г азота при температуре t = 17 °С и давлении р = 0,18 МПа. Найти концентрацию п1 молекул водорода в смеси.
8.14.Определить концентрации n1 и n2 неона и аргона, если при давлении р = 0,16 МПа и температуре t = 47 °С плотность их смеси ρ = 2,0 кг/м3.
8.15.В сосуде объемом V = 1 л находится m = 2 г парообразного йода при температуре Т = 1200 К. Давление в сосуде р = 90 кПа. Найти степень диссоциации α молекул йода.
8.16.Вычислить среднюю квадратичной скорость 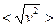 молекул воздуха при температуре t = 17 °С. Воздух считать идеальным газом.
молекул воздуха при температуре t = 17 °С. Воздух считать идеальным газом.
8.17.Плотность некоторого газа ρ = 3·10-2 кг/м3. Найти давление р газа, которое он оказывает на стенки сосуда, если средняя квадратичная скорость молекул газа равна 500 м/с.
8.18.Средняя квадратичная скорость молекул некоторого газа равна 450 м/с. Давление газа р = 25 кПа. Найти удельный объем V газа при этих условиях.
8.19.Найти отношение η средних квадратичных скоростей молекул водорода и кислорода при одинаковых температурах.
8.20.Вычислить среднюю квадратичную скорость 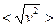 и среднюю энергию атома гелия <W> при температуре Т = 300 К.
и среднюю энергию атома гелия <W> при температуре Т = 300 К.
8.21.Вычислить среднюю кинетическую энергию поступательного движения <W>пост и полную среднюю кинетическую энергию <W> молекулы азота при температуре Т = 300 К. Молекулу азота считать жесткой.
8.22.Вычислить энергию теплового движения U молекул двухатомного газа, занимающего объем V = 2,5 л при давлении р = 20 Па. Молекулы газа считать жесткими.
8.23.При какой температуре Т средняя кинетическая энергия теплового движения атомов гелия окажется достаточной для того, чтобы атомы гелия навсегда покинули атмосферу Земли?
8.24.Вычислить среднюю энергию поступательного <W>пост вращательного <Wвр> и колебательного <Wкол> движений двухатомной молекулы газа при температуре T = 3·103 К.
8.25.Определить отношение η средней квадратичной скорости молекулы газа к скорости распространения звука в нем при одной и той же температуре. Газ взять двухатомный, молекулы газа считать жесткими.
8.26.Найти относительное число молекул Δn/n, скорости которых отличаются от наиболее вероятной не более чем на 10 м/с, при температурах газа: а) Т1 = 300 К; б) Т2 = 600 К.
8.27.Найти относительное число молекул Δn/n гелия, скорости которых лежат в интервале от v1 = 990 м/с до v2 = 1010 м/с при температурах: а) Т1 = 300 К; б) Т2 = 600 К.
8.28.Найти относительное число молекул Δn/n гелия, скорости которых лежат в интервале от v1 = 1990 м/с до v2 = 2010 м/с при температурах: а) Т1 = 300 К; б) Т2 = 600 К.
8.29.Найти отношение η числа молекул гелия, движущихся со скоростями в интервале от v1 = 2000 м/с до v2 = 2010 м/с, к числу молекул, скорости которых лежат в интервале от v3 = 1000 м/с до v4 = 1010 м/с. Температура гелия Т = 600 К.
8.30.Какая часть Δn/n молекул азота при температуре t = 230 С обладает скоростями в интервале: а) от v1 = 290 м/с до v2 = 310 м/с; б) от v3 = 690 м/с до v4 = 710 м/с.
8.31.При какой температуре Т наиболее вероятная скорость молекул азота меньше их средней квадратичной скорости на 50 м/с?
8.32.Найти относительное число молекул Δn/n газа, скорости которых отличаются не более чем на одну сотую от: а) наиболее вероятной скорости; б) средней арифметической скорости; в) средней квадратичной скорости.
8.33.На какой высоте h давление воздуха составляет 80 % давления на уровне моря? Температуру считать постоянной по высоте и равной t = 7° С.
8.34.Давление воздуха у поверхности Земли р = 100 кПа. Считая температуру воздуха постоянной и равной Т = 270 К, определить концентрацию молекул n воздуха: а) у поверхности Земли; б) на высоте h = 8 км.
8.35.На какой высоте h концентрация молекул водорода составляет 50 % концентрации на уровне моря? Температуру считать постоянной и равной 273 К. Ускорение свободного падения постоянно и равно 9,8 м/с2.
8.36.В кабине вертолета барометр показывает давление p1 = 86 кПа. На какой высоте h летит вертолет, если у поверхности Земли давление равно р2 = 0,10 МПа. Считать, что температура воздуха постоянна и равна 280 К.
8.37.На какой высоте h содержание водорода в воздухе по сравнению с содержанием углекислого газа увеличится вдвое? Среднюю по высоте температуру воздуха считать Т = 300 К.
8.38.Определить число молекул в единице объема n воздуха на высоте h = 2 км над уровнем моря. Температуру считать постоянной и равной 10 °С. Давление на уровне моря р0 = 101 кПа.
8.39.Для вычисления числа Авогадро NA. Перрен определял с помощью микроскопа распределение по высоте шарообразных частиц гуммигута, взвешенных в воде. Он нашел, что отношение числа частиц в слоях, отстоящих друг от друга на расстояние l = 38 мкм, равно α = 2,08. Плотность гуммигута ρ = 1,2·103 кг/м3, радиусы его частиц R = 0,212 мкм. Температура воды t = 18 °С. Используя эти данные, найти число Авогадро.
8.40.Найти, на какой высоте hc находится центр тяжести вертикального цилиндрического столба воздуха. Температуру Т, молярную массу М и ускорение свободного падения g считать известными и не зависящими от h.
8.41.Найти среднюю длину свободного пробега λср молекул воздуха при температуре Т = 300 К и давлении р = 0,15 МПа. Эффективный диаметр молекулы воздуха dэф = 0,30 нм.
8.42.Найти среднюю продолжительность τ свободного пробега молекул кислорода при температуре Т = 300 К и давлении р = 150 Па. Эффективный диаметр молекулы кислорода dэф = 0,27 нм.
8.43.Определить концентрацию n молекул водорода, при которой среднее расстояние между молекулами в сто раз меньше длины свободного пробега молекул. Эффективный диаметр молекулы водорода dэф = 0,23 нм.
8.44.Средняя длина свободного пробега электрона в газе приблизительно в 5,7 раз больше, чем средняя длина свободного пробега молекул газа. Найти среднюю длину пробега <λЭЛ> электронов в разрядной трубке, содержащей водород при температуре t = 127° С и давлении р =1,2 Па. Эффективный диаметр молекулы водорода dэф = 0,23 нм.
8.45.Расстояние между стенками дьюаровского сосуда l = 10 мм. Оценить, при каком давлении р теплопроводность воздуха, находящегося между стенками сосуда, начнет уменьшаться при его откачке? Температура воздуха t = 20 °С. Эффективный диаметр молекулы воздуха dэф = 0,30 нм.
8.46.Динамическая вязкость аргона при нормальных условиях η = 22 мкПа·с. Вычислить длину свободного пробега λ молекулы аргона и коэффициент диффузии D аргона при нормальных условиях.
8.47.Между двумя пластинами, расположенными на расстоянии l = 2 мм друг от друга, находится воздух при нормальных условиях. Между пластинами поддерживается разность температур ΔT = 20 К. Площадь каждой пластины S = 150 см2. Найти количество теплоты Q, передаваемое от одной пластины к другой за τ = 0,5 ч. Эффективный диаметр молекулы воздуха d = 0,30 нм.
8.48.Кислород и углекислый газ находятся при одинаковых температуре и давлении. Эффективные диаметры молекул этих газов соответственно равны 0,35 нм и 0,40 нм. Найти для этих газов отношения: а) коэффициентов диффузии D1/D2; б) коэффициентов внутреннего трения η1/η2.
8.49.Относительное число молекул газа, длина свободного пробега которых лежит в пределах от l до l + dl, определяется по формуле Δn/n = Ае-1/λdl, где А – постоянный коэффициент (нормирующий множитель). Найти относительное число Δn/n молекул газа, длина свободного пробега которых больше, чем 5λ.
8.50.Два однородных диска каждый радиусом R = 0,3 м расположены друг над другом так, что их оси совпадают. Верхний диск неподвижен, а нижний вращается с угловой скоростью ω = 126 рад/с. Расстояние между плоскостями дисков l = 5 мм. Динамическая вязкость воздуха η = 17 мкПа·с. Найти момент сил трения М, действующий на верхний диск. Краевыми эффектами пренебречь.
Задание 9. ОСНОВЫ ТЕРМОДИНАМИКИ
 2015-02-14
2015-02-14 2481
2481








