Теплоемкость определяет «температурную инерционность» системы.
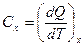 .
.
X - условия теплообмена. Удельные теплоемкости
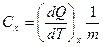 - массовая удельная теплоемкость
- массовая удельная теплоемкость
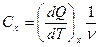 - мольная удельная теплоемкость.[12]
- мольная удельная теплоемкость.[12]
 В справочной литературе обычно приводятся значения теплоемкостей при постоянном объеме CV и постоянном давлении CP. Величина теплоемкости может быть любой (положительной, отрицательной, нулевой, бесконечной). Величина определяется условиями теплообмена.
В справочной литературе обычно приводятся значения теплоемкостей при постоянном объеме CV и постоянном давлении CP. Величина теплоемкости может быть любой (положительной, отрицательной, нулевой, бесконечной). Величина определяется условиями теплообмена.
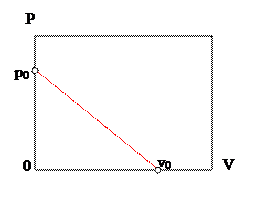
d Задача. Определите величину теплоемкости моля идеального одноатомного газа на прямой линии диаграммы P – V.
Уравнение прямой линии в координатах P – V
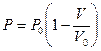 .
.
Используемые уравнения (термическое и калорическое уравнения газа, первый закон термодинамики)
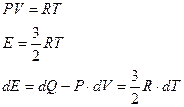 .
.
Из последнего уравнения
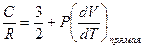 .
.
Производную на прямой линии p0 – v0 определяем, используя уравнение прямой и термическое уравнение.
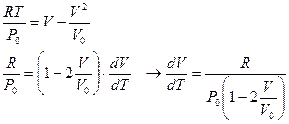 .
.
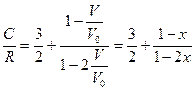 .
. 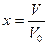 .
.
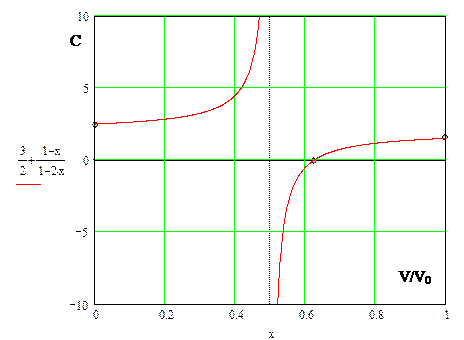 |
График полученного результата показывает диапазон изменения теплоемкости вдоль прямой. В середине линии теплоемкость терпит разрыв. Граничные теплоемкости соответственно равны 5/2 и 3/2. В точке 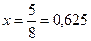 теплоемкость равна 0.
теплоемкость равна 0.
d Задача. Получить уравнение политропического процесса. Политропическим процессом называется процесс при постоянной теплоемкости.
Будем использовать
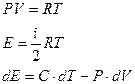 .
.
Используя первые два уравнения, преобразуем дифференциальное уравнение первого закона термодинамики
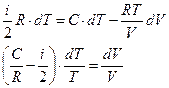 .
.
Обозначим 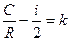 . Дифференциальное уравнение политропы переписывается
. Дифференциальное уравнение политропы переписывается
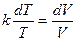 . Интегрирование приводит к уравнению
. Интегрирование приводит к уравнению
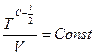 . (10)
. (10)
Здесь и далее теплоемкость выражена в единицах R.
- Изохорный процесс. Очевидно, что в этом случае
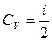 .
. - Изобарный процесс. В формуле (10) перейдем к давлению
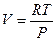
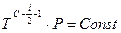 .
.
Очевидно, что давление будет постоянным при условии 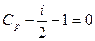 . Отсюда
. Отсюда
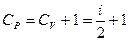 .
.
- Адиабатный процесс. C = 0. Подстановка в (10) определяет уравнение адиабаты
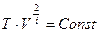 .
.
- Изотермический процесс. Преобразуем формулу (10) к виду
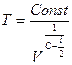 .
.
Температура будет константой при условии 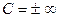 .
.
- Процесс с линейной зависимостью давления от объема. В формуле (10) избавляемся от температуры
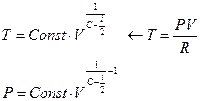 .
.
Для линейной зависимости давления от объема необходимо выполнения условия
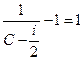 . Отсюда получаем
. Отсюда получаем 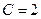 .
.
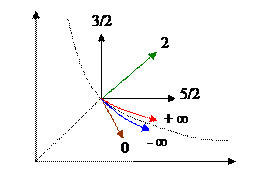
Рисунок иллюстрирует спектр политропных процессов с различными теплоемкостями. Процессы идущие вблизи изотермы имеют бесконечные теплоемкости.
III. 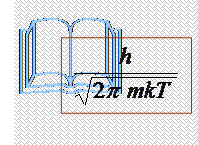 Статистическая термодинамика.
Статистическая термодинамика.
 2014-01-25
2014-01-25 1113
1113
