Аналогично получают уравнение изохоры:
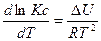
Эти уравнения были выведены Вант-Гоффом и известны как уравнения изохоры и изобары Вант-Гоффа
В этих уравнениях левую часть уравнения величину 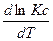 и
и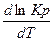 называют температурными коэффициентами логарифма константы химического равновесия, т.е. это есть изменение ln Кр и ln Кс при изменении температуры на единицу.
называют температурными коэффициентами логарифма константы химического равновесия, т.е. это есть изменение ln Кр и ln Кс при изменении температуры на единицу.
В правой части уравнения стоит тепловой эффект. Следовательно, знак теплового эффекта может предсказать, как будет изменяться константа равновесия при изменении температуры.
Если ΔН =0, то и 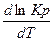 =0, т.е. Кр не зависит от температуры.
=0, т.е. Кр не зависит от температуры.
Если ΔН<0, то Кр уменьшается,
Если ΔН>0, то Кр растет.
Это так называемая качественная оценка зависимости Кр от температуры.
Для количественной оценки необходимо проинтегрировать уравнение изобары от температуры Т1 до температуры Т2, считая тепловой эффект постоянным:
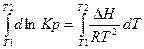
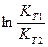 =
=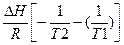 или, если интегрировать в неопределенных пределах, то имеем:
или, если интегрировать в неопределенных пределах, то имеем:

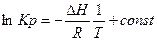
на графике это будет прямая y=ах+b у которой a= -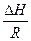 , x=1|T.
, x=1|T.
Принцип Ле-Шателье-Брауна
Под влиянием внешних воздействий или при изменении условий существования системы состояние равновесия изменяется и может наступить новое состояние равновесия, при этом сдвиг его влево или вправо устанавливается принципом Ле-Шателье_-Брауна:
Если на систему, находящуюся в равновесии, оказать воздействие извне, то возникает такое смещение равновесия. которое ослабляет это воздействие.
Поясним на примере.
N2 + 3H2 = 2 NH3
Если давление увеличится, то равновесие сдвинется слева направо, так как эта реакция протекает с уменьшением объема.
А уменьшение объема вызовет снижение давления (произойдет уменьшение количества молекул в реагирующей смеси), т. е. идет ослабление внешнего воздействия.
В соответствии с принципом Ле-Шателье увеличение концентрации реагирующих веществ сдвигает равновесие вправо, а увеличение концентрации продуктов реакции сдвигает равновесие сдвигает влево.
 2014-02-09
2014-02-09 1510
1510
