1. Если окислитель и восстановитель – разные вещества, то такие реакции относят к межмолекулярным. Примерами таких процессов служат все рассмотренные ранее реакции.
2. При термическом разложении сложных соединений, в состав которых входят окислитель и восстановитель в виде атомов разных элементов, происходят окислительно-восстановительные реакции, называемые внутримолекулярными: ( H4)2
H4)2  2O7
2O7 
 2 +
2 +  2O3 + 4H2O
2O3 + 4H2O
3. Реакции диспропорционирования могут происходить, если соединения, содержащие элементы в промежуточных степенях окисления, попадают в условия, где они оказываются неустойчивыми (например, при повышенной температуре). Степень окисления этого элемента и повышается и понижается: 2Н2  2
2 
 2 + 2Н2
2 + 2Н2 
4. Реакции контрпропорционирования – это процессы взаимодействия окислителя и восстановителя, в состав которых входит один и тот же элемент в разных степенях окисления. В результате продуктом окисления и продуктом восстановления является вещество с промежуточной степенью окисления атомов данного элемента: Na2  O3 + 2Na2
O3 + 2Na2  + 6HCl = 3
+ 6HCl = 3 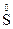 + 6NaCl + 3H2O
+ 6NaCl + 3H2O
5. Существуют также реакции смешанного типа. Например, к внутримолекулярной реакции контрпропорционирования относится реакция разложения нитрата аммония:  H4
H4  O3
O3 
 2O + 2H2O
2O + 2H2O
Составление уравнений. Для составления уравнений окислительно-восстановительных реакций наиболее часто используют метод электронно-ионных полуреакций и метод электронного баланса. Метод электронно-ионных полуреакций применяют при составлении уравнений реакций, протекающих в водном растворе, а также реакций с участием веществ, в которых трудно определить степени окисления элементов (например, KNСS, CH3CH2OH). Согласно этому методу выделяют следующие главные этапы составления уравнения реакций:
1. Записывают общую молекулярную схему процесса с указанием восстановителя, окислителя и среды, в которой протекает реакция (кислотная, нейтральная или щелочная). Например:
SO2 + K2Cr2O7 + H2SO4(разб) ®...
2. Учитывая диссоциацию электролитов в водном растворе, данную схему представляют в виде молекулярно-ионного взаимодействия. Ионы, степени окисления атомов которых не изменяются, в схеме не указывают, за исключением ионов Н+ и ОН-:
SO2 + Cr2O72– + H+ ®...
3. Определяют степени окисления восстановителя и окислителя, а также продуктов их взаимодействия:
| Окисление восстановителя | Восстановление окислителя |
 ® ® 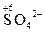 |  ® 2Cr3+ ® 2Cr3+ |
4. Записывают материальный баланс полуреакции окисления и восстановления:
| Окисление восстановителя | Восстановление окислителя |
 + 2H2O – 2 e = + 2H2O – 2 e = 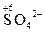 + 4H+ + 4H+ |  + 14H+ + 6 e = 2Cr3+ + 7H2O + 14H+ + 6 e = 2Cr3+ + 7H2O |
5. Суммируют полуреакции, учитывая принцип равенства отданных и принятых электронов:
3∙ôSO2 + 2H2O – 2 e =  + 4H+
+ 4H+
1∙ô  + 14H+ + 6 e = 2Cr3+ + 7H2О
+ 14H+ + 6 e = 2Cr3+ + 7H2О
3  + 6H2O +
+ 6H2O +  + 14H+ = 3
+ 14H+ = 3  + 12H+ + 2Cr3+ + 7H2О
+ 12H+ + 2Cr3+ + 7H2О
и, сокращая одноименные частицы, получают общее ионно-молекулярное уравнение:
3  +
+  + 2H+ = 3
+ 2H+ = 3  + 2Cr3+ + H2О.
+ 2Cr3+ + H2О.
6. Добавляют ионы, не участвовавшие в процессе окисления-восстановления, уравнивают их количества слева и справа, и записывают молекулярное уравнение реакции:
3SO2 + K2Cr2O7 + H2SO4 (разб) = Cr2(SO4)3 + K2SO4 + H2O.
При составлении материального баланса полуреакций окисления и восстановления, когда изменяется число атомов кислорода, входящих в состав частиц окислителя и восстановителя, следует учитывать, что в водных растворах связывание или присоединение кислорода происходит с участием молекул воды и ионов среды.
В процессе окисления на один атом кислорода, присоединяющийся к частице восстановителя, в кислотной и нейтральной средах расходуется одна молекула воды и образуются два иона Н+; в щелочной среде расходуются два гидроксид-иона ОН- и образуется одна молекула воды (табл.8.1).
Таблица 8.1. Присоединение атомов кислорода к восстановителю в процессе окисления
| Среда | Частицы, участвующие в присоединении одного атома кислорода | Образующиеся частицы | Примеры полуреакций окисления |
| Кислотная, нейтральная | Н2О | 2Н+ | SO32– + H2O – 2 e = SO42– + 2H+ SO2 + 2H2O – 2 e = SO42– + 4H+ |
| Щелочная | 2ОН- | Н2О | SO32– + 2OH- – 2 e = SO42– + H2O SO2 + 4OH- – 2 e = SO42– + 2H2O |
В процессе восстановления для связывания одного атома кислорода частицы окислителя в кислотной среде расходуются два иона Н+ и образуется одна молекула воды; в нейтральной и щелочной средах расходуется одна молекула Н2О и образуются два иона ОН- (табл.1.2).
Таблица 8.2. Связывание атомов кислорода окислителя в процессе восстановления
| Среда | Частицы, участвующие в связывании одного атома кислорода | Образующиеся частицы | Примеры полуреакций восстановления |
| Кислотная | 2Н+ | Н2О |  + 14H+ + 6e = 2Cr3+ + 7H2О MnO4- + 8H+ +5 e = Mn2+ + 4H2O + 14H+ + 6e = 2Cr3+ + 7H2О MnO4- + 8H+ +5 e = Mn2+ + 4H2O |
| Нейтральная, щелочная | Н2О | 2ОН- | CrO42-+4H2O +3 e =[Cr(OH)6]3- + 2ОН- MnO4- +3H2O+3 e = MnO(OH)2 + 4OH- |
Метод электронного баланса обычно используют для составления уравнений окислительно-восстановительных реакций, протекающих между газами, твердыми веществами и в расплавах. Последовательность операций следующая:
1. Записывают формулы реагентов и продуктов реакции в молекулярном виде:
FeCl3 + H2S ® FeCl2 + S + HCl;
2. Определяют степени окисления атомов, меняющих ее в процессе реакции:
 Cl3 + H2
Cl3 + H2  ®
®  Cl2 +
Cl2 + 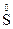 + HCl;
+ HCl;
3. По изменению степеней окисления устанавливают число электронов, отдаваемых восстановителем, и число электронов, принимаемых окислителем, и составляют электронный баланс с учетом принципа равенства числа отдаваемых и принимаемых электронов: 2∙ ½  +1 e =
+1 e = 
1∙ ½  – 2 e =
– 2 e = 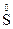
4. Множители электронного баланса записывают в уравнение окислительно-восстановительной реакции как основные стехиометрические коэффициенты: 2FeCl3 + H2S ® 2FeCl2 + S + HCl
5. Подбирают стехиометрические коэффициенты остальных участников реакции: 2FeCl3 + H2S = 2FeCl2 + S + 2HCl.
6. При составлении уравнений следует учитывать, что окислитель (или восстановитель) могут расходоваться не только в основной окислительно-восстановительной реакции, но и при связывании образующихся продуктов реакции, т.е. выступать в роли среды и солеобразователя. Примером, когда роль среды играет окислитель, служит реакция окисления металла в азотной кислоте, составленная методом электронно-ионных полуреакций:
Cu + HNO3(разб) ®...
Cu + NO3- + H+ ®...
3∙ ½ Cu – 2 e = Cu2+
2∙ ½ NO3- + 4H+ + 3 e = NO + 2H2O
3Cu + 2NO3- + 8H+ = 3Cu2+ + 2NO + 4H2O
3Cu + 2HNO3(окислитель) + 6HNO3(среда) = 3Cu(NO3)2 + 2NO + 4H2O
или 3Cu + 8HNO3(разб) = 3Cu(NO3)2 + 2NO + 4H2O.
Примером, когда восстановитель является средой, в которой протекает реакция, служит реакция окисления соляной кислоты дихроматом калия, составленная методом электронного баланса:
HCl + K2Cr2O7 ® CrCl3 + Cl2 + KCl + H2O
H  + K2
+ K2  2O7 + HCl ®
2O7 + HCl ®  Cl3 +
Cl3 + 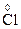 2 + KCl + H2O
2 + KCl + H2O
6∙ ½  – 1 e =
– 1 e = 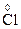
2∙ ½  + 3 e =
+ 3 e = 
6 HCl(восстановитель) + K2Cr2O7 + HCl(среда) ® 2CrCl3 + 3Cl2 + KCl + H2O
6 HCl + K2Cr2O7 + 8HCl = 2CrCl3 + 3Cl2 +2 KCl + 7H2O
или 4HCl + K2Cr2O7 = 2CrCl3 + 3Cl2 +2 KCl + 7H2O
При расчете количественных, массовых и объемных соотношений участников окислительно-восстановительных реакций, используют основные стехиометрические законы химии, и, в частности, закон эквивалентов, учитывая, что число эквивалентности окислителя равно числу электронов, которые принимает одна формульная единица окислителя, а число эквивалентности восстановителя равно числу электронов, которые отдает одна формульная единица восстановителя.
Окисление-восстановление – это единый взаимосвязанный процесс. Атом элемента в своей высшей степени окисленности не может ее повысить (отдавать электроны) и проявляет только окислительные свойства, а в своей низшей степени окисленности не может ее понизить (принять электроны) и проявляет только восстановительные свойства. Атом же элемента, имеющий промежуточную степень окисленности, может проявлять как окислительные, так и восстановительные свойства.
Например:
N 5+ (HNO 3) проявляет только окислительные свойства;
N 4+ (NO 2) проявляет окислительные и восстановительные свойства;
N 3+ (HNO 2) проявляет окислительные и восстановительные свойства;
N 2+ (NO) проявляет окислительные и восстановительные свойства;
N 1+ (N 2 O) проявляет окислительные и восстановительные свойства;
N 0 (N 2) проявляет окислительные и восстановительные свойства;
N 1- (NH 2 OH) проявляет окислительные и восстановительные свойства;
N 2- (N 2 H 2) проявляет окислительные и восстановительные свойства;
N 3- (NH 3) проявляет только восстановительные свойства.
Пример 1. Исходя из степени окисленности (n) азота, серы и марганца в соединениях NH 3 HNO 2 HNO 3 H 2 S H 2 SO 3 H 2 SO 4 MnO 2 KMnO 4, определите какие из них могут быть только восстановителями, только окислителями, и какие проявляют как окислительные, так и восстановительные свойства.
Решение. Степень окисленности для азота в указанных соединениях соответственно равна: -3 (низшая), +3 (промежуточная), +5 (высшая); n для серы соответственно равна –2 (низшая), +4 (промежуточная), +6 (высшая); n для марганца соответственно равна +4 (промежуточная), +7 (высшая). Отсюда: NH 3, H 2 S – только восстановители; HNO 3, H 2 SO 4, KMnO 4 – только окислители; HNO 2, H 2 SO 3, MnO 2 – окислители и восстановители.
Пример 2. Составьте уравнение окислительно-восстановительной реакции идущей по схеме
+3 +7 +2 +5
H 3 PO 3 +KMnO 4 +H 2 SO 4 =MnSO 4 +H 3 PO 4 +K 2 SO 4 +H 2 O
Решение. Если в условии задачи даны как исходные вещества, так и продукты их взаимодействия, то написание уравнения реакции сводится, как правило, к нахождению и расстановке коэффициентов. Коэффициенты определяют методом электронного баланса с помощью электронных уравнений. Вычисляем, как изменяет свою степень окисленности восстановитель и окислитель, и отражаем это в электронных уравнениях:
 восстановитель 5 P 3+ - 2e - = P 5+ - процесс окисления
восстановитель 5 P 3+ - 2e - = P 5+ - процесс окисления
окислитель 2 Mn 7+ + 5e - = Mn 2+ - процесс восстановления
Общее число электронов отданных восстановителем, должно быть равно числу электронов, которое присоединяет окислитель. Общее наименьшее кратное для отданных и принятых электронов десять. Разделив это число на 5, получаем коэффициент 2 для окислителя, а при делении 10 на 2 получаем коэффициент 5 для восстановителя. Коэффициент перед веществами, атомы которых не меняют свою степень окисленности, находят подбором. Уравнение реакции будет иметь вид:
5H 3 PO 3 +2KMnO 4 +3H 2 SO 4 =2MnSO 4 +5H 3 PO 4 +K 2 SO 4 +3H 2 O
Пример 3. Составьте уравнение реакции взаимодействия цинка с концентрированной серной кислотой, учитывая максимальное восстановление последней.
Решение. Цинк, как и любой металл, проявляет только восстановительные свойства.
В концентрированной серной кислоте окислительную функцию несет сера (+6). Максимальное восстановление серы означает, что приобретает минимальную степень окисленности. Минимальная степень окисленности серы как элемента VI группы равна –2. Цинк как металл II группы имеет постоянную степень окисленности +2. Поэтому электронные уравнения будут иметь вид:
 восстановитель 4 Zn 0 - 2e - = Zn 2+ - процесс окисления
восстановитель 4 Zn 0 - 2e - = Zn 2+ - процесс окисления
окислитель 1 S 6+ + 8e - = S 2- - процесс восстановления
Составляем уравнение реакции:
4Zn+5H 2 SO 4 =4ZnSO 4 +H 2 S+4H 2 O
Перед H 2 SO 4 стоит коэффициент 5, а не 1, так как четыре молекулы H 2 SO 4 идут на связывание четырех ионов Zn 2+.
Пример 5. Определите типы окислительно-восстановительных реакций для следующих процессов:
а) H 2 S+ HNO 3 = H 2 SO 4 + NO 2 + H 2 O
б) H 3 PO 3 = H 3 PO 4 + PH 3
в) (NH 4) 2 Cr 2 O 7 =N 2 + Cr 2 O 3 + H 2 O
Решение.
2- 5+ 6+ 4+
а) H 2 S+8HNO 3 = H 2 SO 4 +8NO 2 +4H 2 O

 восстановитель 1 S 2- - 8e - = S 6+ - процесс окисления
восстановитель 1 S 2- - 8e - = S 6+ - процесс окисления
окислитель 8 N 5+ +1e - = N 4+ - процесс восстановления
В этой реакции взаимодействуют два вещества, одно из которых служит восстановителем, а другое – окислителем. Такие реакции относятся к реакциям межмолекулярного окисления-восстановления.
3+ 5+ 3-
б) 4H 3 PO 3 =3H 3 PO 4 + PH 3

 восстановитель 3 P 3+ -2e - =P 5+ процесс окисления
восстановитель 3 P 3+ -2e - =P 5+ процесс окисления
 4{
4{
окислитель 1 P 3+ +6e - =P 3- процесс восстановления
В этой реакции исходное вещество проявляет функции как окислителя, так и восстановителя. Такие реакции являются реакциями самоокисления-самовосстановления (диспропорционирования).
3- 6+ 0 3+
в) (NH 4) 2 Cr 2 O 7 = N 2 + Cr 2 O 3 + H 2 O
 восстановитель 1 2N 3- - 6e - = 2N 0 - процесс окисления
восстановитель 1 2N 3- - 6e - = 2N 0 - процесс окисления
окислитель 1 2Cr 6+ + 6e - = 2Cr 3+ - процесс восстановления
В этой реакции и окислитель, и восстановитель входят в состав одного и того же вещества. Реакции такого типа называются реакциями внутримолекулярного окисления-восстановления.
211. Какие из приведенных реакций являются окислительно-восстановительными? Укажите для каждой из них окислитель и восстановитель. а)Fe + 2HCl = FeCl2 + H2; б) FeCl2 + 2NaOH = Fe(OH)2 + 2NaCl; в) Ba(NO3)2 + K2SO4 = BaSO4 + 2KNO3; г) 2KI + Cl2 = 2KCl + I2
212. Какой процесс окисления или восстановления происходит при следующих превращениях: 

 ;
; 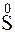

 ;
; 

 ;
; 

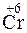 ;
; 

 ;
; 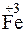

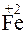 ?
?
213. Реакция выражается схемами: а) KClO3  KClO4 + KCl; б) (NH4)2S + K2Cr2O7 + H2O
KClO4 + KCl; б) (NH4)2S + K2Cr2O7 + H2O  S + Cr(OH)3 + NH3 + KOH. Составьте электронные уравнения, расставьте коэффициенты, укажите окислитель и восстановитель.
S + Cr(OH)3 + NH3 + KOH. Составьте электронные уравнения, расставьте коэффициенты, укажите окислитель и восстановитель.
214. Диоксид азота при растворении в воде образует смесь двух кислот. Напишите уравнение реакции и составьте уравнения электронного баланса.
215. Рассмотрите восстановительную способность щелочных металлов на примере взаимодействия лития с кислородом, водородом, хлором, серой, азотом, углеродом и водой.
216. Почему пероксид водорода может проявлять как окислительные, так и восстановительные свойства? На основании электронных уравнений напишите реакции взаимодействия пероксида водорода с диоксидом свинца в азотнокислой среде, с сульфидом свинца в нейтральной среде.
217. Допишите уравнения реакций: а) Na2O2 + KI + H2SO4 ® …; б) Na2O2 + Fe(OH)2 + H2O ® …; в) Na2O2 + KMnO4 + H2SO4 ® …; г) Na2O2 + H2O ® …; д) Na2O2 + H2SO4 ®… Окислителем или восстановителем является пероксид натрия в этих реакциях?
218. Напишите реакции получения нитрида и гидроксида бария и разложения их водой. К окислительно-восстановительным реакциям составьте электронные уравнения.
219. Почему хлор способен к реакциям самоокисления-самовосстановления (диспропорционирования)? На основании электронных уравнений напишите реакцию растворения хлора в едком натре.
220. На основании электронных уравнений составьте уравнение реакции взаимодействия серы с азотной кислотой, учитывая, что сера окисляется максимально, а азот восстанавливается минимально.
221. Напишите формулы и назовите оксиды азота, укажите степени окисления азота в каждом из них. Какой из этих оксидов более сильный окислитель? На основании электронных уравнений закончите уравнение реакции, учитывая, что азот приобретает минимальную степень окисления: KNO2 + Al + KOH + H2O = KAlO2 + …
222. Какие степени окисления проявляет марганец в соединениях? Составьте формулы оксидов марганца, отвечающих этим степеням окисления. Как меняются кислотно-основные свойства оксидов марганца при переходе от низшей к высшей степени окисления? Составьте уравнения реакций взаимодействия оксида марганца (II) с серной кислотой и оксида марганца(III) с гидроксидом калия.
223. Составьте электронные и молекулярные уравнения реакций растворения золота в царской водке и взаимодействия вольфрама с хлором. Золото окисляется до степени окисления (+3), а вольфрам - до максимальной.
224. Через подкисленный серной кислотой раствор дихромата калия пропустили газообразный сероводород. Через некоторое время оранжевая окраска перешла в зеленую и одновременно жидкость стала мутной. Составьте молекулярное и электронное уравнения происходящей реакции, учитывая минимальное окисление сероводорода.
225. Расставьте коэффициенты методом электронного баланса в следующем уравнении: NaCrO2 + Br2 + NaOH → Na2CrO4 + NaBr + H2O.
226. Составить уравнение реакции сульфида мышьяка (III) As2S3 с концентрированной азотной кислотой по схеме: A2S2 + NO3– → AsO43– + SO42– + NO2 + H2O.
227. Сколько граммов FeSO4 можно окислить в присутствии H2SO4 с помощью 100 мл 0,25 н. раствора K2CrO4?
228. Соединения меди, серебра и золота хорошие окислители. Почему? Составьте электронные и молекулярные уравнения реакций: а) CuO + NH4Cl → N2 + …; б) Ag2O + Cr(OH)3 + NaOH → …; в) Au2O3 + H2O2 →…
229. Подберите коэффициенты методом электронно-ионного баланса в уравнении окислительно-восстановительной реакции: KMnO4 + H2SO4 + Na2SO3 → MnSO4 + H2O + Na2SO4 + …
230. Подберите коэффициенты методом электронно-ионного баланса в уравнении окислительно-восстановительной реакции: Na2SO3 + KOH + KMnO4 → Na2SO4 + H2O + K2MnO4
231. Подберите коэффициенты в уравнении реакции, протекающей в нейтральной среде: KMnO4 + H2О + Na2SO3 → MnО2(т) + Na2SO4 + …
232. Подберите коэффициенты в уравнении реакции, протекающей в слабокислотной среде: KMnO4 + H2SO4 + Na2SO3 → MnО2(т) + H2O + Na2SO4 + …
233. Напишите уравнение реакции окисления дисульфида железа (II) концентрированной азотной кислотой. Составьте: схемы электронного и электронно-ионного баланса.
234. Напишите уравнения реакций, протекающих в водной среде: а) Na2SО3 + КМnО4 + Н2SО4 → X + …; б) Х + КОН →...
235. Могут ли проходить окислительно-восстановительные реакции между следующими веществами: а) H 2 S и HI; б) H 2 S и H 2 SO 3; в) H 2 SO 3 и HClO 4?
236. Определите типы окислительно-восстановительных реакций для следующих процессов: а) H 2 S+ HNO 3 = H 2 SO 4 + NO 2 + H 2 O; б) H 3 PO 3 = H 3 PO 4 + PH 3; в) (NH 4) 2 Cr 2 O 7 =N 2 + Cr 2 O 3 + H 2 O
237. Какие из указанных ниже соединений могут проявлять только окислительные свойства: CrSO4; K2CrO4; NaCrO2. Ответ обосновать.
238. Укажите, какие из приведенных процессов являются процессами окисления: а) SO2 → S2–; б) ClO– → Cl–; в) CrO2– → CrO42–
239. Укажите, какие из реакций являются окислительно-восстановительными: а) 2Al + Cr2O3 → Al2O3 + 2Cr; б) Al2(SO4)3 + 6 NaOH → 2Al(OH)3 + 3Na2SO4; в) Al(OH)3 + NaOH → Na[Al(OH)4]. Ответ обосновать.
240. Уравняйте методом электронного баланса уравнения окислительно-восстановительных реакций и укажите количество молекул окислителя: Na2MoO4 + HCl + Al → MoCl2 + AlCl3 + NaCl + H2O
 2015-10-22
2015-10-22 3023
3023
