В настоящее время с целью создания эффективных противоопухолевых препаратов активно изучается группа полипептидных токсинов высших растений, действие которых обусловлено, как принято считать, ингиби-рованием синтеза белка в клетках млекопитающих. К ним относятся аб-рин, модецин, кротин, рицин и другие вещества, сходные по молекулярной массе, структуре и характеру биологического действия.
Одним из наиболее изученных и токсичных представителей группы является рицин, рассматривавшийся ранее на предмет возможности использования в качестве боевого отравляющего вещества (В. В. Мясников, 1989; Курочкин и соавт., 1994).
Рицин
Рицин в большом количестве (до 3%) содержится в бобах клещевины обыкновенной (Ricinus communis L), откуда его и извлекают методом экстракции.
Физико-химические свойства. Токсичность
Рицин относится к классу лектинов — растительных гликопротеидов, in vitro агглютинирующих клетки млекопитающих в результате избирательного связывания с углеводными компонентами поверхности клеточной мембраны. Белок этот состоит из двух полипептидных цепей, соединенных дисульфидной связью. А-цепь состоит из 265 аминокислот и 6 углеводных фрагментов. Молекулярная масса А-цепи — 32 ООО дальтон. В-цепь рицина состоит из 260 аминокислот, фрагментов глюкозамина и маннозы. Молекулярная масса В-цепи равна 34 ООО дальтон.
Очищенный рицин представляет собой белый, не имеющий запаха, легко диспергируемый в воздухе и растворимый в воде порошок. Вещество малоустойчиво в водных растворах и при хранении постепенно теряет токсичность. При низких температурах водные растворы сохраняются достаточно долго.
Рицин токсичен для большинства видов теплокровных животных. Расчетная смертельная доза вещества для человека при приеме через рот составляет около 0,3 мг/кг. При ингаляции мелкодисперсного аэрозоля его токсичность значительно выше. Через неповрежденную кожу рицин не оказывает токсического действия.
Токсикокинетика
Вещество легко проникает в организм через легкие, значительно хуже — через желудочно-кишечный тракт. Взаимодействуя с клетками, формирующими альвеолярно-капиллярный барьер и слизистую оболочку ЖКТ, рицин повреждает их. Попав в кровь, вещество распределяется в организме. Через гематоэнцефалический барьер проникает плохо. Значительная его часть быстро фиксируется на поверхности эритроцитов, клеток эндотелия различных органов и тканей. Время пребывания несвязанной формы токсина в крови не превышает нескольких минут. Токсикант разрушается при участии протеолитических ферментов.
Основные проявления интоксикации
Сведения о токсическом действии рицина скудны. Они получены главным образом при изучении случаев отравления людей клещевиной, а также в экспериментах на лабораторных животных. Признаки поражения проявляется, как правило, через сутки — трое после попадания вещества в организм. Даже значительное увеличение дозы токсиканта не приводит к существенному сокращению продолжительности скрытого периода. Проявления интоксикации складываются из картины местного и резорб-тивного действия, в основе которого лежат цитотоксический и цитостатический эффекты, нарушение процессов метаболизма в клетках, с которыми вещество вступает в контакт.
При заглатывании семян клещевины животными или людьми через 10-12 ч или позднее появляются признаки сильного раздражения желудочно-кишечного тракта: тошнота, рвота, сильные боли в животе, приступы кишечной колики, профузный понос (часто с кровью). Позже развиваются лихорадка, головная боль, цианоз кожных покровов, появляется чувство жажды, артериальное давление падает, пульс частый слабого наполнения, выступает холодный пот. В крайне тяжелых случаях на высоте интоксикации (на вторые — третьи сутки) наблюдаются судорожный синдром, признаки поражения печени (желтуха) и почек (альбуминурия, гематурия, уменьшение количества отделяемой мочи вплоть до анурии). При смертельных интоксикациях летальный исход наступает, как правило, на 2—7-е сут. Для несмертельного отравления клещевиной характерно затяжное течение, проявляющееся гипертермией, гиподинамией, заторможенностью, прогрессирующей слабостью, анорексией, поносом, истощением.
Описан случай имплантации частиц бобов клещевины под кожу голени с целью умышленного членовредительства. Через 12—24 ч у отравленного наблюдались сильный озноб, повышение температуры тела до 39-41° С, сильная головная боль и общая слабость. Через 7 сут на месте введения образовалась глубокая, болезненная язва, не заживавшая более 2 лет.
Пыль, образующаяся при переработке клещевины и других растений, содержащих токсичные лектины, может вызывать конъюнктивит, острый ринит, фарингит, хроническое воспаление бронхов. У пострадавших наблюдаются слезотечение, головная боль, кашель, одышка со свистящим дыханием и т. д. При попадании порошкообразного рицина в глаза развивается воспалительный процесс, переходящий в тяжелый панофталь-мит.
Характерно аллергизирующее действие рицина. Человек, однажды подвергшийся действию пыли, содержащей вещество, становится чувствительным к ничтожным количествам токсиканта.
В эксперименте установлена высокая ингаляционная токсичность рицина. При поражении аэрозолем в высокой концентрации у животных развиваются тяжелое острое воспаление слизистой оболочки дыхательных путей с перибронхиальным отеком ткани, переходящее в гнойный трахеобронхит, крайне тяжелая очаговая пневмония, завершающаяся некрозом легочной ткани.
Резорбтивное действие рицина при его системном введении экспериментальным животным проявляется выраженным нарушением проницаемости сосудов, изменениями со стороны системы крови, деструктивными процессами в печени, почках, миокарде. У отравленных животных обнаруживаются умеренный отек легких и кровоизлияния в легочную ткань, гидроторакс, экссудативный плеврит, отек мозга, асцит, выраженный геморрагический гастроэнтероколит, кровоизлияния во внутренние органы. В основе нарушения сосудистой проницаемости лежат повреждение эндотелиальных клеток, а также деструктивные изменения стенок сосудов.
У крыс, отравленных рицином, уже в первые часы после воздействия наблюдаются морфологические признаки активации ретикуло-эндотели-альных элементов печени в виде их гипертрофии и гиперплазии, затем отмечаются некротические изменения синусных клеток, а затем жировое перерождение и некроз гепатоцитов. Участки некроза располагаются как в центральных, так и в периферических отделах печеночных долек. В почках в выделительных канальцах первого и второго порядка выражена дистрофия эпителия. В сердечной мышце выявляются признаки острого очагового миокардита.
В крови отравленных лабораторных животных (на 3-й — 20-е сут) отмечаются умеренный гемолиз, стойкий нейтрофильный лейкоцитоз, лимфоцитоз, моноцитоз. Изменяются реологические свойства крови. Повышается уровень фибриногена в крови, активируется система превращения фибриногена в фибрин. Складываются условия для диссеми-нированного внутрисосудистого свертывания крови.
Механизм токсического действия
Всю совокупность токсических процессов, развивающихся при поражении рицином, можно объяснить повреждением клеток различных органов и тканей. В токсическом действии рицина на клетки можно выделить три периода: фиксации токсина на мембране клеток, проникновения в клетку, повреждения клетки.
Фиксация рицина на мембране клеток осуществляется путем взаимодействия В-цепи молекулы с рецепторами, активно связывающими лектины. Центры связывания имеются в клетках различных типов, однако количество таких центров на поверхности мембран различных клеток неодинаково. Этим объясняется и неодинаковая чувствительность различных клеточных популяций к токсиканту. Так, в опытах in vitro установлено, что у лимфоцитов и некоторых других соматических клеток количество участков связывания рицина достигает 106— 108 на клетку, У эритроцитов — значительно меньше. Связывание токсина клетками in vitro существенно блокируется лактозой.
Проникновение токсина, фиксировавшегося на поверхности мембраны, в клетку осуществляется путем эндоцитоза. Вещества, усиливающие проницаемость биологических мембран (нигерицин), in vitro в несколько раз увеличивают цитотоксическое действие рицина. Внутри клетки молекула токсина разрушается с высвобождением А-цепи, которая и оказывает повреждающее действие.
Основной «точкой приложения» А-цепи рицина являются рибосомы, а именно их 60-S (большие) субъединицы. Как известно, процесс трансляции — синтез полипептидных цепей на матрице информационной РНК согласно генетическому коду — осуществляется преимущественно на рибосомах сложным комплексом макромолекул. Этот комплекс, помимо рибосомальных макромолекул, включает: информационные РНК, транспортные РНК, аминоацил-тРНК-синтетазы, а также белковые факторы инициации (начала) синтеза, элонгации (удлинения) полипептидной цепи, терминации (окончания) процесса. Рицин связывается с рибосомами в той их области, где последние взаимодействуют с факторами элонгации (ФЭ-1 и ФЭ-2). В результате удлинение формируемых на рибосомах полипептидных цепей прекращается — нарушается синтез белка в клетке и она погибает. Синергистами токсического действия рицина являются ингибиторы синтеза белка с иными механизмами повреждающего действия, в частности, актиномицин Д, который нарушает процесс транскрипции (ДНК-зависимый синтез информационной РНК в клетках), задерживая продвижение РНК-полимеразы вдоль цепи ДНК.
По некоторым данным, рицин выводит из строя эндогенные ингибиторы протеолиза в клетках, активирует протеолитические процессы, инициируя разрушение клеточных белков, что также приводит к гибели клеток.
Рицин, как и другие лектины, действуя в малых дозах, является сильным митогеном, активирующим клеточное деление и, в частности, пролиферацию популяции Т-лимфоцитов в организме. Не исключено, что повреждение клеток органов и тканей, наблюдаемое при отравлении, может быть также следствием атаки на них активированных Т-киллеров, других фагоцитирующих элементов иммунной системы.
Мероприятия медицинской защиты
Специальные санитарно-гигиенические мероприятия:
• использование индивидуальных технических средств защиты (средства защиты органов дыхания) в зоне химического заражения;
• участие медицинской службы в проведении химической разведки в районе расположения войск, проведение экспертизы воды и продовольствия на зараженность ОВТВ;
• запрет на использование воды и продовольствия из непроверенных источников;
• обучение личного состава правилам поведения на зараженной местности.
Специальные профилактические медицинские мероприятия:
• проведение санитарной обработки пораженных на передовых этапах медицинской эвакуации.
Специальные лечебные мероприятия:
•своевременное выявление пораженных;
• оказание первой, доврачебной и первой врачебной (элементы) помощи пострадавшим;
• подготовка и проведение эвакуации.
Помощь пораженным оказывается по общим правилам с использованием этиотропных и патогенетических средств терапии состояний, развивающихся после воздействия яда (см. 6.4. «Основные принципы оказания первой, доврачебной и первой врачебной помощи при острых отравлениях»). Для ослабления местного действия рицина на догоспитальном этапе пораженным необходимо тщательно промыть глаза, обработать слизистые оболочки носоглотки и полости рта водой, раствором соды или физиологическим раствором. При пероральном отравлении с целью оказания помощи показано промывание желудка. При болях в глазах, по ходу желудочно-кишечного тракта показано назначение местных анестетиков. Поскольку токсический процесс развивается медленно, имеется резерв времени для эвакуации пораженных в специализированные лечебные учреждения.
Специальные табельные средства медицинской защиты отсутствуют. Существует теоретическая возможность разработки таких средств. Поскольку рицин является полным антигеном, возможно создание специфических антитоксических сывороток. Использование таких препаратов с профилактической целью могло бы оказывать защитное действие. Однако их лечебное применение будет затруднено, так как рицин быстро элиминируется из крови отравленных.
Тиоловые яды
К тиоловым ядам относятся вещества, в основе механизма токсического действия которых лежит способность связываться с сульфгидрильными группами, входящими в структуру большого количества биологических молекул, среди которых: структурные белки, энзимы, нуклеиновые кислоты, регуляторы биологической активности и т. д. В частности, к числу ферментов, содержащих сульфгидрильные группы, относятся: гидролазы (амилаза, липаза, холинэстераза, уреаза и др.), оксидоредуктазы (алко-гольдегидрогеназа, аминоксидазы, дегидрогеназы яблочной, янтарной, олеиновой кислот и др.), фосфатазы (аденозинтрифосфатаза, миокиназа, креатинфосфокиназа, гексокиназа и др.), ферменты антирадикальной защиты клетки (глутатионпероксидаза, глутатионредуктаза, глутатион-S-трансфераза, каталаза). Рибосомы клеток млекопитающего содержат около 120 сульфгидрильных групп, причем примерно половина из них имеет функциональное значение для осуществления белкового синтеза. Гормоны полипептидной структуры, такие как инсулин и глюкагон, также содержат сульфгидрильные группы в молекулах и т. д.
Образование комплекса токсиканта с SH-группами биомолекул сопровождается их повреждением, нарушением функции, что и инициирует развитие токсического процесса.
К числу тиоловых ядов прежде всего относятся металлы: мышьяк, ртуть, цинк, хром, никель, кадмий, и их многочисленные соединения. Сродство различных тиоловых ядов к разным соединениям, содержащим SH-группы, неодинаково. Неодинакова и токсикокинетика ядов. Этим объясняются различия токсичности веществ и особенности формирующегося токсического процесса. Среди веществ рассматриваемой группы для военной медицины наибольший интерес представляют соединения мышьяка.
Соединения мышьяка
Мышьяксодержащие вещества широко используются в медицине, а также в качестве пестицидов (инсектицидов и гербицидов), осушителей в производстве изделий из хлопка, консервантов древесины, пищевых добавок в рацион некоторых животных и т. д. Хотя случаи массовых интоксикаций соединениями мышьяка в настоящее время редки, сохраняется потенциальная возможность таких инцидентов. Так, в Японии (1972 г.) более 12 тыс детей получили отравление консервированным молоком, зараженным мышьяком. Случай привел к гибели 130 человек. Широкое применение мы-шьяксодержащих веществ в хозяйственной деятельности, их доступность делают возможным их применение с террористическими целями.
На основе мышьяка в начале XX в. были созданы высокотоксичные боевые отравляющие вещества, запасы которых в настоящее время подлежат уничтожению.
Мышьяк (As) — переходный элемент V группы периодической системы, металлоид, атомный номер 33, атомная масса 74,9. В природе встречается в виде минералов: ауропигмент (AS2O3), реальгар (AS4S4), арсенопирит (FeAsS), примесей к рудам различных металлов. Способен пчаимодсйствовать с углеродом, водородом, кислородом, хлором, серой и образовывать многочисленные соединения.
По особенностям строения и биологической активности соединения мышьяка подразделяют на 3 основные группы:
в) арсин (ASH3).
К настоящему времени синтезировано более 6000 неорганических и органических соединений мышьяка. В группе неорганических соединений выделяют соединения трехвалентного (As+3 — арсениты — триоксид мышьяка, арсенит натрия, трихлорид мышьяка и т. д.) и пятивалентного (As+5 — арсенаты) мышьяка (пятиокись мышьяка, мышьяковая кислота и т. д.).
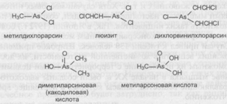
Среди органических соединений также различают вещества, в которых мышьяк может находиться в трех- и пятивалентном состоянии. Кроме того, выделяют алкильные и арильные органические производные этого элемента (рис. 37). К числу наиболее опасных органических соединений трехвалентного мышьяка относятся хлорсодержащие алкильные производные — метилдихлорарсин, этилдихлорарсин, дихлорвинилхло-рарсин, трихлорвиниларсин и р-хлорвинилдихлорарсин — известное боевое отравляющее вещество кожно-нарывного действия (люизит). Арильные производные трехвалентного мышьяка, представляющие интерес для военной медицины, это прежде всего вещества, раздражающие носоглотку, например адамсит (фенарсазинхлорид) — боевое отравляющее вещество (см. гл. 8. «Отравляющие и высокотоксичные вещества раздражающего действия»).
Представителями группы органических производных пятивалентного мышьяка являются, в частности, метиларсоновая кислота, диметиларси-новая кислота (какодиловая кислота). Последнее вещество входило в состав «голубой жидкости», применявшейся американскими войсками в период Вьетнамской войны (70-е гг. XX в.) в качестве фитотоксиканта.
Некоторые соединения мышьяка обладают высокой биологической активностью при местном и резорбтивном действии на организм. При резорбции наиболее токсичными являются арсин (ASH3 — см. гл. 10. «Отравляющие и высокотоксичные вещества общеядовитого действия»), хлорсодержа-щие органические соединения трехвалентного мышьяка (люизит, этилдих-лорарсин и др.), а также неорганические соединения трехвалентного мышьяка (арсенит натрия, триоксид мышьяка). Менее токсичны неорганические соединения пятивалентного мышьяка (арсенат натрия, пятиокись мышьяка). Органические соединения пятивалентного мышьяка (какодиловая кислота, метиларсоновая ксилота и др.) по большей части относятся к числу малотоксичных соединений.
При местном действии наивысшей активностью обладает люизит (вызывает воспалительные изменения покровных тканей) и ароматические производные трехвалентного мышьяка (адамсит — раздражающее действие на слизистые оболочки глаз и дыхательных путей).
Токсические процессы, развивающиеся в результате острого действия неорганических соединений мышьяка и металлорганических соединений, имеют существенные особенности.
 2017-12-16
2017-12-16 1074
1074
